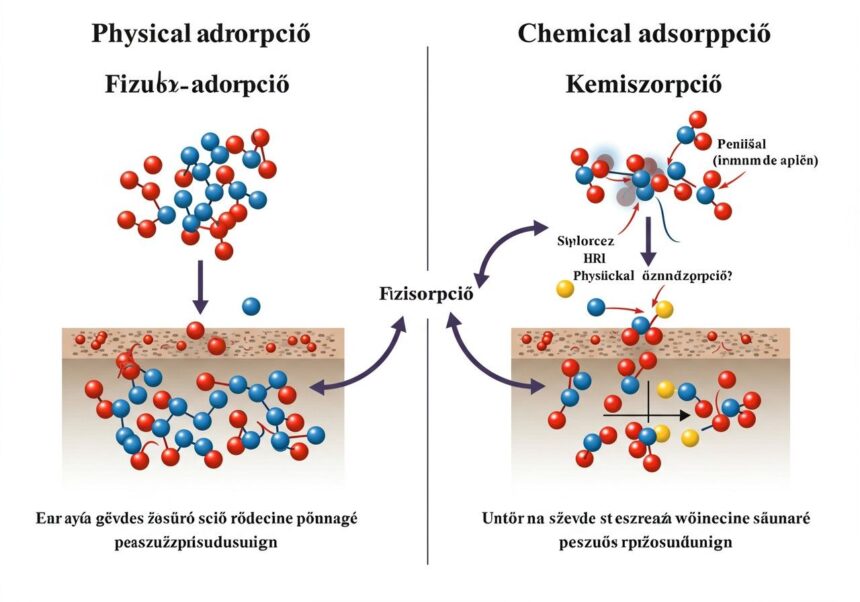
Az anyagok felületi jelenségei az anyagtudomány, a kémia és a fizika egyik legizgalmasabb és legfontosabb területe, amely alapjaiban határozza meg, hogyan lépnek kölcsönhatásba az anyagok egymással, különösen szilárd felületek és gáz- vagy folyadékfázisú molekulák között. Ezen interakciók közül az adszorpció kiemelten fontos, hiszen számos természeti folyamatban és ipari technológiában kulcsszerepet játszik. Az adszorpció nem más, mint az a jelenség, amikor egy gáz vagy folyadék molekulái (az adszorbátum) egy szilárd vagy folyékony anyag (az adszorbens) felületéhez tapadnak. Bár az adszorpció fogalma egyszerűnek tűnhet, valójában két alapvetően különböző mechanizmust takar: a fiziszorpciót és a kemiszorpciót. E két jelenség megértése elengedhetetlen a felületi folyamatok mélyebb megismeréséhez, az anyagok tervezéséhez és az ipari eljárások optimalizálásához.
A felületi kölcsönhatások spektrumán belül a fiziszorpció és a kemiszorpció két végpontot képvisel, melyek között számos átmeneti állapot is létezhet. A különbségek alapvetően az interakciók erejében és jellegében gyökereznek, amelyek viszont meghatározzák a folyamatok termodinamikai és kinetikai tulajdonságait, valamint a gyakorlati alkalmazhatóságukat. Míg a fiziszorpció inkább fizikai jellegű, gyenge erők által vezérelt folyamat, addig a kemiszorpció egy kémiai reakcióhoz hasonló, erős kötésekkel járó jelenség. Ennek a két mechanizmusnak a részletes feltárása, jellemzőinek bemutatása, valamint a közöttük lévő éles és néha elmosódó határvonalak megértése kulcsfontosságú ahhoz, hogy hatékonyan alkalmazhassuk tudásunkat például katalizátorok fejlesztésében, gáztárolásban, szennyezőanyagok eltávolításában vagy éppen új nanoanyagok tervezésében.
A fiziszorpció, a felületi tapadás finom művészete
A fiziszorpció, vagy más néven fizikai adszorpció, egy olyan felületi jelenség, amely során az adszorbátum molekulái gyenge, nem kovalens vagy ionos kölcsönhatások révén kötődnek az adszorbens felületéhez. Ezen interakciók alapját elsősorban a Van der Waals erők képezik, amelyek magukban foglalják a diszperziós (London), dipólus-dipólus és indukciós erőket. Ezek az erők, bár egyenként gyengék, nagy számban és megfelelő geometriai elrendezésben jelentős adhéziót biztosíthatnak. A fiziszorpció univerzális jelenség, amely bármely gáz és szilárd felület között lejátszódhat, feltéve, hogy a hőmérséklet elegendően alacsony, és a nyomás elegendően magas.
A Van der Waals erők természete miatt a fiziszorpció nem igényel specifikus kémiai kölcsönhatást vagy elektronátmenetet az adszorbens és az adszorbátum között. Ez azt jelenti, hogy a folyamat nem szelektivitás-vezérelt, hanem inkább a felületi energiától, a molekulák polarizálhatóságától és a hőmérséklettől függ. Minél nagyobb a molekula polarizálhatósága, annál erősebbek lehetnek a diszperziós erők, és annál könnyebben adszorbeálódik. Ezenkívül a felület morfológiája és a pórusméret-eloszlás is döntő szerepet játszik, mivel a pórusokban fellépő fokozott kölcsönhatások (ún. pórusfeltöltődés) jelentősen növelhetik az adszorpciós kapacitást.
A fiziszorpció alapvető jellemzői és mechanizmusai
A fiziszorpciót számos jellegzetes tulajdonság különbözteti meg más felületi folyamatoktól. Az egyik legfontosabb jellemzője a reverzibilitás. Mivel a kötési energiák alacsonyak (jellemzően 20-40 kJ/mol alatt), az adszorbeált molekulák viszonylag könnyen deszorbeálódhatnak a felületről a hőmérséklet növelésével vagy a nyomás csökkentésével. Ez a reverzibilis természet teszi lehetővé a fiziszorpciós rendszerek regenerálását és újrahasznosítását, ami számos ipari alkalmazásban, például gázleválasztásban vagy szárításban kulcsfontosságú.
A fiziszorpciós folyamatok során nem egyetlen molekuláris réteg, hanem gyakran többrétegű adszorpció (multiréteg képződés) figyelhető meg. Amint a felület telítődik az első molekuláris réteggel, további molekulák tapadhatnak meg az előzőleg adszorbeált rétegen, rétegenként építve fel a molekulákból álló filmet. Ez a jelenség különösen alacsony hőmérsékleten és magas nyomáson válik hangsúlyossá, és a BET elmélet (Brunauer-Emmett-Teller elmélet) írja le a legjobban, amely az ipari felületmérés alapjává vált.
Az adszorpciós hő, vagyis az a hőmennyiség, ami egy mol adszorbátum felülethez kötődésekor felszabadul, a fiziszorpció esetében viszonylag alacsony. Ez az érték általában a kondenzációs hő nagyságrendjébe esik, ami megerősíti a gyenge fizikai kölcsönhatások elméletét. Az alacsony adszorpciós hő azt is jelenti, hogy a fiziszorpció nem igényel jelentős aktiválási energiát, így gyorsan és könnyedén lejátszódhat még alacsony hőmérsékleten is. Az adszorpciós sebesség általában diffúzió-kontrollált, ami azt jelenti, hogy a molekulák felülethez jutásának sebessége korlátozza a folyamatot.
A fiziszorpció az anyagok közötti finom tánc, ahol a Van der Waals erők láthatatlan szálakkal kötik össze a molekulákat a felületekkel, anélkül, hogy kémiai kötések születnének.
A hőmérséklet és nyomás hatása a fiziszorpcióra
A hőmérséklet és a nyomás rendkívül befolyásos tényezők a fiziszorpció dinamikájában. Az alacsony hőmérséklet kedvez a fiziszorpciónak, mivel az adszorbeált molekulák kinetikus energiája kisebb, így kevésbé hajlamosak deszorbeálódni. Ahogy a hőmérséklet emelkedik, a molekulák mozgása fokozódik, ami növeli a deszorpció valószínűségét, és csökkenti az adszorpciós kapacitást. Ezért a fiziszorpciót gyakran kriogén hőmérsékleten (pl. folyékony nitrogén hőmérsékletén) vizsgálják és alkalmazzák.
A nyomás szintén kulcsfontosságú paraméter. Magasabb nyomáson a gázfázisú molekulák koncentrációja megnő, ami növeli a felület és a molekulák közötti ütközések számát, és így az adszorpciós sebességet is. Ennek eredményeként magasabb nyomáson nagyobb mennyiségű adszorbátum kötődik a felülethez. Az adszorpciós izotermák, amelyek az adszorbeált mennyiség nyomásfüggését írják le állandó hőmérsékleten, jellemző görbéket mutatnak, amelyek a fiziszorpció esetében gyakran S-alakúak vagy lépcsőzetesek, különösen a multiréteg képződés miatt.
A kemiszorpció: kémiai kötések a felületen
A kemiszorpció, vagy kémiai adszorpció, egy olyan felületi jelenség, amely során az adszorbátum molekulái kémiai kötések (kovalens vagy ionos) révén kötődnek az adszorbens felületéhez. Ez a folyamat sokkal specifikusabb és erősebb, mint a fiziszorpció, és valójában egy heterogén kémiai reakcióként értelmezhető, ahol a felület a reagens egyik partnere. A kemiszorpció során az adszorbátum molekuláinak elektronállapota megváltozhat, és új kémiai fajok keletkezhetnek a felületen.
A kémiai kötések kialakulása azt jelenti, hogy a kemiszorpcióhoz az adszorbens felületén aktív centrumoknak kell lenniük, amelyek képesek kémiai kölcsönhatásba lépni az adszorbátum molekuláival. Ezek az aktív centrumok lehetnek hiányok, élek, sarokatomok vagy speciális kristályrács-síkú atomok, amelyek nem telített vegyértékkel rendelkeznek, vagy szabad elektronpárokat kínálnak. Ennek következtében a kemiszorpció sokkal szelektívebb, mint a fiziszorpció: csak bizonyos gázok adszorbeálódnak specifikus felületeken.
A kemiszorpció alapvető jellemzői és mechanizmusai
A kemiszorpció legfontosabb jellemzője az irreverzibilitás vagy csak nehezen reverzibilis jellege. Mivel a kötési energiák magasak (jellemzően 40-800 kJ/mol között, ami egy kémiai kötés energiájának felel meg), az adszorbeált molekulák eltávolítása a felületről jelentős energia befektetést igényel, gyakran magas hőmérséklet és/vagy vákuum alkalmazásával jár. Ez a deszorpció gyakran kémiai változással is járhat, például a molekula disszociációjával.
A kemiszorpció során általában monoréteg képződés figyelhető meg. Mivel a kémiai kötések specifikus aktív centrumokhoz kötődnek, amint ezek a centrumok telítődnek, további molekulák nem tudnak kémiai kötéssel kapcsolódni az első réteghez. Az első réteg felett esetlegesen kialakuló további rétegek már fiziszorpciós jellegűek lennének, de a kemiszorpció definíciója szigorúan az első, kémiailag kötött rétegre vonatkozik. Ez a monoréteg telítődése gyakran a Langmuir adszorpciós izotermával írható le.
Az adszorpciós hő a kemiszorpció esetében magas, gyakran meghaladja a 100 kJ/mol értéket, ami egyértelműen jelzi a kémiai kötések kialakulását. Ez az energia felszabadulás a folyamat exoterm jellegére utal. Fontos megjegyezni, hogy a kemiszorpció gyakran aktiválási energiát igényel. Ez azt jelenti, hogy a reakció megindulásához egy bizonyos energiaszintet át kell lépni, még akkor is, ha a teljes folyamat exoterm. Az aktiválási energia magyarázza, miért nem indulnak el azonnal bizonyos kemiszorpciós folyamatok szobahőmérsékleten, és miért van szükség fűtésre vagy katalizátorra.
A kemiszorpció nem csupán tapadás, hanem egy intim kémiai kapcsolat, ahol a felület és a molekula elektronjai új konfigurációba rendeződnek, átírva a felületi reakciók szabályait.
A szelektivitás és az aktiválási energia szerepe
A kemiszorpció szelektivitása az egyik legfontosabb jellemzője. A specifikus kémiai kölcsönhatások miatt az adszorbens felülete csak bizonyos molekulákat fog megkötni, míg másokat elutasít. Ez a tulajdonság teszi a kemiszorpciót különösen értékessé a heterogén katalízisben, ahol a katalizátor felülete szelektíven aktiválja a reaktánsokat, lehetővé téve a kívánt termék képződését, miközben gátolja a mellékreakciókat. A katalizátor felületén lejátszódó kemiszorpció a reakciósebesség növelésének és a termelékenység javításának kulcsa.
Az aktiválási energia (Ea) fogalma kulcsfontosságú a kemiszorpció kinetikájának megértésében. Ha a kemiszorpció aktiválási energiát igényel, azt aktivált kemiszorpciónak nevezzük. Ez azt jelenti, hogy a molekuláknak elegendő energiával kell rendelkezniük ahhoz, hogy legyőzzék az energiagátat, mielőtt kémiai kötést hoznának létre a felülettel. Ez az energia hő formájában, vagy a molekulák kinetikus energiájából származhat. Az aktiválási energia létezése magyarázza a kemiszorpciós reakciók hőmérsékletfüggését, és azt, hogy miért van szükség magasabb hőmérsékletre a folyamat elindításához vagy felgyorsításához. Az aktiválási energia nélküli kemiszorpciót nem-aktivált kemiszorpciónak hívjuk, ami ritkább, de előfordulhat rendkívül reaktív felületek és molekulák között.
A fiziszorpció és kemiszorpció összehasonlítása: kulcsfontosságú különbségek
A fiziszorpció és a kemiszorpció közötti különbségek alapvetőek, és számos aspektusban megnyilvánulnak. Ezeknek a különbségeknek az ismerete elengedhetetlen a felületi folyamatok helyes értelmezéséhez és az anyagok jellemzéséhez. A legfontosabb megkülönböztető jegyeket az alábbiakban részletezzük, majd egy táblázatban is összefoglaljuk.
A kölcsönhatás jellege és ereje
A legfundamentálisabb különbség a kötőerőkben rejlik. A fiziszorpciót gyenge Van der Waals erők (diszperziós, dipólus-dipólus, indukciós) dominálják, amelyek tisztán fizikai jellegűek és nem járnak elektronátmenettel. Ezek az erők viszonylag nagy távolságban is hatnak, és nem specifikusak. Ezzel szemben a kemiszorpció erős kémiai kötések (kovalens, ionos, fémes) kialakulásával jár, amelyek specifikusak, rövid hatótávolságúak és magukban foglalják az elektronok átrendeződését vagy átadását a felület és az adszorbátum között. Ez az alapvető különbség határozza meg a többi eltérést.
Adszorpciós hő és aktiválási energia
Az adszorpciós hő nagysága egyértelműen megkülönbözteti a két jelenséget. A fiziszorpció esetében ez az érték alacsony, jellemzően 20-40 kJ/mol alatti, ami a kondenzációs hőhöz hasonló. Ez azt jelenti, hogy a molekulák kötődése a felülethez nem sokkal erősebb, mint a molekulák egymáshoz való kötődése a folyékony fázisban. A kemiszorpció adszorpciós hője viszont magas, gyakran 40-800 kJ/mol tartományba esik, ami egy kémiai reakcióra jellemző energiafelszabadulás. Ez az energia felszabadulás a kémiai kötések kialakulásából származik.
Az aktiválási energia tekintetében is jelentős a különbség. A fiziszorpció általában nem igényel aktiválási energiát, vagy ha igen, az minimális, mivel a gyenge Van der Waals erők azonnal kialakulhatnak, amint a molekula elég közel kerül a felülethez. A kemiszorpció viszont gyakran igényel aktiválási energiát ahhoz, hogy a kémiai kötések kialakulhassanak. Ez az aktiválási gát a reaktánsok molekuláinak és a felület atomjainak elektronállapot-átrendeződéséhez szükséges energiát tükrözi.
Reverzibilitás és rétegszám
A reverzibilitás kulcsfontosságú. A fiziszorpció reverzibilis folyamat, ami azt jelenti, hogy az adszorbeált molekulák viszonylag könnyen deszorbeálódhatnak a hőmérséklet növelésével vagy a nyomás csökkentésével. A kemiszorpció viszont jellemzően irreverzibilis, vagy csak nagyon nehezen reverzibilis. A deszorpcióhoz magas hőmérséklet és/vagy vákuum szükséges, és gyakran kémiai változással jár.
A rétegszám tekintetében is eltérés mutatkozik. A fiziszorpció során gyakori a multiréteg képződés, különösen alacsony hőmérsékleten és magas nyomáson, ahol az adszorbeált molekulák további rétegeket képezhetnek az első rétegen. Ezzel szemben a kemiszorpció jellemzően monoréteg képződéssel jár, mivel a kémiai kötések specifikus felületi centrumokhoz kötődnek, és ezek telítődése után nincs lehetőség további kémiai kötés kialakítására ugyanazon a ponton.
Hőmérséklet- és nyomásfüggés, szelektivitás
A hőmérsékletfüggés ellentétes. A fiziszorpció alacsonyabb hőmérsékleten kedvezőbb, mivel a gyenge kötések könnyen felbomlanak magasabb hőmérsékleten. A kemiszorpcióra viszont gyakran magasabb hőmérséklet szükséges az aktiválási energia legyőzéséhez, bár extrém magas hőmérsékleten a deszorpció dominálhat.
A nyomásfüggés mindkét esetben pozitív, azaz a nyomás növelésével az adszorbeált mennyiség is nő, de az izotermák alakja eltérő. A fiziszorpciós izotermák gyakran S-alakúak vagy lépcsőzetesek, míg a kemiszorpciós izotermák jellemzően telítési platót mutatnak a monoréteg telítődése után (pl. Langmuir izoterma).
A szelektivitás a kemiszorpció egyik legfontosabb megkülönböztető jegye. Míg a fiziszorpció univerzális és bármely gáz-szilárd felület rendszerben felléphet, addig a kemiszorpció rendkívül szelektív, és csak akkor következik be, ha az adszorbátum és az adszorbens között megfelelő kémiai affinitás áll fenn, és aktív centrumok rendelkezésre állnak. Ez a szelektivitás teszi lehetővé a kemiszorpció alkalmazását katalízisben és szelektív gázérzékelésben.
| Jellemző | Fiziszorpció (Fizikai adszorpció) | Kemiszorpció (Kémiai adszorpció) |
|---|---|---|
| Kötőerők | Gyenge Van der Waals erők (diszperziós, dipólus-dipólus, indukciós) | Erős kémiai kötések (kovalens, ionos, fémes) |
| Adszorpciós hő | Alacsony (20-40 kJ/mol alatt), a kondenzációs hőhöz hasonló | Magas (40-800 kJ/mol), a kémiai kötések energiájának megfelelő |
| Aktiválási energia | Gyakran nincs, vagy nagyon alacsony | Gyakran magas, aktivált folyamat |
| Reverzibilitás | Reverzibilis, könnyen deszorbeálható | Irreverzibilis, vagy nehezen reverzibilis |
| Rétegszám | Multiréteg képződés lehetséges | Monoréteg képződés jellemző |
| Hőmérsékletfüggés | Alacsony hőmérsékleten kedvezőbb | Gyakran magasabb hőmérsékleten indul meg (aktiválási energia miatt) |
| Szelektivitás | Nem szelektív, univerzális | Rendkívül szelektív, specifikus kölcsönhatásokat igényel |
| Felületi változás | Az adszorbens felülete változatlan marad | Az adszorbens felülete megváltozhat, új felületi vegyületek képződhetnek |
| Adszorbátum állapota | Az adszorbátum molekuláris identitása megmarad | Az adszorbátum disszociálhat, átalakulhat a felületen |
| Példák | N2 adszorpció aktív szenes felületen alacsony hőmérsékleten, gázok tárolása zeolitokban | O2 adszorpció fémfelületen, H2 adszorpció platina felületen (katalízis) |
Átmeneti esetek és a spektrum
Fontos megjegyezni, hogy bár a fiziszorpció és a kemiszorpció két elkülönülő kategória, a valóságban gyakran előfordulnak átmeneti esetek. Néha a kölcsönhatások ereje a két tartomány határán helyezkedik el, vagy akár egyazon rendszerben mindkét típusú adszorpció is lejátszódhat egymás mellett. Például, egy erős kemiszorpciós réteg felett fiziszorbeált molekulák is megjelenhetnek. Ezen túlmenően, bizonyos esetekben a fiziszorpció előfutára lehet a kemiszorpciónak, ahol a molekula először gyengén kötődik a felülethez (prekurzor állapot), majd elegendő energia hatására aktiválódik és erősebben, kémiailag kötődik.
A felületi jelenségek spektruma tehát sokkal árnyaltabb, mint pusztán két bináris kategória. A kutatók folyamatosan vizsgálják ezeket az átmeneti állapotokat és a kölcsönhatások finomabb részleteit, hogy pontosabb modelleket alkossanak és jobban megértsék a komplex felületi reakciókat. Az in situ spektroszkópiai módszerek, mint például az infra vörös (IR) spektroszkópia vagy az X-sugaras fotoelektron-spektroszkópia (XPS), lehetővé teszik a felületi kötések jellegének azonosítását és a két mechanizmus elkülönítését.
Mérési módszerek és anyagjellemzés a fiziszorpció és kemiszorpció segítségével

A fiziszorpció és a kemiszorpció nem csupán elméleti koncepciók, hanem konkrét, mérhető jelenségek, amelyek segítségével számos fontos anyagtulajdonság meghatározható. A megfelelő mérési módszerek kiválasztása kulcsfontosságú a két adszorpciós típus elkülönítéséhez és a felületi jellemzők pontos leírásához.
Adszorpciós izotermák mérése
Az adszorpciós izotermák mérése az egyik legelterjedtebb módszer a felületek jellemzésére. Az izoterma az adszorbeált gáz mennyiségét mutatja a nyomás függvényében, állandó hőmérsékleten. A fiziszorpciós izotermák, különösen a nitrogén adszorpciója folyékony nitrogén hőmérsékletén (77 K), alapvető fontosságúak a specifikus felület, a pórusméret-eloszlás és a pórustérfogat meghatározásában. A BET elmélet (Brunauer-Emmett-Teller) a leggyakrabban használt modell a specifikus felület számítására a fiziszorpciós izotermák alapján. Ez a módszer széles körben alkalmazott a gyógyszeriparban, a katalizátorgyártásban és az anyagtudományban.
A kemiszorpciós izotermák mérése hasonló elven működik, de általában magasabb hőmérsékleten és specifikus reaktáns gázokkal történik (pl. hidrogén vagy szén-monoxid fémkatalizátorokon). A kemiszorpciós izotermák gyakran Langmuir típusúak, ami egy monoréteg telítődését írja le. Ezek az izotermák információt szolgáltatnak az aktív centrumok számáról és a diszperzióról (azaz a felületen lévő aktív fázis arányáról), ami kritikus a katalizátorok teljesítményének értékelésében.
Kalorimetriai módszerek
Az adszorpciós hő közvetlen mérése kalorimetriás módszerekkel szintén hatékony eszköz a fiziszorpció és kemiszorpció elkülönítésére. Mivel a fiziszorpció adszorpciós hője alacsony, a kemiszorpcióé pedig magas, a mért hőmennyiség egyértelműen utalhat a domináns mechanizmusra. A differenciális adszorpciós kalorimetria (DAC) vagy az izotermikus titrációs kalorimetria (ITC) segítségével pontosan meghatározható az adszorpciós hő, ami értékes termodinamikai információkat szolgáltat a felületi kölcsönhatásokról.
Spektroszkópiai technikák
A spektroszkópiai módszerek lehetővé teszik a felületen adszorbeált molekulák kémiai természetének és kötésének közvetlen vizsgálatát. Ezek a technikák különösen hasznosak a kemiszorpció tanulmányozásában, mivel érzékenyek a kémiai kötések kialakulására és az elektronállapotok változásaira.
- Infravörös (IR) és Raman spektroszkópia: Ezek a módszerek az adszorbeált molekulák vibrációs spektrumát vizsgálják. A kémiai kötés kialakulása az adszorbátum molekuláiban lévő kötések rezgési frekvenciáinak eltolódását vagy új rezgési módusok megjelenését okozza. Például, a CO kemiszorpciója fémfelületen jellegzetes IR abszorpciós sávokat mutat, amelyek a fém-szén kötés kialakulására utalnak.
- X-sugaras fotoelektron-spektroszkópia (XPS): Az XPS a felületi atomok elektronszerkezetét vizsgálja. A kémiszorpció során bekövetkező elektronátmenetek és töltésátrendeződések kimutathatók az XPS spektrumokban, mint az elemek kötésszint energiáinak eltolódása (ún. kémiai eltolódás). Ez a módszer információt szolgáltat a felületi fajok oxidációs állapotáról és a kémiai környezetükről.
- Auger-elektron spektroszkópia (AES) és Alacsony Energiájú Elektron Diffrakció (LEED): Ezek a módszerek a felület elemi összetételét és kristályszerkezetét vizsgálják. Bár közvetlenül nem mutatják ki a kötéstípusokat, segítenek azonosítani az aktív centrumokat és a felületi rendszerek szerkezetét, amelyek befolyásolják a kemiszorpciót.
Felületi mikroszkópiai technikák
A modern felületi mikroszkópiai technikák, mint a pásztázó alagútmikroszkópia (STM) és az atomi erőmikroszkópia (AFM), atomi felbontásban képesek vizsgálni az adszorbeált molekulákat a felületen. Ezekkel a módszerekkel közvetlenül megfigyelhető az adszorbátum elrendeződése, a monoréteg képződése, sőt, bizonyos esetekben az egyes molekulák kölcsönhatásai is. Bár ezek a technikák inkább a molekuláris elrendezésre fókuszálnak, a molekulák viselkedésének megfigyelése atomi szinten segíthet megkülönböztetni a gyenge fizikai és az erős kémiai kötéseket.
A fiziszorpció és kemiszorpció jelentősége a gyakorlatban
A fiziszorpció és a kemiszorpció nem csupán elméleti érdekességek, hanem rendkívül fontosak a modern technológiák és a mindennapi élet számos területén. Az alapvető mechanizmusok megértése lehetővé teszi, hogy célzottan fejlesszünk új anyagokat és optimalizáljuk a meglévő eljárásokat.
Ipari alkalmazások
Az iparban mindkét adszorpciós típus széles körben alkalmazott.
- Katalízis: A heterogén katalízis a kemiszorpció legfontosabb alkalmazási területe. A katalizátorok felületén a reaktánsok kemiszorbeálódnak, ami aktiválja őket, csökkenti a reakció aktiválási energiáját és felgyorsítja a kémiai átalakulást. Például az ammónia szintézise (Haber-Bosch folyamat), a kőolajfinomítás vagy az autóipari katalizátorok mind kemiszorpciós folyamatokon alapulnak. A katalizátorok tervezésénél kulcsfontosságú az aktív centrumok számának és a kemiszorpciós erősség optimalizálása.
- Gázleválasztás és tisztítás: A fiziszorpciót széles körben használják gázok szétválasztására és tisztítására. Például a levegőből történő oxigén- és nitrogén-előállítás (PSA – Pressure Swing Adsorption), a földgáz tisztítása (pl. CO2 eltávolítása) vagy a szén-dioxid leválasztása (Carbon Capture) mind fiziszorpciós elveken alapul. Az adszorbensek, mint a zeolitok, aktív szenes anyagok vagy fém-organikus vázak (MOF-ok) pórusméretét és felületi tulajdonságait úgy optimalizálják, hogy szelektíven adszorbeáljanak bizonyos gázokat.
- Szárítás: A levegő vagy egyéb gázok nedvességtartalmának eltávolítása gyakran fiziszorpcióval történik, ahol a vízgőz molekulái szilikagél, alumínium-oxid vagy zeolit felületén adszorbeálódnak.
- Gáztárolás: A fiziszorpció ígéretes technológia gázok, például hidrogén vagy metán biztonságos és hatékony tárolására. Porózus anyagok, mint a MOF-ok vagy a COF-ok (kovalens organikus vázak) nagy felülete és szabályozott pórusmérete lehetővé teszi nagy mennyiségű gáz tárolását viszonylag alacsony nyomáson, fiziszorpcióval.
Környezetvédelem
A környezetvédelem területén mindkét adszorpciós mechanizmus alapvető szerepet játszik.
- Szennyezőanyagok eltávolítása: Az aktív szenes szűrők, amelyek a fiziszorpció elvén működnek, széles körben alkalmazottak a víz és levegő tisztításában. Eltávolítják a szerves szennyezőanyagokat, illékony szerves vegyületeket (VOC-k) és szagokat. A kemiszorpcióval specifikus szennyezőanyagok, például nehézfémionok vagy kénvegyületek is eltávolíthatók a vízből és a levegőből, szelektív adszorbensek segítségével.
- Katalitikus konverterek: Az autók kipufogógázainak tisztításában a kemiszorpciós folyamatokon alapuló katalitikus konverterek alakítják át a káros gázokat (CO, NOx, szénhidrogének) ártalmatlan anyagokká (CO2, N2, H2O).
A felületi jelenségek megértése hidat képez az atomi szintű interakciók és a milliárd dolláros iparágak között, alapjaiban formálva, hogyan élünk és termelünk.
Anyagtudomány és nanotechnológia
Az anyagtudományban az adszorpciós jelenségek kulcsfontosságúak az anyagok jellemzésében és új anyagok fejlesztésében.
- Anyagok jellemzése: Ahogy korábban említettük, a fiziszorpciós izotermák (különösen a BET módszer) a specifikus felület és a pórusméret-eloszlás standard mérési módszerei, amelyek kritikusak a porózus anyagok, nanoméretű részecskék és bevonatok minőségellenőrzéséhez.
- Nanométeres anyagok tervezése: A nanotechnológia területén a felületi tulajdonságok finomhangolása elengedhetetlen. A felületi funkcionalizálás, amely gyakran kemiszorpciós folyamatokon keresztül valósul meg, lehetővé teszi a nanoanyagok tulajdonságainak (pl. biokompatibilitás, katalitikus aktivitás) szabályozását.
- Gázérzékelők: A felületi adszorpció, különösen a kemiszorpció, az alapja számos gázérzékelő működésének. Amikor a célgáz kemiszorbeálódik az érzékelő felületén, az megváltoztatja az anyag elektromos vezetőképességét vagy optikai tulajdonságait, ami mérhető jelet generál.
Orvostudomány és gyógyszeripar
Az orvostudomány és a gyógyszeripar is profitál az adszorpciós jelenségek megértéséből.
- Gyógyszerhordozók: A porózus anyagok, mint a szilikagél vagy a mezopórusos szilikátok, fiziszorpcióval képesek nagy mennyiségű gyógyszerhatóanyagot adszorbeálni, majd szabályozottan felszabadítani a szervezetben.
- Bioszenzorok: A felületi adszorpció, mind fizikai, mind kémiai, alapvető fontosságú a bioszenzorok működésében. A biológiai molekulák (pl. fehérjék, DNS) szelektív adszorpciója a szenzor felületén specifikus detekciót tesz lehetővé.
- Implantátumok felületi módosítása: Az implantátumok felületének módosítása kemiszorpciós rétegekkel javíthatja a biokompatibilitást és elősegítheti a sejtek adhézióját.
Jövőbeli perspektívák és kutatási irányok
A fiziszorpció és a kemiszorpció területe folyamatosan fejlődik, új anyagok és elméleti megközelítések jelennek meg, amelyek tovább bővítik a jelenségek megértését és alkalmazási lehetőségeit. A kutatás számos izgalmas irányba mutat.
Új adszorbens anyagok fejlesztése
A fém-organikus vázak (MOF-ok) és a kovalens organikus vázak (COF-ok) megjelenése forradalmasította a porózus anyagok kutatását. Ezek az anyagok rendkívül nagy specifikus felülettel és szabályozható pórusmérettel rendelkeznek, ami ideálissá teszi őket gáztárolásra, gázleválasztásra és katalízisre. A MOF-ok és COF-ok esetében a fiziszorpció dominál a gáztárolásban, de a keretet alkotó fémközpontok és ligandumok módosításával specifikus kemiszorpciós centrumok is beépíthetők, amelyek fokozhatják a szelektivitást és az aktivitást.
A kétdimenziós anyagok, mint a grafén, a MXene-ek vagy a fém-dikalkogenidek (TMD-k), szintén ígéretes adszorbensek, rendkívül nagy felületük és egyedi elektronikus tulajdonságaik miatt. Ezeken az anyagokon mind fiziszorpciós, mind kemiszorpciós folyamatok vizsgálhatók, különösen gázérzékelésben és energiatárolásban.
Számítógépes modellezés és szimuláció
A számítógépes modellezés, mint a sűrűségfunkcionál-elmélet (DFT) alapú számítások vagy a molekuladinamikai szimulációk, egyre fontosabb szerepet játszik a fiziszorpciós és kemiszorpciós folyamatok megértésében. Ezek a módszerek lehetővé teszik a felületi kölcsönhatások atomi szintű vizsgálatát, az adszorpciós energiák, az aktiválási energiák és a molekuláris elrendezések előrejelzését. A számítási kémia segítségével virtuálisan tesztelhetők új adszorbens anyagok, és optimalizálhatók a meglévő rendszerek, csökkentve a kísérleti munka igényét.
Fenntartható technológiák és környezeti kihívások
A jövőben a fiziszorpció és a kemiszorpció kulcsfontosságú lesz a fenntartható technológiák fejlesztésében. A szén-dioxid leválasztása és hasznosítása, a hidrogéngazdaság megvalósítása, a megújuló energiaforrásokhoz kapcsolódó energiatárolás, valamint a környezetszennyezés hatékonyabb leküzdése mind olyan területek, ahol az adszorpciós folyamatok optimalizálása elengedhetetlen. A kutatás a környezetbarát, költséghatékony és nagy teljesítményű adszorbensek és katalizátorok fejlesztésére fókuszál, amelyek hozzájárulnak egy tisztább és fenntarthatóbb jövő megteremtéséhez.
A fiziszorpció és a kemiszorpció közötti különbségek mélyreható megértése nemcsak a tudományos alapokat erősíti, hanem gyakorlati eszközöket is biztosít a mérnökök és kutatók számára, hogy innovatív megoldásokat fejlesszenek ki a modern társadalom kihívásaira. Ahogy az anyagtudomány és a felületi kémia fejlődik, úgy nyílnak meg újabb és újabb lehetőségek ezen alapvető felületi jelenségek kiaknázására, a molekuláris szintű manipulációtól az ipari léptékű alkalmazásokig.