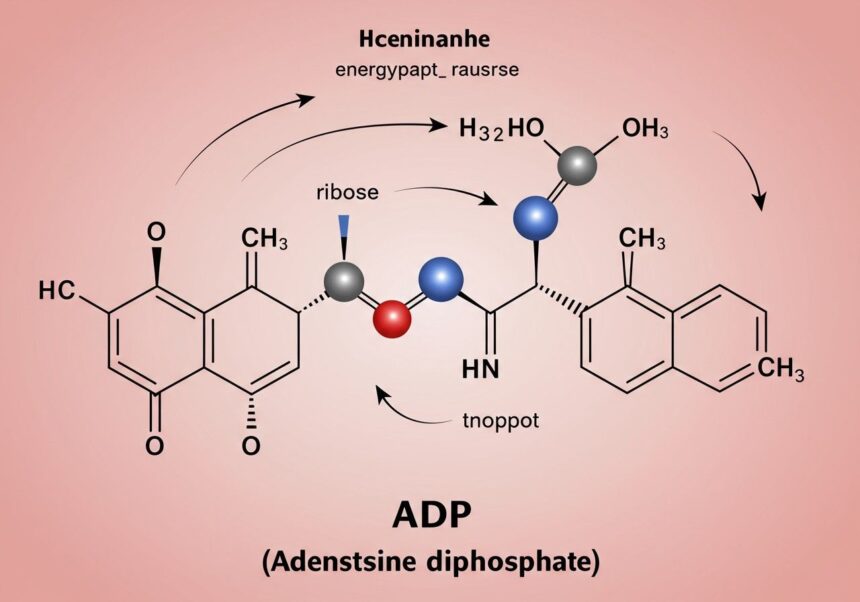
Az adenozin-difoszfát, röviden ADP, a sejtbiológia és a biokémia egyik alapvető molekulája, melynek központi szerepe van az élőlények energiacseréjében. Bár gyakran az ATP (adenozin-trifoszfát) árnyékában emlegetik, az ADP nem csupán egy „lemerült” ATP-molekula; önálló, kritikus funkciókkal rendelkezik, amelyek nélkülözhetetlenek az életfolyamatok fenntartásához. Az ADP a sejt energiaállapotának kulcsfontosságú indikátora, és aktívan részt vesz az energiaátvitel, a jelátvitel, sőt még a véralvadás szabályozásában is. Ennek a molekulának a megértése elengedhetetlen a sejtek működésének, az anyagcsere-folyamatoknak és számos betegség patomechanizmusának mélyebb megismeréséhez.
A molekula elnevezése is utal szerkezetére: az „adenozin” egy purin bázisból (adenin) és egy öt szénatomos cukorból (ribóz) álló nukleozid, míg a „difoszfát” két foszfátcsoport jelenlétére utal. Ezek a foszfátcsoportok speciális, magas energiájú kötésekkel kapcsolódnak egymáshoz, amelyek felbomlása jelentős energiát szabadít fel. Ez az energia az, amit a sejtek a különböző biológiai folyamatok meghajtására használnak fel, legyen szó izomösszehúzódásról, aktív transzportról, szintézisről vagy idegimpulzusok továbbításáról. Az ADP tehát nem passzív melléktermék, hanem egy dinamikus résztvevője a sejtek energiafelhasználási és -termelési ciklusainak, egyfajta „energiahordozó akkumulátor”, amely készen áll az újra feltöltésre.
Az ADP szerkezeti felépítése és kémiai jellemzői
Az adenozin-difoszfát (ADP) molekuláris felépítése alapvetően három fő komponensre bontható, amelyek együttesen alkotják a vegyületet és meghatározzák annak biológiai funkcióit. Ezek a komponensek az adenin bázis, a ribóz cukor és a két foszfátcsoport. Mindegyik elemnek specifikus szerepe van a molekula stabilitásában, reaktivitásában és interakcióiban más biológiai molekulákkal.
Az adenin, a nitrogéntartalmú bázis
Az adenin egy purin típusú nitrogéntartalmú heterociklusos bázis, amely a DNS és RNS felépítésében is részt vesz. Kémiai képlete C₅H₅N₅. Az adenin két gyűrűből áll: egy hatos gyűrűből (pirimidin) és egy ötös gyűrűből (imidazol), amelyek közösen alkotják a purin vázat. Ez a szerkezet lehetővé teszi az adenin számára, hogy hidrogénkötéseket képezzen más molekulákkal, ami alapvető a nukleinsavak kettős spiráljának stabilitásában, és fontos szerepet játszik az enzimekkel való kölcsönhatásokban is. Az ADP esetében az adenin az a rész, amely a molekula specifikusságát adja, és lehetővé teszi, hogy bizonyos enzimek felismerjék és megkössék.
A ribóz, az öt szénatomos cukor
A ribóz egy pentóz, azaz öt szénatomos monoszacharid, amely az adeninhez N-glikozidos kötéssel kapcsolódik. Pontosabban, az adenin 9-es nitrogénatomja a ribóz 1′-es szénatomjához kötődik. Ez a kombináció – az adenin és a ribóz – alkotja az adenozin nevű nukleozidot. A ribóz hidroxilcsoportjai (különösen a 2′-es és 3′-es szénatomon lévők) fontosak lehetnek az ADP molekula oldhatóságában és az enzimekkel való kölcsönhatásaiban. A ribóz jelenléte különbözteti meg az adenozin-származékokat a dezoxiribonukleotidoktól, ahol a 2′-es szénatomon hidrogénatom található hidroxilcsoport helyett.
A foszfátcsoportok és a magas energiájú kötések
Az adenozin molekulához két foszfátcsoport kapcsolódik észterkötésekkel. Az első foszfátcsoport a ribóz 5′-es szénatomjához kötődik, létrehozva az adenozin-monofoszfátot (AMP). Az ADP-ben egy második foszfátcsoport is kapcsolódik az elsőhöz egy speciális, úgynevezett anhidrid kötéssel. Ez a foszfoanhidrid kötés az, amit „magas energiájú kötésnek” nevezünk a biokémiában. Ez a kifejezés azt jelenti, hogy a kötés hidrolízise során viszonylag nagy mennyiségű szabad energia szabadul fel, amit a sejt felhasználhat. A második foszfátcsoport leválasztása az ADP-ről (AMP + Pi) is energiafelszabadulással jár, de általában az ATP -> ADP + Pi reakció a legfontosabb energiaforrás. Az ADP esetében a két foszfátcsoport közötti kötés a kulcs a molekula energiatároló képességében.
A foszfátcsoportok negatív töltésűek, ami befolyásolja a molekula oldhatóságát és interakcióit. A magas energiájú kötések nem azért „magas energiájúak”, mert sok energia szükséges a kialakításukhoz, hanem azért, mert a hidrolízis termékei (ADP és Pi, vagy AMP és Pi) sokkal stabilabbak, mint az eredeti ADP vagy ATP molekula. Ezt a stabilitáskülönbséget a rezonancia stabilizáció, az elektrosztatikus taszítás csökkenése és a hidráció különbségei magyarázzák. Ez a kémiai tulajdonság teszi az ADP-t és az ATP-t ideális molekulává az energiaátvitelhez.
„Az ADP szerkezete egy mesteri alkotás, melyben az adenin specifikussága, a ribóz rugalmassága és a foszfátcsoportok magas energiájú kötései tökéletes összhangban szolgálják a sejt energiaigényeit.”
Összefoglalva, az ADP egy nukleotid, amely adeninből, ribózból és két foszfátcsoportból áll. Kémiai felépítése teszi lehetővé, hogy a sejtek energiatároló és -átvivő molekulaként használják. Az adenin és ribóz alkotja az adenozin nukleozidot, míg a két foszfátcsoport kapcsolódása, különösen a második foszfát anhidrid kötése, a molekula biológiai funkciójának alapja.
Az ADP és az ATP ciklus: A sejt energiaellátásának alapja
A sejtek folyamatosan energiát igényelnek a túléléshez és működéshez. Ezt az energiát elsősorban az ATP (adenozin-trifoszfát) biztosítja, amely a sejtek univerzális energiavalutája. Az ATP azonban nem egy végtelen forrás; folyamatosan termelődnie és felhasználódnia kell egy dinamikus ciklusban, amelynek központi szereplője az ADP. Az ADP-ATP ciklus az élet alapja, egy állandó körforgás, amelyben az energia felszabadul és újratöltődik.
ATP hidrolízis ADP-re és Pi-re: Energiafelszabadulás
Amikor egy sejtnek energiára van szüksége valamilyen folyamat végrehajtásához (pl. izomösszehúzódás, aktív transzport, makromolekulák szintézise), az ATP molekula hidrolízisen megy keresztül. Ez azt jelenti, hogy egy vízmolekula segítségével az ATP terminális foszfátcsoportja leválik, és ADP (adenozin-difoszfát) és egy szabad anorganikus foszfát (Pi, vagy ortofoszfát) keletkezik. Ez a reakció, az ATP → ADP + Pi + energia, rendkívül egzoterm, azaz jelentős mennyiségű szabad energiát (körülbelül -30.5 kJ/mol standard körülmények között) szabadít fel. Ez a felszabaduló energia az, amit a sejt a munkájának elvégzésére fordít. Az ATP hidrolízise gyakran közvetlenül kapcsolódik a végrehajtandó folyamathoz, például egy fehérje konformációjának megváltoztatásához vagy egy szubsztrát foszforilálásához.
A reakció reverzibilis, de a sejtben a hidrolízis dominál az energiaigényes folyamatok során. Az ATP magas energiájú foszfoanhidrid kötéseinek felhasadása kulcsfontosságú a sejtek energiaellátásában. Az ADP képződése jelzi a sejt energiafelhasználását, és egyben szignálként is szolgál az ATP termelésének fokozására.
ADP visszaalakítása ATP-vé: Energiafelhasználás és szintézis
Az ADP önmagában nem képes sokáig tárolni az energiát; célja, hogy minél hamarabb visszaalakuljon ATP-vé. Ez a folyamat, az ADP + Pi + energia → ATP, valójában az a lépés, ahol a sejt az élelemből vagy a fényből származó energiát „feltölti” az ATP molekulákba. Ezt a foszforilációnak nevezett folyamatot a sejtek különböző módon hajtják végre, attól függően, hogy milyen típusú élőlényről van szó, és milyen metabolikus útról van szó. A három fő mechanizmus a következő:
Oxidatív foszforiláció
Ez a legjelentősebb ATP-termelő folyamat az aerob szervezetekben, és a mitokondriumokban zajlik. Az oxidatív foszforiláció során az energia a táplálékmolekulák oxidációjából származó elektronok transzportjából ered. Az elektrontranszport lánc (ETL) elektronok áramlását biztosítja, amelynek során protonok pumpálódnak ki a mitokondriális mátrixból az intermembrán térbe, létrehozva egy elektrokémiai potenciálgrádienst. Ezt a proton-grádienst használja fel az ATP szintáz enzimkomplex, amely egyfajta molekuláris turbinaként működik, és az ADP-t és anorganikus foszfátot ATP-vé szintetizálja. Ez a folyamat rendkívül hatékony, és a sejt ATP-termelésének nagy részéért felelős.
Szubsztrát szintű foszforiláció
A szubsztrát szintű foszforiláció egy közvetlenebb ATP-termelési mechanizmus, amely nem igényel oxigént vagy elektrontranszport láncot. Ebben a folyamatban egy magas energiájú foszfátcsoportot tartalmazó szubsztrátmolekula közvetlenül adja át foszfátcsoportját az ADP-nek, ATP-t képezve. Ez a mechanizmus a citoplazmában, a glikolízis során (pl. foszfoglicerát kináz és piruvát kináz reakciókban) és a mitokondriális mátrixban, a citromsavciklus során (GTP/ATP szintézis) is megfigyelhető. Bár kevesebb ATP-t termel, mint az oxidatív foszforiláció, gyors energiaforrást biztosít és anaerob körülmények között is működőképes.
Fotofoszforiláció
A fotoszintetikus szervezetekben (növények, algák, cianobaktériumok) a fény energiáját használják fel az ATP előállítására egy folyamatban, amelyet fotofoszforilációnak neveznek. Ez a folyamat a kloroplasztiszokban (eukariótákban) vagy a membránrendszerekben (prokariótákban) zajlik. A fényenergia gerjeszti az elektronokat, amelyek egy elektrontranszport láncon haladnak keresztül, hasonlóan az oxidatív foszforilációhoz. Az elektronok áramlása proton-grádienst hoz létre, amelyet az ATP szintáz használ fel az ADP és Pi ATP-vé való átalakítására. Ez a folyamat alapvető a Földön zajló élethez, mivel ez biztosítja az energiát a szerves anyagok szintéziséhez.
„Az ADP-ATP ciklus egy elegáns biológiai gépezet, melyben az energia nem vész el, csupán átalakul, biztosítva a sejtek állandó működését és az élet folytonosságát.”
Az ADP-ATP ciklus tehát egy folyamatos tánc az energiafelszabadítás és az energiafeltöltés között. Az ADP a sejt energiaállapotának kulcsfontosságú szenzora, és koncentrációja szorosan szabályozza az ATP termelésének sebességét. Amikor az ADP szintje magas, az azt jelzi, hogy a sejtnek több energiára van szüksége, és stimulálja az ATP-t termelő metabolikus utakat. Ez a kifinomult szabályozási mechanizmus biztosítja, hogy a sejt mindig elegendő energiával rendelkezzen, de ne pazarolja el feleslegesen.
Az ADP szerepe a sejten belüli energiaátvitelben és szabályozásban
Az ADP nem csupán egy köztes termék az ATP-ATP ciklusban, hanem aktív és dinamikus szereplője a sejten belüli energiaátvitelnek és számos metabolikus út szabályozásának. Koncentrációja a sejtben közvetlenül tükrözi annak energiaszükségletét és energiaállapotát, ami lehetővé teszi, hogy allosztérikus szabályozóként működjön, befolyásolva számos kulcsenzim aktivitását.
Katalizátor a különböző anyagcsereutakban
Az ADP, mint a foszfátcsoportok akceptora, esszenciális katalizátor számos biokémiai reakcióban, ahol ATP-szintézis történik. A sejtben zajló több ezer enzimreakció közül sok függ az ADP-től, mint szubsztráttól. Például az ATP szintáz, a glikolízisben részt vevő kinázok (pl. piruvát kináz, foszfoglicerát kináz) és a citromsavciklusban működő szukcinil-CoA szintetáz mind az ADP-t használják fel ATP előállítására. Ezek az enzimek speciálisan az ADP-hez kötődnek, és a foszfátcsoportok átadásával katalizálják az ATP képződését. Az ADP jelenléte tehát elengedhetetlen a sejt energiaellátását biztosító fő anyagcsere-utak működéséhez.
Regulátor szerepe: Allosztérikus szabályozás
Az ADP koncentrációja kulcsfontosságú allosztérikus szabályozó számos enzim számára. Az allosztérikus szabályozás azt jelenti, hogy egy molekula (az allosztérikus effektor) egy enzim aktív centrumától eltérő helyhez kötődik, és ezzel megváltoztatja az enzim konformációját és aktivitását. Az ADP, mint az alacsony energiaszint jelzője, gyakran pozitív allosztérikus szabályozója az ATP-t termelő enzimeknek, és negatív allosztérikus szabályozója az ATP-t fogyasztó enzimeknek. Ez a mechanizmus biztosítja, hogy a sejt metabolikus aktivitása az aktuális energiaigényekhez igazodjon.
Példák az allosztérikus szabályozásra:
- Foszfofruktokináz-1 (PFK-1): A glikolízis egyik kulcsfontosságú szabályozó enzime. Az ADP (és AMP) pozitív allosztérikus aktivátorként működik a PFK-1-en. Magas ADP/AMP szint azt jelzi, hogy a sejtnek több ATP-re van szüksége, ezért az ADP serkenti a glikolízist, hogy fokozza az ATP termelést.
- Piruvát kináz: A glikolízis utolsó lépésében részt vevő enzim. Az ADP szubsztrátja, de egyben aktivátora is lehet bizonyos izoenzimeknek, növelve az enzim affinitását a foszfoenolpiruvát (PEP) iránt.
- Izocitrát dehidrogenáz: A citromsavciklus egy szabályozó enzime. Az ADP pozitív allosztérikus aktivátorként hat rá, stimulálva a ciklust, hogy több NADH-t és FADH₂-t termeljen, amelyek az oxidatív foszforilációhoz szükségesek.
- ATP szintáz: Bár az ADP szubsztrátja, az ATP szintáz aktivitását is befolyásolja az ADP koncentrációja. Magas ADP szint növeli az ATP szintézis sebességét, amíg van elegendő proton-gradiens.
Enzimaktivitás befolyásolása: Az energiaállapot szenzora
Az ADP, az AMP és az ATP aránya a sejtben az úgynevezett energiaállapotot vagy energiaszintet (energy charge) jelzi. Ezt az arányt a következő képlettel lehet kifejezni: [ATP] + 0.5 [ADP] / ([ATP] + [ADP] + [AMP]). Egy magas energiaszint azt jelenti, hogy a sejtnek sok ATP-je van, és kevés ADP-je és AMP-je, míg egy alacsony energiaszint az ellenkezőjét jelzi. A sejtek az energiaszintet szigorúan szabályozzák, és az ADP kulcsfontosságú szerepet játszik ebben.
Az ADP koncentrációjának változása gyors választ vált ki a sejtekben. Ha az ATP felhasználás meghaladja a termelést, az ADP szint emelkedik. Ez az emelkedés azonnal aktiválja az ATP-t termelő utakat (pl. glikolízis, citromsavciklus, oxidatív foszforiláció) és gátolja az ATP-t fogyasztó utakat (pl. anabolikus folyamatok, szintézisek). Ez a visszacsatolási mechanizmus biztosítja, hogy a sejt energiaellátása mindig optimális legyen, és hatékonyan reagáljon a változó körülményekre, például fokozott fizikai aktivitásra vagy táplálékhiányra.
Egy másik fontos enzim, az adenilát kináz (vagy miokináz), folyamatosan fenntartja az egyensúlyt az ATP, ADP és AMP között: 2 ADP ⇌ ATP + AMP. Ez az enzim gyorsan reagál az ATP szint csökkenésére, két ADP molekulából egy ATP-t és egy AMP-t képezve. Az AMP szint emelkedése rendkívül érzékeny jelzője az energiahiánynak, és számos más metabolikus útvonalat is szabályoz, például az AMP-aktivált protein kinázt (AMPK), amely egy „főkapcsoló” a sejt metabolizmusában.
Az ADP tehát nem csupán egy passzív szubsztrát, hanem egy aktív molekuláris jelző és szabályozó, amely finomhangolja a sejt anyagcseréjét az aktuális energiaigényekhez. Ez a komplex szabályozási hálózat teszi lehetővé a sejtek számára, hogy hatékonyan működjenek és alkalmazkodjanak a változó környezeti feltételekhez.
Az ADP és a glikolízis: Az anaerob energiaátalakítás kulcsa
A glikolízis az egyik legősibb és leguniverzálisabb metabolikus út a Földön, amely a glükóz lebontásával energiát termel. Ez a folyamat a citoplazmában zajlik, és oxigén jelenlététől függetlenül képes ATP-t előállítani, bár nettó ATP hozama viszonylag alacsony. Az ADP kulcsfontosságú szerepet játszik ebben az útvonalban, mind szubsztrátként, mind allosztérikus szabályozóként.
ATP termelés és ADP felhasználás a glikolízisben
A glikolízis tíz lépésből álló folyamat, amely során egy molekula glükózból két molekula piruvát keletkezik. Bár a folyamat kezdeti lépései ATP-t igényelnek (glükóz foszforilációja és fruktóz-6-foszfát foszforilációja), a későbbi lépésekben ATP termelődik szubsztrát szintű foszforiláció révén. Két ilyen kulcsfontosságú lépés van, ahol az ADP közvetlenül felhasználásra kerül:
- 1,3-biszfoszfoglicerát → 3-foszfoglicerát: Ezt a reakciót a foszfoglicerát kináz enzim katalizálja. Az 1,3-biszfoszfoglicerátból származó magas energiájú foszfátcsoport átkerül az ADP-re, ATP-t képezve. Mivel egy glükóz molekulából két 1,3-biszfoszfoglicerát molekula keletkezik, ebben a lépésben két ATP termelődik.
- Foszfoenolpiruvát (PEP) → Piruvát: Ezt a reakciót a piruvát kináz enzim katalizálja. A PEP rendkívül magas energiájú foszfátcsoportját az ADP veszi fel, szintén ATP-t eredményezve. Szintén két ATP molekula termelődik ebben a lépésben glükóz molekulánként.
Nettó eredményként a glikolízis során két ATP molekula termelődik glükóz molekulánként, ami anaerob körülmények között a sejt fő energiaforrását jelenti. Az ADP tehát elengedhetetlen szubsztrátja ezeknek a kináz enzimeknek, amelyek az energiát átadják a glikolízis folyamatából az ATP-be.
Kulcsenzimek szabályozása: A glikolízis finomhangolása
Az ADP és az AMP nem csak szubsztrátként, hanem fontos szabályozó molekulaként is működnek a glikolízisben. Az energiaállapot változása közvetlenül befolyásolja a glikolízis sebességét, biztosítva, hogy a sejt csak akkor termeljen ATP-t ezen az úton, amikor arra valóban szüksége van.
- Foszfofruktokináz-1 (PFK-1): Ahogy már említettük, ez az enzim a glikolízis sebességét korlátozó (rate-limiting) lépését katalizálja, a fruktóz-6-foszfát foszforilációját fruktóz-1,6-biszfoszfáttá. A PFK-1 egy allosztérikus enzim, amelyet az ADP és különösen az AMP pozitívan szabályoz. Amikor az ADP/AMP szint magas (azaz az ATP szint alacsony), az ADP és AMP kötődnek a PFK-1 allosztérikus helyeihez, növelve az enzim aktivitását és felgyorsítva a glikolízist. Ez biztosítja, hogy a sejt fokozza az ATP termelést, amikor energiahiány van.
- Piruvát kináz: Ez az enzim is allosztérikusan szabályozott. Az ADP szubsztrátja, de egyben aktivátora is lehet bizonyos izoformáknak, fokozva a glikolízis utolsó lépését. Az ATP viszont gátolja a piruvát kinázt, ami egy negatív visszacsatolás, biztosítva, hogy ne termelődjön feleslegesen ATP, ha már elegendő van.
A glikolízis tehát egy kifinomultan szabályozott folyamat, ahol az ADP, mint a sejt energiaállapotának jelzője, központi szerepet játszik. A magas ADP/AMP arány aktiválja a glikolízist, míg a magas ATP szint gátolja azt. Ez a mechanizmus teszi lehetővé a sejtek számára, hogy gyorsan reagáljanak az energiaigények változására, és fenntartsák a metabolikus homeosztázist. Különösen fontos ez olyan szövetekben, mint az izom, ahol az energiaigény drámaian változhat rövid idő alatt, vagy olyan sejtekben, mint a vörösvértestek, amelyek kizárólag glikolízissel termelnek ATP-t.
Az ADP tehát elengedhetetlen a glikolízis hatékony működéséhez, nem csak mint szubsztrát, hanem mint egy kulcsfontosságú szabályozó, amely biztosítja, hogy a sejt energiatermelése szinkronban legyen az energiafelhasználásával.
Az ADP és a citromsavciklus (Krebs-ciklus): A mitokondriális energia-előfutár
A citromsavciklus, más néven Krebs-ciklus vagy trikarbonsav-ciklus, az aerob anyagcsere központi útvonala, amely a mitokondriális mátrixban zajlik. Bár ez a ciklus közvetlenül nem termel nagy mennyiségű ATP-t, kulcsfontosságú szerepet játszik az ADP-ATP ciklusban, mivel nagy mennyiségű redukált koenzimet (NADH és FADH₂) állít elő, amelyek az oxidatív foszforilációhoz szükségesek. Az ADP itt is, mint sok más metabolikus útvonalban, kulcsszerepet játszik a szabályozásban.
NADH és FADH₂ termelés, mint az oxidatív foszforiláció „üzemanyaga”
A citromsavciklus fő feladata az acetil-CoA (amely a szénhidrátok, zsírok és fehérjék lebontásából származik) teljes oxidációja szén-dioxiddá. Ennek során az elektronok egy sor redoxi reakción keresztül kerülnek át NAD⁺-ra és FAD-ra, redukált formájukat, a NADH-t és FADH₂-t képezve. Ezek a redukált koenzimek hordozzák azokat a magas energiájú elektronokat, amelyek az elektrontranszport láncba kerülnek, és ott az ATP szintézisét hajtják. Glükóz molekulánként (azaz két acetil-CoA molekulánként) a ciklus 6 NADH és 2 FADH₂ molekulát termel, amelyek mindegyike jelentős potenciális ATP hozamot képvisel az oxidatív foszforiláció során. Az ADP közvetlenül nem vesz részt a NADH és FADH₂ képződésében, de a ciklus sebességét közvetetten befolyásolja az ATP/ADP arány.
GTP/ATP termelés szubsztrát szinten
A citromsavciklus egyetlen szubsztrát szintű foszforilációs lépést tartalmaz, amely közvetlenül ATP-t (vagy GTP-t) termel. Ez a reakció a szukcinil-CoA szintetáz enzim által katalizált lépés, ahol a szukcinil-CoA tioszter kötésében tárolt energia felhasználásra kerül a GTP (guanozin-trifoszfát) szintézisére. A GTP molekula funkcionálisan egyenértékű az ATP-vel, és könnyen átalakítható ATP-vé egy másik enzim, a nukleozid-difoszfát kináz segítségével: GTP + ADP ⇌ GDP + ATP. Ebben a lépésben az ADP közvetlenül szubsztrátként vesz részt, átalakulva ATP-vé. Ez a reakció tehát egy közvetlen kapcsolat a citromsavciklus és az ADP-ATP ciklus között.
Az ADP mint szabályozó: A ciklus sebességének finomhangolása
Az ADP, mint a sejt alacsony energiaállapotának jelzője, kulcsszerepet játszik a citromsavciklus sebességének szabályozásában. Számos kulcsfontosságú enzim aktivitását befolyásolja allosztérikus úton:
- Izocitrát dehidrogenáz: Ez az enzim katalizálja az izocitrát oxidatív dekarboxilezését α-ketoglutarátra, NADH termelése mellett. Az ADP egy pozitív allosztérikus aktivátor az izocitrát dehidrogenáz számára. Amikor az ADP szint magas (azaz a sejtnek energiára van szüksége), az ADP kötődik az enzimhez, növelve annak aktivitását. Ez felgyorsítja a ciklust, ami több NADH és FADH₂ termeléséhez vezet, és ezáltal több ATP-t generál az oxidatív foszforilációban. Az ATP viszont negatív allosztérikus gátlója ennek az enzimnek, lassítva a ciklust, ha elegendő energia áll rendelkezésre.
- α-ketoglutarát dehidrogenáz komplex: Ez a komplex katalizálja az α-ketoglutarát oxidatív dekarboxilezését szukcinil-CoA-vá, szintén NADH termelése mellett. Bár az ADP közvetlen allosztérikus hatása kevésbé hangsúlyos, mint az izocitrát dehidrogenáz esetében, a NADH és a szukcinil-CoA, mint termékek, visszacsatolással gátolják a komplexet. Az ADP magas szintje közvetetten enyhítheti ezt a gátlást, jelezve az energiaigényt.
Az ADP tehát egy fontos molekuláris jel, amely biztosítja, hogy a citromsavciklus sebessége szinkronban legyen a sejt energiaigényével. Amikor a sejt energiaigénye megnő (magasabb ADP koncentráció), a ciklus felgyorsul, több NADH-t és FADH₂-t termelve, ami az oxidatív foszforiláció révén több ATP-t eredményez. Ez a precíz szabályozás alapvető a sejt metabolikus homeosztázisának fenntartásához és az energia hatékony termeléséhez aerob körülmények között.
„A citromsavciklus, bár közvetlenül kevés ATP-t ad, az ADP szabályozó hatásával válik a sejt aerob energiatermelésének motorjává, előkészítve a terepet az oxidatív foszforiláció gigantikus energiatermeléséhez.”
Az ADP és az ATP aránya folyamatosan monitorozza a sejt energiaállapotát, és ennek megfelelően hangolja a citromsavciklus aktivitását. Ez a finomhangolás kulcsfontosságú a metabolikus rugalmasság és az alkalmazkodóképesség szempontjából, lehetővé téve a sejtek számára, hogy optimalizálják az energiatermelést a különböző fiziológiai körülmények között.
Az ADP és az oxidatív foszforiláció: Az aerob ATP-generálás csúcsa
Az oxidatív foszforiláció az eukarióta sejtek legjelentősebb ATP-termelő folyamata, amely a mitokondrium belső membránján zajlik. Ez a komplex mechanizmus a táplálékmolekulák teljes lebontásából származó elektronok energiáját használja fel az ATP szintézisére. Az ADP itt nem csupán szubsztrát, hanem a folyamat sebességét meghatározó egyik legfontosabb tényező, amely szorosan összekapcsolja az elektrontranszport láncot az ATP szintézisével.
Mitokondriális elektrontranszport lánc: A proton-gradiens létrehozása
Az oxidatív foszforiláció két fő részből áll: az elektrontranszport láncból (ETL) és a kemiozmotikus ATP szintézisből. Az ETL egy sor fehérjekomplexből áll, amelyek a mitokondrium belső membránjában helyezkednek el (I-IV komplexek). A citromsavciklus és a glikolízis során termelt redukált koenzimek, a NADH és a FADH₂, átadják elektronjaikat az ETL-nek. Az elektronok az ETL komplexeken keresztül vándorolnak, miközben energiát veszítenek. Ez a felszabaduló energia arra használódik fel, hogy protonokat (H⁺ ionokat) pumpáljanak a mitokondriális mátrixból az intermembrán térbe. Ez a folyamat létrehoz egy elektrokémiai proton-grádienst a belső mitokondriális membránon keresztül, amely potenciális energiát tárol.
A proton-gradiens a mitokondriális belső membrán két oldalán eltérő protonkoncentrációt és töltéskülönbséget jelent. Ez a gradiens egyfajta „energiahordozó” állapot, amelyet a sejt felhasználhat. Az ADP közvetlenül nem vesz részt az elektrontranszport láncban, de a proton-gradiens fenntartása és az ATP szintézis sebessége szorosan összefügg az ADP rendelkezésre állásával.
Az ATP szintáz működése: Az ADP mint kulcsfontosságú szubsztrát
A proton-gradiens által tárolt energiát az ATP szintáz enzimkomplex használja fel az ATP szintézisére. Az ATP szintáz egy lenyűgöző molekuláris gép, amelynek két fő része van: az F₀ alegység, amely a membránba ágyazódik és protoncsatornaként funkcionál, és az F₁ alegység, amely a mitokondriális mátrixba nyúlik be, és katalizálja az ATP képződését. Amikor a protonok a proton-gradiensnek megfelelően visszaáramlanak az intermembrán térből a mátrixba az F₀ alegységen keresztül, az F₀ alegység forogni kezd. Ez a forgás mechanikai energiát generál, amelyet az F₁ alegység konformációs változásainak kiváltására használnak fel.
Az F₁ alegységben három aktív centrum található, amelyek ciklikusan váltakoznak három különböző állapot között:
- Nyitott (O) állapot: Alacsony affinitással köti az ADP-t és a Pi-t.
- Laza (L) állapot: Erősebben köti az ADP-t és a Pi-t.
- Szoros (T) állapot: Erősen köti az ADP-t és a Pi-t, és katalizálja az ATP szintézisét.
A forgás során az aktív centrumok átmennek az O → L → T → O állapotokon. A szoros (T) állapotban az ADP és az anorganikus foszfát (Pi) olyan szorosan kötődik az enzimhez, hogy az ATP szintézise gyakorlatilag spontán módon, energia befektetése nélkül megy végbe. Azonban az ATP felszabadulásához energia szükséges, ami a következő forgási lépésből származik, amikor az aktív centrum visszatér a nyitott állapotba. Az ADP tehát közvetlenül, mint szubsztrát vesz részt ebben a folyamatban, és a rendelkezésre állása alapvetően befolyásolja az ATP szintézis sebességét.
Az ADP mint a folyamat sebességét korlátozó tényező
Az oxidatív foszforiláció sebességét elsősorban az ADP és a Pi rendelkezésre állása szabályozza. Ezt nevezzük respirációs kontrollnak. Amikor a sejt energiaigénye megnő (pl. izommunka során), az ATP hidrolízise fokozódik, ami az ADP és Pi koncentrációjának növekedéséhez vezet. Ez az ADP és Pi növekedés serkenti az ATP szintázt, ami felgyorsítja a protonok áramlását a membránon keresztül, és ezzel az elektrontranszport lánc sebességét is. Az elektronok áramlása az elektrontranszport láncon keresztül csak akkor tud hatékonyan megtörténni, ha az ATP szintáz „levezeti” a proton-grádienst az ADP foszforilálásával.
Ha az ADP és Pi koncentrációja alacsony (azaz elegendő ATP van), az ATP szintáz aktivitása lelassul, a proton-gradiens megnő, és ez visszahat az elektrontranszport láncra, lassítva az elektronáramlást és az oxigénfogyasztást. Ez a szoros összekapcsolódás biztosítja, hogy a sejt csak akkor termeljen ATP-t nagy mennyiségben, amikor arra valóban szüksége van, elkerülve a felesleges hőtermelést és az anyagpazarlást.
Az oxidatív foszforiláció tehát egy rendkívül hatékony és finoman szabályozott folyamat, amelyben az ADP nem csupán egy reaktáns, hanem a sejt energiaállapotának közvetlen jelzője és a folyamat sebességét meghatározó kulcsfontosságú szabályozója. Az ADP rendelkezésre állása garantálja az élethez szükséges energia folyamatos és szabályozott termelését.
Az ADP és a fotoszintézis: Az élet alapvető energiaátalakítása
A fotoszintézis az a folyamat, amely során a növények, algák és bizonyos baktériumok a napfény energiáját kémiai energiává alakítják, szerves anyagokat szintetizálva a szén-dioxidból és vízből. Ez a folyamat alapvető az élet fenntartásához a Földön, és az ADP itt is, hasonlóan a sejtlégzéshez, kulcsfontosságú szerepet játszik az energiaátvitelben, különösen az ATP képződésében.
Fényreakciók (fotofoszforiláció): ATP és NADPH termelése
A fotoszintézis két fő szakaszra osztható: a fényfüggő reakciókra (vagy fényreakciókra) és a fényfüggetlen reakciókra (vagy Calvin-ciklusra). A fényreakciók a kloroplasztiszok tilakoid membránjában zajlanak, és a fényenergiát használják fel ATP és NADPH (redukált nikotinamid-adenin-dinukleotid-foszfát) előállítására. Ezek a molekulák szolgálnak majd energia- és redukciós erőforrásként a szén-dioxid fixálásához a Calvin-ciklusban.
A fényreakciók során a klorofill és más pigmentek elnyelik a fényenergiát, ami gerjeszti az elektronokat. Ezek az elektronok egy elektrontranszport láncon haladnak keresztül a tilakoid membránban. Az elektronok áramlása során protonok (H⁺ ionok) pumpálódnak a sztómából a tilakoid lumenbe, létrehozva egy proton-grádienst a tilakoid membránon keresztül. Ez a mechanizmus rendkívül hasonló az oxidatív foszforilációhoz, és a folyamatot fotofoszforilációnak nevezzük.
A proton-gradiens által tárolt potenciális energiát az ATP szintáz enzimkomplex használja fel, amely a tilakoid membránban helyezkedik el. Az ATP szintáz az ADP-t és az anorganikus foszfátot (Pi) ATP-vé foszforilálja, ahogy a protonok a grádiensnek megfelelően visszaáramlanak a tilakoid lumenből a sztómába. Az ADP tehát itt is, mint az oxidatív foszforilációban, szubsztrátként funkcionál az ATP szintéziséhez. A fényreakciók során termelt ATP a Calvin-ciklushoz szükséges energiát biztosítja.
Calvin-ciklus (ATP felhasználás): Az ADP regenerációja
A Calvin-ciklus a kloroplasztiszok sztómájában zajlik, és a fényreakciók során termelt ATP-t és NADPH-t használja fel a szén-dioxid fixálásához és cukrok szintéziséhez. Ez a ciklus három fő szakaszra bontható:
- Szén-dioxid fixáció: A CO₂ egy öt szénatomos cukorhoz, a ribulóz-1,5-biszfoszfáthoz (RuBP) kapcsolódik a RuBisCO enzim segítségével.
- Redukció: A fixált szén-dioxid molekulákat NADPH segítségével redukálják, és ATP felhasználásával foszforilálják, glicerinaldehid-3-foszfátot (G3P) képezve, amely a cukrok építőköve. Ebben a fázisban az ATP hidrolízise révén ADP és Pi keletkezik.
- RuBP regeneráció: A ciklus utolsó szakaszában a G3P molekulák egy részét felhasználják a ribulóz-1,5-biszfoszfát regenerálására, ami további ATP hidrolízist igényel, így ismét ADP keletkezik.
A Calvin-ciklusban tehát az ADP folyamatosan regenerálódik az ATP felhasználása során, majd visszakerül a tilakoid membránba, ahol a fényreakciók során újra ATP-vé foszforilálódik. Ez a ciklus biztosítja a fotoszintetikus szervezetek energiaellátásának folytonosságát.
„A fotoszintézisben az ADP a napfény energiájának közvetítőjévé válik, lehetővé téve a növények számára, hogy a Föld életét tápláló szerves anyagokat szintetizálják.”
Az ADP tehát elengedhetetlen a fotoszintézis mindkét fő szakaszában. A fényreakciók során szubsztrátként szolgál az ATP szintéziséhez, míg a Calvin-ciklusban az ATP hidrolízisével keletkezik, jelezve az energiafelhasználást és biztosítva a folyamatos ATP regenerációt. Ez a körforgás alapvető a szén-dioxid fixálásához és a szerves anyagok képződéséhez, amelyek az egész tápláléklánc alapját képezik.
Az ADP szerepe a jelátvitelben és sejtkommunikációban

Az ADP nem csupán az energiaanyagcserében játszik központi szerepet; egyre inkább felismerik, hogy jelentős jelátviteli molekula is, amely a sejtkommunikáció számos aspektusában részt vesz. Különösen fontos a purinerg receptorokon keresztül történő jelátvitelben, amelyek az extracelluláris nukleotidokat, így az ADP-t is felismerik. Ezek a jelátviteli utak alapvetőek a véralvadásban, a gyulladásos folyamatokban, az idegrendszeri működésben és számos más fiziológiai reakcióban.
P2Y és P2X purinerg receptorok
Az ADP, ATP és más purin nukleotidok extracelluláris jelmolekulaként működnek, és specifikus receptorokhoz, az úgynevezett purinerg receptorokhoz kötődnek. Két fő típusuk van:
- P2Y receptorok: Ezek G-protein-kapcsolt receptorok (GPCR-ek), amelyek aktiválásukkor intracelluláris jelátviteli kaszkádokat indítanak el. Az ADP a P2Y1, P2Y12 és P2Y13 receptorok specifikus agonistája. Ezek a receptorok a sejtmembránon helyezkednek el, és számos sejttípusban megtalálhatók, beleértve a vérlemezkéket, az endotélsejteket és az idegsejteket.
- P2X receptorok: Ezek ligandum-kapcsolt ioncsatornák, amelyek az ADP vagy ATP kötődésekor megnyílnak, lehetővé téve az ionok (pl. Ca²⁺, Na⁺) áramlását a sejtbe. Bár az ATP a P2X receptorok fő agonistája, az ADP is képes modulálni egyes P2X receptorok működését, vagy bizonyos körülmények között agonistaként hatni.
Az ADP kötődése ezekhez a receptorokhoz specifikus válaszokat vált ki a célsejtekben, amelyek messze túlmutatnak az energiaanyagcserén.
Vérlemezkék aggregációja (thrombus képződés)
Az ADP talán legismertebb jelátviteli szerepe a vérlemezkék aggregációjában rejlik, ami a vérzés megállításának (hemosztázis) és a vérrögképződésnek (trombózis) alapvető folyamata. Amikor egy érfal megsérül, a sérült sejtekből és a vörösvértestekből ADP szabadul fel a keringésbe. Ez az extracelluláris ADP azonnal aktiválja a vérlemezkéken található P2Y1 és P2Y12 receptorokat.
- A P2Y1 receptor aktiválása gyors, reverzibilis vérlemezke alakváltozást és aggregációt indít el, valamint Ca²⁺ felszabadulást okoz az intracelluláris raktárakból.
- A P2Y12 receptor aktiválása egy Gᵢ-proteinhez kapcsolódik, amely gátolja az adenilát-ciklázt, és csökkenti a cAMP szintjét a vérlemezkékben. Ez a cAMP szint csökkenés további vérlemezke aktivációhoz és stabil aggregációhoz vezet, valamint fokozza a fibrinogén receptorok (GPIIb/IIIa) affinitását, ami a vérlemezkék összetapadását eredményezi.
Ezek a folyamatok kulcsfontosságúak a vérrög kialakulásában. A P2Y12 receptor gátlása a modern trombózisellenes gyógyszerek (pl. klopidogrél, prasugrel, tikagrelor) egyik fő célpontja, amelyek megakadályozzák a vérlemezkék aggregációját szívinfarktus vagy stroke esetén.
Gyulladásos folyamatok
Az ADP részt vesz a gyulladásos válaszban is. Sérült vagy stresszes sejtekből felszabadulva az ADP aktiválhatja a P2Y receptorokat az immunsejteken (pl. makrofágok, neutrofilek, limfociták), modulálva azok működését. Például, az ADP stimulálhatja a citokin felszabadulást, befolyásolhatja a fagocitózist és a kemotaxist. Ez a szerep arra utal, hogy az ADP egyfajta „veszélyjelző” molekulaként is funkcionálhat, amely riasztja az immunrendszert egy sérülés vagy fertőzés esetén.
Idegrendszeri funkciók
Az agyban és a perifériás idegrendszerben is expresszálódnak purinerg receptorok, és az ADP szerepet játszik az idegsejtek közötti kommunikációban (neurotranszmisszió) és a gliasejtek működésében. Az ADP modulálhatja a szinaptikus átvitelt, befolyásolhatja a neuronális excitabilitást és részt vehet a fájdalomérzékelésben. Kutatások szerint az ADP szerepet játszik a neurodegeneratív betegségekben és az agyi ischaemiában is, ahol a felszabaduló ADP káros hatásokat válthat ki, vagy éppen védő szerepet tölthet be.
Az ADP tehát egy sokoldalú molekula, amely az energiaanyagcserén túlmenően, extracelluláris jelzőanyagként is funkcionál. Kötődése specifikus purinerg receptorokhoz széleskörű fiziológiai válaszokat vált ki, a vérzés megállításától az immunválasz szabályozásáig. Ennek a kettős szerepnek a megértése kulcsfontosságú a biológiai rendszerek komplexitásának és a gyógyszerfejlesztés új célpontjainak feltárásában.
Az ADP és a betegségek: Patofiziológiai vonatkozások
Az ADP, mint a sejt energiaanyagcseréjének és jelátvitelének központi molekulája, számos betegség patofiziológiájában is szerepet játszik. Az ADP anyagcsere vagy jelátviteli útjainak zavarai súlyos egészségügyi problémákhoz vezethetnek, a mitokondriális diszfunkcióktól a vérzési rendellenességekig, sőt a rákos megbetegedésekig. Ennek a molekulának a megértése kulcsfontosságú a diagnosztika és a terápiás beavatkozások fejlesztésében.
Mitokondriális diszfunkciók és energiahiányos állapotok
A mitokondriumok a sejtek „erőművei”, ahol az oxidatív foszforiláció révén az ATP nagy része termelődik. Az ADP kulcsfontosságú szubsztrátja az ATP szintáznak, és a rendelkezésre állása szabályozza az ATP termelés sebességét. Bármilyen zavar a mitokondriális működésben – legyen szó genetikai mutációkról, toxinokról vagy oxidatív stresszről – befolyásolhatja az ADP-ATP ciklust, és energiahiányos állapotokhoz vezethet.
Mitokondriális betegségek: Ezek olyan ritka, örökletes rendellenességek, amelyek a mitokondriális gének vagy a nukleáris gének mutációi miatt alakulnak ki, és befolyásolják a mitokondriális fehérjék, beleértve az elektrontranszport lánc komplexeit és az ATP szintázt. Az ilyen betegségekben a sejtek nem képesek elegendő ATP-t termelni, ami az ADP felhalmozódásához és krónikus energiahiányhoz vezet. Ez különösen súlyosan érinti a nagy energiaigényű szerveket, mint az agy, a szív és az izmok, ami neurológiai zavarokat, szívizombetegségeket és izomgyengeséget okozhat.
Ischaemia és reperfúziós sérülés: Oxigénhiányos állapotokban (ischaemia), például szívinfarktus vagy stroke esetén, az oxidatív foszforiláció leáll. Ez drasztikus ATP szint csökkenéshez és ADP/AMP felhalmozódáshoz vezet. Bár az ADP szint emelkedése kezdetben serkenti az anaerob glikolízist, ez nem elegendő az energiaigény fedezésére. A reperfúzió (oxigénellátás helyreállítása) során az ADP és más purin nukleotidok gyors felszabadulása tovább ronthatja a helyzetet a gyulladásos reakciók fokozásával és a vérlemezkék aktiválásával.
Vérzési rendellenességek és trombózis
Az ADP jelátviteli szerepe a vérlemezkék aktiválásában teszi a molekulát központi szereplővé a vérzési rendellenességek és a trombózis patofiziológiájában.
- Trombózis: A túlzott vérrögképződés (trombózis) súlyos következményekkel járhat, mint például szívinfarktus, stroke vagy mélyvénás trombózis. Ezekben az állapotokban az ADP által kiváltott vérlemezke-aggregáció kulcsfontosságú a kóros vérrögök kialakulásában. A P2Y12 receptor gátlása az anti-trombotikus terápia egyik sarokköve, amely megakadályozza az ADP által közvetített vérlemezke-aktivációt és aggregációt.
- Vérzési rendellenességek: Ritkán előfordulhatnak olyan genetikai rendellenességek, amelyek befolyásolják az ADP receptorok működését vagy az ADP felszabadulását a vérlemezkékből. Ezek az állapotok vérzési hajlamhoz vezethetnek, mivel a vérlemezkék nem képesek megfelelően aggregálódni a sérült érfalnál.
Rákos sejtek energiaanyagcseréje
A rákos sejtek gyakran megváltoztatják anyagcseréjüket, hogy támogassák gyors növekedésüket és osztódásukat. Ez az úgynevezett „Warburg-effektus”, ahol a rákos sejtek még oxigén jelenlétében is preferenciálisan anaerob glikolízissel termelnek energiát. Az ADP és ATP szintek, valamint az ADP-t szabályozó enzimek (pl. PFK-1) aktivitása jelentősen eltérhet a rákos sejtekben, befolyásolva a sejtproliferációt és a túlélést. Az ADP jelátviteli útjai is szerepet játszhatnak a rákos sejtek migrációjában és inváziójában, ami metasztázishoz vezethet. Az ADP metabolizmusának vagy jelátviteli útjainak modulálása potenciális terápiás célpont lehet a rákellenes kezelésekben.
Gyulladásos és autoimmun betegségek
Az ADP, mint gyulladásos mediátor, szerepet játszik számos gyulladásos és autoimmun betegségben. A sérült vagy stresszes szövetekből felszabaduló ADP aktiválhatja az immunsejteket, és hozzájárulhat a krónikus gyulladáshoz. A purinerg receptorok gátlása vagy modulálása ígéretes terápiás stratégia lehet olyan állapotokban, mint az ízületi gyulladás, asztma vagy gyulladásos bélbetegségek.
Az ADP tehát nem csupán egy ártatlan molekula a sejtben; annak hibás működése vagy szabályozása súlyos betegségekhez vezethet. A molekula szerkezetének, biológiai szerepének és jelátviteli útjainak mélyebb megértése kulcsfontosságú a modern orvostudomány számára a betegségek diagnosztizálásában, megelőzésében és hatékony kezelésében.
Az ADP analógok és a kutatás: Eszközök és terápiás ígéretek
Az ADP analógok olyan vegyületek, amelyek az ADP kémiai szerkezetéhez hasonlítanak, de valamilyen módosítást tartalmaznak. Ezeket az analógokat széles körben alkalmazzák a biokémiai és farmakológiai kutatásokban, hogy feltárják az ADP biológiai szerepét, az enzimekkel való kölcsönhatásait és a jelátviteli útvonalait. Emellett számos ADP-analóg alapú gyógyszer is létezik, vagy fejlesztés alatt áll, amelyek terápiás célokra szolgálnak, különösen a trombózisellenes kezelésekben.
Kutatási eszközök az ADP biológiai szerepének megértéséhez
Az ADP analógok lehetővé teszik a kutatók számára, hogy specifikusan beavatkozzanak az ADP-függő folyamatokba:
- Enzimkinetikai vizsgálatok: Az analógok használhatók kompetitív vagy nem-kompetitív gátlóként az ADP-t szubsztrátként használó enzimek (pl. ATP szintáz, kinázok) tanulmányozására. Segítségükkel meghatározhatók az enzimek kinetikai paraméterei és a kötőhelyek szerkezete.
- Receptor-ligandum kölcsönhatások: Az ADP analógok, különösen a stabil, nem hidrolizálható formák, ideálisak a purinerg receptorok (P2Y, P2X) kötőhelyeinek és aktivációs mechanizmusainak vizsgálatára. Különböző analógok szelektív kötődése segíthet az egyes receptoraltípusok azonosításában és funkcionális jellemzésében.
- Jelátviteli útvonalak elemzése: Az analógok segítségével megérthető, hogyan vált ki az ADP specifikus intracelluláris jelátviteli kaszkádokat, például a Ca²⁺ mobilizációt vagy a cAMP szint változását. Fluoreszcensen jelölt ADP analógok például nyomon követhetik az ADP mozgását és kötődését a sejten belül.
- Metabolikus fluxus vizsgálatok: Radioaktívan vagy stabil izotóppal jelölt ADP analógok felhasználhatók a metabolikus útvonalak fluxusának nyomon követésére, az ADP-ATP ciklus sebességének és szabályozásának kvantitatív elemzésére.
Ezek az eszközök alapvetőek az ADP molekuláris szintű működésének megértéséhez, és új terápiás célpontok azonosításához vezethetnek.
Gyógyszerészeti alkalmazások: A trombózisellenes szerek
Az ADP analógok legismertebb és legszélesebb körben alkalmazott gyógyszerészeti felhasználása a trombózisellenes kezelésben van. A P2Y12 receptor, amely a vérlemezkék felületén található, kulcsfontosságú az ADP által kiváltott vérlemezke aggregációban. Ennek a receptornak a gátlása hatékony módszer a vérrögképződés megelőzésére és kezelésére.
- Tienopiridinek (pl. Klopidogrél, Prasugrel): Ezek prodrogok, amelyek a szervezetben aktív metabolittá alakulnak, és irreverzibilisen gátolják a P2Y12 receptort. Az aktív metabolit kovalensen kötődik a receptorhoz, megakadályozva az ADP kötődését és a vérlemezke aktivációt. Széles körben alkalmazzák akut koronária szindróma (ACS) és perkután koronária intervenció (PCI) után a trombózis megelőzésére.
- Ciklopentil-triazolopirimidinek (pl. Tikagrelor): Ez egy reverzibilis, direkt P2Y12 receptor gátló, amely nem tienopiridin típusú. Nem prodrog, és közvetlenül kötődik a receptorhoz, gátolva az ADP-t. Gyorsabban hat és erősebb gátlást biztosít, mint a klopidogrél, és gyakran használják magas kockázatú ACS betegeknél.
Ezek a gyógyszerek az ADP jelátviteli útjainak modulálásával mentik meg életeket, és jelentősen javítják a kardiovaszkuláris betegségekben szenvedők prognózisát. A további kutatások újabb, még szelektívebb és biztonságosabb ADP receptor antagonisták kifejlesztését célozzák.
Egyéb potenciális terápiás alkalmazások
Az ADP jelátviteli útjainak modulálása más betegségek kezelésében is ígéretes lehet:
- Gyulladásos betegségek: Az ADP szerepe a gyulladásban azt sugallja, hogy a purinerg receptorok modulálása gyulladáscsökkentő hatású lehet.
- Fájdalomkezelés: Az ADP részt vesz a fájdalomérzékelésben az idegrendszerben, így az ADP receptor antagonisták potenciálisan fájdalomcsillapítóként is funkcionálhatnak.
- Rákellenes terápia: Az ADP metabolizmusának és jelátvitelének eltérései a rákos sejtekben új célpontokat kínálhatnak a rákellenes gyógyszerek számára.
Az ADP analógok és az ADP jelátviteli útjainak kutatása tehát folyamatosan bővíti tudásunkat erről a sokoldalú molekuláról, és új lehetőségeket nyit meg a diagnosztika és a terápiás beavatkozások terén. A jövőbeli kutatások valószínűleg még több, eddig ismeretlen szerepét tárják fel az ADP-nek, és még célzottabb gyógyszeres megoldásokat kínálnak.
A jövőbeli kutatási irányok és az ADP
Az ADP kutatása továbbra is dinamikusan fejlődik, ahogy egyre mélyebben megértjük komplex szerepét a sejtbiológiában és a fiziológiában. Bár a molekula alapvető energiaátviteli funkciói jól ismertek, az elmúlt években számos új, izgalmas kutatási irány bontakozott ki, amelyek az ADP jelátviteli és regulációs szerepeire fókuszálnak, új terápiás célpontokat és diagnosztikai lehetőségeket ígérve.
Újabb szerepek felfedezése a sejten kívüli térben
Az extracelluláris ADP, mint jelmolekula, egyre inkább a figyelem középpontjába kerül. Bár a vérlemezkék aktiválásában betöltött szerepe jól dokumentált, a kutatók most azt vizsgálják, hogy az ADP milyen más sejttípusokat befolyásol, és milyen fiziológiai vagy patofiziológiai folyamatokban vesz részt.
- Immunmoduláció: Az ADP befolyásolja az immunsejtek (pl. makrofágok, dendritikus sejtek, limfociták) működését, aktiválhatja vagy modulálhatja azok válaszát. A jövőbeli kutatások feltárhatják az ADP szerepét krónikus gyulladásos betegségekben, autoimmunitásban és fertőzésekre adott válaszokban.
- Neurodegeneráció és neuroplaszticitás: Az agyban az extracelluláris ADP-szintek változása befolyásolhatja a szinaptikus plaszticitást, a neuronális túlélést és a gliasejtek működését. Ez utat nyithat az ADP-alapú terápiáknak neurodegeneratív betegségek (pl. Alzheimer-kór, Parkinson-kór) és agyi sérülések kezelésében.
- Csontanyagcsere: Egyre több bizonyíték utal arra, hogy az ADP és a purinerg receptorok szerepet játszhatnak a csontképződésben és a csontreszorpcióban, befolyásolva az oszteoblasztok és oszteoklasztok aktivitását.
Az ADP metabolizmusának és transzportjának finomhangolása
Az ADP intracelluláris és extracelluláris koncentrációját szigorúan szabályozzák különböző enzimek (pl. adenilát kináz, nukleozid-difoszfát kináz) és transzporterek. A jövőbeli kutatások egyre inkább ezekre a szabályozó mechanizmusokra fókuszálnak:
- ADP/ATP transzlokátorok: Ezek a mitokondriális membránban található transzporterek felelősek az ADP bejuttatásáért a mátrixba és az ATP kiviteléért a citoplazmába. A transzlokátorok diszfunkciója súlyos energiahiányos állapotokhoz vezethet, és potenciális terápiás célpont lehet mitokondriális betegségekben.
- Ecto-ATPázok és Ecto-ADPázok: Ezek a sejtfelszíni enzimek szabályozzák az extracelluláris ATP és ADP szinteket, befolyásolva a purinerg receptorokon keresztül történő jelátvitelt. Ezen enzimek modulálása új terápiás stratégiákat kínálhat.
Terápiás célpontok az ADP útvonalakon
A P2Y12 receptor antagonisták sikere a trombózis kezelésében inspirálja a kutatókat, hogy más ADP-függő útvonalakat is megcélozzanak terápiás célokra.
- Szelektívebb P2Y receptor antagonisták: A jövőbeli gyógyszerek még szelektívebben gátolhatják az egyes P2Y receptor altípusokat, minimalizálva a mellékhatásokat és célzottabb terápiát biztosítva.
- P2X receptor modulátorok: Bár az ATP a fő ligandum, az ADP moduláló hatása a P2X receptorokon keresztül is kutatási területet jelent, különösen a fájdalom, gyulladás és neurodegeneratív betegségek kezelésében.
- Az ADP anyagcsere enzimeinek gátlása: Az ADP szintjét szabályozó enzimek gátlása vagy aktiválása szintén ígéretes terápiás stratégia lehet.
A jövőbeli kutatások valószínűleg integrálják az ADP-re vonatkozó molekuláris, sejtes és rendszerszintű megfigyeléseket, hogy teljesebb képet kapjunk ennek a fundamentális molekulának a biológiai komplexitásáról. A technológiai fejlődés, mint például a nagy áteresztőképességű szűrés (high-throughput screening) és a génszerkesztési technikák (pl. CRISPR-Cas9), felgyorsítja majd az új ADP-vel kapcsolatos felfedezéseket. Az ADP-vel kapcsolatos ismeretek elmélyítése nemcsak az alapvető biológiai folyamatok megértését segíti elő, hanem új utakat nyit meg számos súlyos betegség diagnosztizálásában és kezelésében is.