Elgondolkodtunk már azon, hogyan képesek sejtjeink, melyek a legapróbb biológiai egységeink, fenntartani belső egyensúlyukat, felvenni a tápanyagokat, megszabadulni a salakanyagoktól, és pontosan kommunikálni egymással egy rendkívül komplex és dinamikus környezetben? A válasz a biológiai membránok áthatolhatatlannak tűnő, mégis rendkívül szelektív falában rejlik, és abban, hogy ezt a falat speciális molekuláris gépezetek, a szállító fehérjék hálózzák be. Ezek a lenyűgöző szerkezetek nem csupán passzív kapuk, hanem aktív, szabályozott rendszerek, amelyek nélkül az élet, ahogy ismerjük, elképzelhetetlen lenne.
A szállító fehérjék a sejtélet alapkövei, hiszen ők felelnek azért, hogy a megfelelő molekulák a megfelelő időben és a megfelelő helyre jussanak. Nélkülük a sejt nem tudna felvenni cukrot, aminosavakat, ionokat, vagy éppen megszabadulni a metabolikus végtermékektől. Ez a cikk részletesen bemutatja ezen létfontosságú fehérjék sokféleségét, működési elveit és azt a kritikus szerepet, amit a biológiai rendszerekben betöltenek, az egysejtű organizmusoktól az emberi test legösszetettebb fiziológiai folyamataiig.
A sejtmembrán mint szelektív határ és a transzport szükségessége
A sejt létét és integritását a sejthártya, vagy más néven plazmamembrán biztosítja, amely elválasztja a sejt belső, rendezett környezetét a külső, gyakran kaotikus világtól. Ez a membrán nem egy egyszerű gát, hanem egy dinamikus, folyékony mozaikmodell szerint felépülő struktúra, melynek alapja a lipid kettősréteg. A hidrofób lipid farokréteg miatt a membrán alapvetően átjárhatatlan a vízoldékony, poláris molekulák és az ionok számára.
Gyakran esik szó arról, hogy a membrán „szelektíven permeábilis”. Ez azt jelenti, hogy bizonyos anyagok viszonylag könnyen átjutnak rajta (például kis, nem poláris molekulák, mint az oxigén, szén-dioxid, vagy a zsírban oldódó molekulák), míg mások, különösen a nagyobb, töltött vagy erősen poláris molekulák, csak speciális mechanizmusok, azaz a szállító fehérjék segítségével kelhetnek át rajta.
A sejteknek folyamatosan szüksége van tápanyagokra (glükóz, aminosavak, vitaminok, ionok), és el kell távolítaniuk a salakanyagokat (karbamid, laktát), valamint fenn kell tartaniuk a belső ionkoncentrációk, a pH és a vízegyensúly pontos szabályozását. Ezeket a feladatokat a membrán transzport folyamatai látják el, amelyek két fő kategóriába sorolhatók: a passzív transzportba és az aktív transzportba.
A szállító fehérjék általános jellemzői és működési elvei
A szállító fehérjék nem csupán lyukak a membránon, hanem rendkívül kifinomult molekuláris gépezetek, melyek speciális tulajdonságokkal rendelkeznek. Ezek a tulajdonságok alapvetően meghatározzák, hogyan és milyen hatékonysággal képesek ellátni feladatukat.
A legfontosabb jellemzők közé tartozik a specificitás. Egy adott szállító fehérje általában csak egy bizonyos típusú molekulát, vagy egy szűk molekulacsoportot képes átjuttatni a membránon. Például a glükóz transzporterek (GLUT) kizárólag glükózt és néhány hasonló szerkezetű hexózt képesek szállítani, míg az aminosav transzporterek specifikusak az aminosavakra. Ez a specificitás a fehérje kötőhelyeinek térbeli szerkezetéből adódik, amely pontosan illeszkedik a szállítandó molekulához, akárcsak egy kulcs a zárba.
Egy másik kulcsfontosságú tulajdonság a telíthetőség. Mivel a szállító fehérjék száma egy adott membránfelületen véges, a szállítás sebessége nem növelhető a végtelenségig a szubsztrát koncentrációjának emelésével. Egy bizonyos koncentráció felett az összes elérhető szállító fehérje telítetté válik, és a szállítás maximális sebességgel zajlik. Ez a jelenség hasonló az enzimek működéséhez, és biokémiai szempontból is jelentős.
A kompetíció is gyakori jelenség. Amennyiben két, szerkezetileg hasonló molekula is képes kötődni ugyanahhoz a szállító fehérjéhez, akkor versengeni fognak egymással a kötőhelyekért. Ez a verseny befolyásolhatja az egyes molekulák szállítási sebességét, és gyógyszerészeti szempontból is fontos lehet, mivel bizonyos gyógyszerek gátolhatják a természetes szubsztrátok felvételét vagy kiválasztását.
A konformációs változások a szállító fehérjék működésének alapját képezik. A legtöbb szállító fehérje úgy működik, hogy a szállítandó molekula megkötése után térbeli szerkezete megváltozik, ami lehetővé teszi a molekula átjutását a membránon. Ez a változás lehet finom reorientáció vagy jelentősebb alakváltozás. A konformációs változás egy energiaigényes folyamat is lehet, különösen az aktív transzport esetében.
Végül, de nem utolsósorban, a szabályozás. A sejtek képesek szabályozni a szállító fehérjék aktivitását és számát a membránban, alkalmazkodva a változó környezeti feltételekhez és a sejt fiziológiai igényeihez. Ez a szabályozás történhet foszforilációval, alloszterikus modulációval, vagy a fehérjék szintézisének és lebontásának szabályozásával. Ez a komplex szabályozás biztosítja a sejt homeosztázisának precíz fenntartását.
Passzív transzport fehérjék: a gradiens mentén
A passzív transzport olyan folyamat, amely nem igényel közvetlen energiafelhasználást a sejttől. A szállított molekulák a koncentrációgradiensük, az elektrokémiai gradiensük vagy a nyomásgradiensük mentén mozognak, a magasabb koncentrációjú helyről az alacsonyabb koncentrációjú felé. Bár a passzív transzport alapja a diffúzió, a szállító fehérjék jelentősen felgyorsíthatják ezt a folyamatot. Két fő típusa van: a csatorna fehérjék által mediált transzport és a hordozó fehérjék (karrier fehérjék) által mediált, más néven facilitált diffúzió.
Csatorna fehérjék: nyitott kapuk az ionok és a víz számára
A csatorna fehérjék, különösen az ioncsatornák, hidrofil pórusokat hoznak létre a membránban, amelyeken keresztül a specifikus ionok vagy a víz szabadon, nagy sebességgel áthaladhatnak a koncentrációgradiensüknek megfelelően. Ezek a csatornák nem kötődnek erősen a szállítandó molekulához, hanem inkább egyfajta „alagútként” működnek. Működésük gyakran szabályozott, azaz „kapuzottak”, ami azt jelenti, hogy képesek nyitott vagy zárt állapotban lenni.
Az ioncsatornák a biológiai membránok egyik legfontosabb alkotóelemei, különösen az ingerlékeny sejtekben, mint az ideg- és izomsejtek. Különböző típusai léteznek:
- Feszültségfüggő csatornák: Ezek a csatornák a membránpotenciál változására reagálnak. Például az idegsejtekben található feszültségfüggő Na+ csatornák és K+ csatornák felelősek az akciós potenciál kialakulásáért és terjedéséért, lehetővé téve az idegimpulzusok gyors továbbítását. A Ca2+ csatornák szintén feszültségfüggőek lehetnek, és fontos szerepet játszanak az izomkontrakcióban és a neurotranszmitterek felszabadulásában.
- Ligandfüggő csatornák: Ezek a csatornák egy specifikus molekula (ligand) kötődésére nyílnak vagy záródnak. A ligand lehet extracelluláris (pl. neurotranszmitterek, mint az acetilkolin a nikotinos acetilkolin receptoron) vagy intracelluláris (pl. cAMP vagy cGMP). Például a GABA-receptor egy kloridion csatorna, amely a GABA neurotranszmitter hatására nyílik ki, gátló hatást kiváltva az idegsejtekben.
- Mechanikusan kapuzott csatornák: Ezek a csatornák mechanikai ingerekre, mint például nyomásra, feszülésre vagy rezgésre reagálnak. Fontos szerepet játszanak a tapintás, hallás és egyensúlyérzékelés folyamataiban.
Egy speciális csatorna típus az aquaporin, amely a víz molekulák rendkívül gyors és szelektív áramlását teszi lehetővé a membránon keresztül. Bár a víz önmagában is képes lassan átjutni a lipid kettősrétegen, az aquaporinok drámaian felgyorsítják ezt a folyamatot, ami létfontosságú a vese vízvisszaszívásában, a sejtek ozmotikus egyensúlyának fenntartásában és a növényi víztranszportban.
Hordozó fehérjék (karrier fehérjék): a facilitált diffúzió mesterei
A hordozó fehérjék, vagy más néven karrier fehérjék, szintén a passzív transzport részét képezik, de működési elvük eltér a csatorna fehérjékétől. Ezek a fehérjék specifikusan megkötik a szállítandó molekulát az egyik oldalon, majd konformációs változáson mennek keresztül, ami a molekulát a membrán másik oldalára juttatja, ahol az leválik. Ez a folyamat a facilitált diffúzió.
A facilitált diffúzió sebessége sokkal nagyobb, mint az egyszerű diffúzióé, de a csatorna fehérjékénél lassabb, mivel minden egyes molekula szállítása egy konformációs változással jár.
A karrier fehérjékre is jellemző a specificitás, telíthetőség és kompetíció. Kiváló példa erre a glükóz transzporterek (GLUT család). Az emberi szervezetben legalább 14 különböző GLUT izoforma létezik, mindegyik specifikus szöveti eloszlással és funkcióval. Például a GLUT1 az agyban és a vörösvértestekben található meg, biztosítva a folyamatos glükózellátást. A GLUT2 a májban, vesében és hasnyálmirigyben játszik szerepet, alacsony affinitással, de nagy kapacitással szállítva a glükózt. A GLUT4 pedig az inzulinérzékeny szövetekben (izom, zsír) expresszálódik, és inzulin hatására a sejtmembránra transzlokálódik, növelve a glükóz felvételt.
Más karrier fehérjék szállítanak aminosavakat, nukleozidokat és számos más kis molekulát. Ezek a rendszerek kulcsfontosságúak a tápanyagok felszívódásában a bélben, a vesékben való visszaszívásban és a sejtek anyagcsere-folyamatainak fenntartásában.
Aktív transzport fehérjék: az energiaigényes szállítás
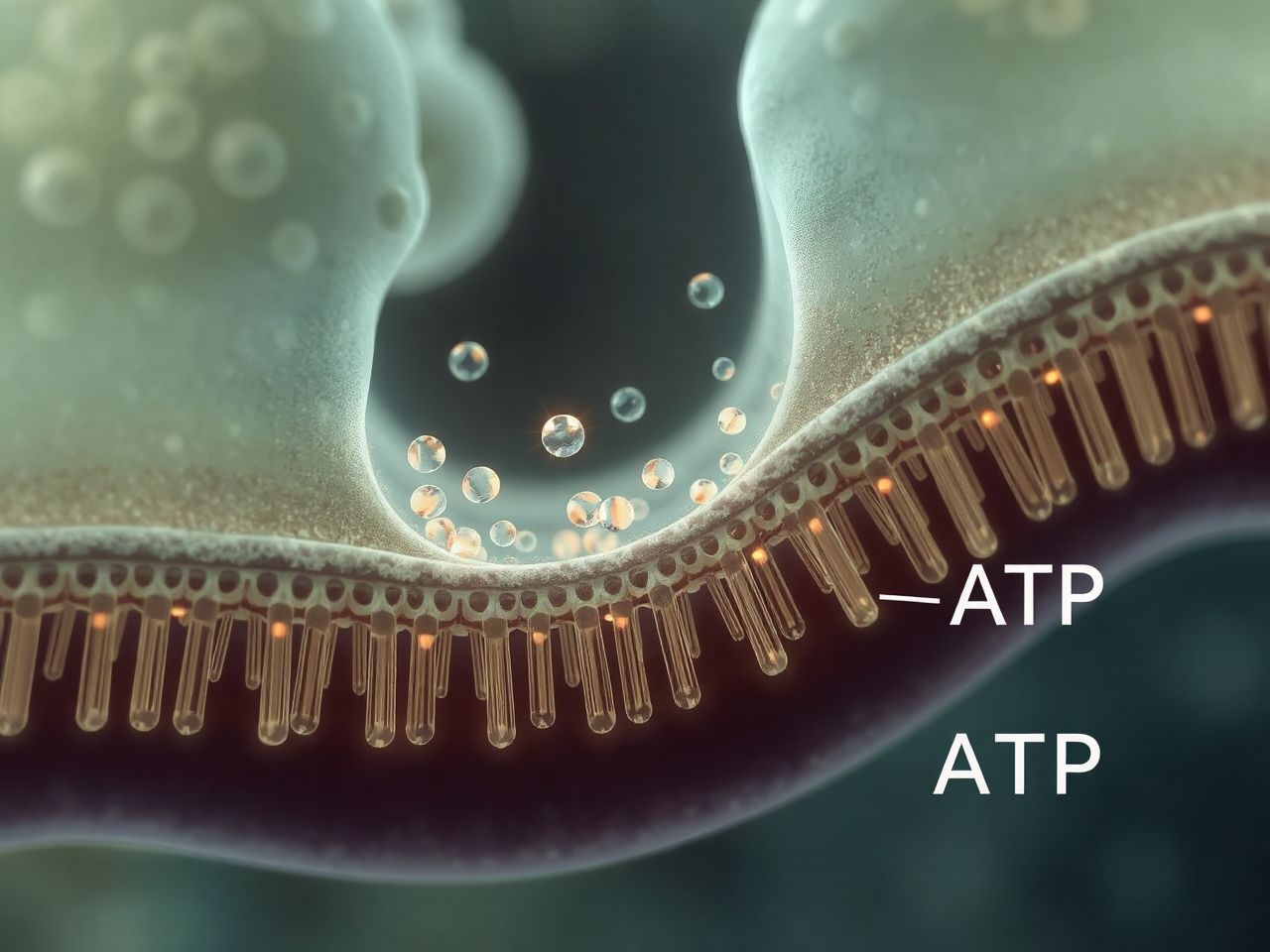
Az aktív transzport olyan folyamat, amely energiafelhasználást igényel ahhoz, hogy a molekulákat a koncentrációgradiensük *ellenében*, azaz az alacsonyabb koncentrációjú helyről a magasabb koncentrációjú felé szállítsa. Ez a „gradiens elleni” szállítás létfontosságú a sejtek ionegyensúlyának fenntartásához, a tápanyagok felhalmozásához és a salakanyagok eltávolításához. Két fő kategóriába sorolható: a primer aktív transzportba és a szekunder aktív transzportba.
Primer aktív transzport (pumpák): közvetlen energiafelhasználás
A primer aktív transzport során a szállító fehérje közvetlenül használ fel energiát, jellemzően ATP hidrolíziséből származót, a molekulák mozgatásához. Ezeket a fehérjéket gyakran pumpa fehérjéknek nevezik. Az ATP hidrolízise során felszabaduló energia konformációs változást idéz elő a fehérjében, ami lehetővé teszi a szubsztrát gradiens elleni szállítását.
A legfontosabb példák közé tartoznak:
- Na+/K+-ATPáz (Nátrium-kálium pumpa): Talán a legismertebb és leginkább tanulmányozott primer aktív transzporter. Ez a pumpa minden állati sejt plazmamembránjában megtalálható, és létfontosságú az iongradiens fenntartásában. Minden egyes működési ciklus során 3 Na+ iont pumpál ki a sejtből és 2 K+ iont pumpál be a sejtbe, egy ATP molekula hidrolízise árán. Ez a folyamat hozza létre és tartja fenn a sejt nyugalmi membránpotenciálját, ami alapvető az idegimpulzusok, az izomkontrakció és számos más celluláris folyamat szempontjából.
- Ca2+-ATPáz (Kálcium pumpa): A sejtekben a citoplazmatikus Ca2+ koncentrációt rendkívül alacsonyan kell tartani, mivel a kalcium fontos intracelluláris jelzőmolekula. A Ca2+-ATPázok a plazmamembránban és az endoplazmatikus/szarkoplazmatikus retikulum membránjában is megtalálhatók, ahonnan Ca2+ ionokat pumpálnak ki a sejtből vagy be a retikulumba, szintén ATP hidrolízissel. Ez a folyamat kulcsfontosságú az izomrelaxációban (szarkoplazmatikus retikulum Ca2+-ATPáza) és a sejtjelátviteli utak szabályozásában.
- H+-ATPáz (Protonpumpák): Ezek a pumpák protonokat (H+ ionokat) szállítanak, és számos helyen megtalálhatók. A lizoszómák membránjában például H+-ATPázok pumpálják be a protonokat, savas környezetet teremtve, ami szükséges a lizoszómális enzimek működéséhez. A gyomor savtermelését is egy speciális H+/K+-ATPáz biztosítja. A mitokondriumok belső membránjában található ATP-szintáz is egyfajta protonpumpa, amely a proton gradiens energiáját használja fel az ATP szintézisére.
- ABC transzporterek (ATP-Binding Cassette transzporterek): Ez egy rendkívül nagy és sokszínű fehérjecsalád, amely prokarióta és eukarióta sejtekben egyaránt megtalálható. Jellemzőjük, hogy két ATP-kötő doménnel (ABC kazetta) rendelkeznek. Az ABC transzporterek képesek kis molekulákat, ionokat, lipideket, gyógyszereket és egyéb metabolitokat szállítani a membránon keresztül. Számos tagjuknak kiemelkedő orvosi jelentősége van. Például a P-glikoprotein (MDR1 vagy ABCB1) gyógyszerek kiválasztásáért felelős a bélben és a vér-agy gáton, és jelentős szerepet játszik a multidrog rezisztencia kialakulásában a rákos sejtekben. A cisztás fibrózis transzmembrán konduktancia regulátor (CFTR), amely egy kloridion csatorna, szintén egy ABC transzporter. Ennek hibás működése okozza a cisztás fibrózist.
Szekunder aktív transzport (kotranszporterek): a gradiens erejének kihasználása
A szekunder aktív transzport során a molekulák gradiens elleni szállítása közvetve használ fel energiát. Nem közvetlenül ATP hidrolíziséből származót, hanem egy másik ion (leggyakrabban Na+ vagy H+) előzőleg létrehozott elektrokémiai gradiensének energiáját. Ezeket a fehérjéket kotranszportereknek nevezik, és mindig két vagy több molekulát szállítanak egyszerre.
Két fő típusa van:
- Szimport (együttszállítás): Ebben az esetben a két molekula azonos irányba halad át a membránon. A leggyakoribb példa a Na+/glükóz kotranszporter (SGLT), amely a vékonybél hámsejtjeiben és a vese tubulusaiban található. Itt a Na+ ionok a koncentrációgradiensük mentén áramlanak be a sejtbe, és ezt az energiát használják fel a glükóz gradiens elleni szállítására. Ez teszi lehetővé a glükóz teljes felszívódását a táplálékból és a vesében a vizeletből.
- Antiport (ellenirányú szállítás): Itt a két molekula ellentétes irányba mozog. Egyikük a gradiens mentén halad, a másik a gradiens ellenében. Egy jó példa a Na+/Ca2+ kicserélő, amely a szívizomsejtekben és más sejtekben található. Ez a transzporter 3 Na+ iont visz be a sejtbe és 1 Ca2+ iont pumpál ki a sejtből. Ez segít fenntartani az alacsony intracelluláris Ca2+ koncentrációt, ami fontos a szívizom relaxációjához. Hasonlóan működik a Na+/H+ kicserélő is, amely a pH szabályozásában játszik szerepet.
A szekunder aktív transzport mechanizmusai kulcsfontosságúak a tápanyagok felszívódásában (aminosavak, vitaminok mellett a glükóz), a sejtek pH-jának szabályozásában és az ionhomeosztázis fenntartásában.
Intracelluláris szállító fehérjék: a sejten belüli logisztika
A szállító fehérjék szerepe nem korlátozódik csupán a sejtek külső membránján keresztüli transzportra. A sejten belül is számos molekula szállításáról gondoskodnak, biztosítva az anyagok megfelelő eljutását a különböző organellumokhoz, vagy éppen a test távoli részeire. Ezek a fehérjék nem feltétlenül membránhoz kötöttek, hanem szabadon lebegnek a citoplazmában vagy más testfolyadékokban.
Hemoglobin és mioglobin: az oxigén hordozói
A hemoglobin az egyik legismertebb és legfontosabb szállító fehérje az emberi szervezetben. A vörösvértestekben található, és fő feladata az oxigén szállítása a tüdőből a test szöveteibe. Négy alegységből álló komplex fehérje, mely mindegyik alegységében tartalmaz egy hem csoportot, ami vasat tartalmaz, és képes reverzibilisen megkötni egy oxigén molekulát. A hemoglobin egyedülálló képessége, az úgynevezett kooperatív kötés, lehetővé teszi, hogy az oxigénkötés az egyik alegységen növeli a többi alegység oxigénkötő affinitását, ami hatékony oxigénfelvételt tesz lehetővé a tüdőben és oxigénleadást a szövetekben.
A mioglobin szerkezetileg és funkcionálisan rokona a hemoglobinnak, de egyetlen alegységből áll, és egyetlen hem csoportot tartalmaz. Főként az izomsejtekben található, ahol az oxigént tárolja, és szükség esetén gyorsan leadja az intenzíven dolgozó izmoknak. Mivel a mioglobin oxigénkötő affinitása magasabb, mint a hemoglobiné, képes „elrabolni” az oxigént a hemoglobintól a szövetekben, biztosítva az izmok oxigénellátását.
Szérum albumin: a vérplazma univerzális szállítója
A szérum albumin a legbőségesebben előforduló fehérje a vérplazmában, és rendkívül sokoldalú szállítóként funkcionál. Képes megkötni és szállítani a vérben számos hidrofób molekulát, amelyek önmagukban nem lennének oldékonyak a vizes plazmában. Ezek közé tartoznak a zsírsavak, amelyek az energiaellátásban játszanak szerepet, különböző hormonok (pl. pajzsmirigyhormonok, szteroidhormonok), gyógyszerek (számos gyógyszer kötődik az albuminhoz, befolyásolva ezzel a biológiai hozzáférhetőségüket és hatásukat), valamint bilirubint és egyéb metabolitokat. Az albumin emellett hozzájárul a vér kolloid ozmotikus nyomásának fenntartásához is, ami alapvető a folyadékegyensúly szempontjából.
Transzferrin: a vas precíz utazása
A transzferrin egy glikoprotein, amely a vas ionok (Fe3+) szállításáért felelős a vérben. A vas egy esszenciális nyomelem, amely számos enzim és fehérje (pl. hemoglobin) működéséhez nélkülözhetetlen, de szabad formában rendkívül toxikus. A transzferrin szorosan megköti a vasat, megakadályozva annak toxikus hatásait, és elszállítja a vasat igénylő sejtekhez, például a vörösvértestek előalakjaihoz a csontvelőben. A sejtek a transzferrin receptorok segítségével veszik fel a transzferrin-vas komplexet, majd a vas felszabadítása után a transzferrin visszakerül a keringésbe. A vasanyagcsere zavarai, mint például a vashiányos anémia, gyakran a transzferrin vagy a transzferrin receptorok működésének rendellenességeivel is összefüggésben állnak.
Lipoproteinek: a lipidek komplex hordozói
A lipoproteinek komplex részecskék, amelyek lipidekből (koleszterin, trigliceridek, foszfolipidek) és fehérjékből (apolipoproteinek) állnak. Fő feladatuk a hidrofób lipidek szállítása a vérplazmában. A lipoproteinek különböző típusai léteznek, amelyek méretükben, sűrűségükben és apolipoprotein tartalmukban különböznek. Ezek közé tartoznak a kilomikronok (táplálékból származó zsírok szállítása), a VLDL (very-low-density lipoprotein), az LDL (low-density lipoprotein) és a HDL (high-density lipoprotein). Az LDL felelős a koleszterin szállításáért a májból a szövetekbe, míg a HDL a felesleges koleszterint szállítja vissza a szövetekből a májba (reverz koleszterin transzport). A lipoprotein anyagcsere zavarai, különösen az emelkedett LDL és alacsony HDL szint, szorosan összefüggnek a szív- és érrendszeri betegségek kockázatával.
Egyéb specifikus intracelluláris szállítók
Számos más specifikus szállító fehérje is létezik a sejten belül. Például a retinol kötő fehérjék (RBP) a A-vitamin (retinol) szállításáért felelősek a vérben és a sejtekben. A tiroxin kötő globulin (TBG) a pajzsmirigyhormonok szállításában játszik kulcsszerepet. Ezek a fehérjék mind hozzájárulnak a precíz és szabályozott anyagforgalomhoz a szervezetben.
A szállító fehérjék szabályozása: a sejt alkalmazkodóképessége
A szállító fehérjék aktivitása és expressziója rendkívül szigorúan szabályozott, ami lehetővé teszi a sejtek és az egész szervezet számára, hogy alkalmazkodjanak a változó környezeti feltételekhez és fiziológiai igényekhez. Ez a szabályozás több szinten is megvalósulhat, biztosítva a homeosztázis precíz fenntartását.
Poszttranszlációs módosítások
Az egyik leggyakoribb szabályozási mechanizmus a foszforiláció és defoszforiláció. Számos szállító fehérje tartalmaz specifikus aminosav-maradékokat (szerin, treonin, tirozin), amelyek foszforilálhatók (foszfátcsoport köthető hozzájuk) kináz enzimek által, vagy defoszforilálhatók foszfatáz enzimek által. Ez a reverzibilis folyamat megváltoztathatja a fehérje konformációját, ezáltal növelve vagy csökkentve annak affinitását a szállított molekulához, vagy befolyásolva a szállítási sebességet. Például a GLUT4 transzporter inzulin által stimulált transzlokációja a membránra, részben foszforilációs kaszkádok révén történik.
Alloszterikus szabályozás
Az alloszterikus szabályozás során egy molekula (alloszterikus effektor) kötődik a szállító fehérje egy, a szubsztrátkötő helytől eltérő pontjához. Ez a kötődés konformációs változást idéz elő a fehérjében, ami befolyásolja a szubsztrátkötő hely affinitását vagy a szállítási sebességet. Az alloszterikus effektorok lehetnek aktivátorok vagy gátlók. Ez a mechanizmus lehetővé teszi a gyors és finomhangolt válaszokat a sejt metabolikus állapotára vagy a környezeti jelekre.
Fehérje expresszió és lokalizáció
A sejtek képesek szabályozni a szállító fehérjék mennyiségét is a membránban. Ez történhet a génexpresszió szintjén (azaz több vagy kevesebb mRNS termelődik, amiből aztán fehérje szintetizálódik), vagy a már meglévő fehérjék lebontásának szabályozásával. Emellett a fehérjék lokalizációja is szabályozott lehet. Egyes szállító fehérjék, mint például a GLUT4, raktározódnak a sejt belsejében vezikulákban, és csak specifikus jelek (pl. inzulin) hatására transzlokálódnak a plazmamembránra, ahol kifejthetik hatásukat. Ez egy gyors és hatékony módja a szállítási kapacitás változtatásának.
Hormonális és egyéb jelátviteli hatások
Számos szállító fehérje aktivitását és expresszióját hormonok és más jelátviteli molekulák szabályozzák. Az inzulin hatása a GLUT4-re már említésre került. A pajzsmirigyhormonok befolyásolják a Na+/K+-ATPáz aktivitását, hozzájárulva a hőtermeléshez. A vesében az antidiuretikus hormon (ADH) az aquaporinok membránba való beépülését stimulálja, növelve a víz visszaszívását. Ezek a komplex szabályozó hálózatok biztosítják a sejtek és a szervek közötti koordinált működést.
A szállító fehérjék biológiai jelentősége és orvosi relevanciája
A szállító fehérjék nem csupán az alapvető celluláris folyamatok biztosítékai, hanem számos betegség patogenezisében is kulcsszerepet játszanak. Működésük megértése elengedhetetlen a betegségek diagnosztizálásához, kezeléséhez és új terápiás stratégiák kidolgozásához.
Homeosztázis fenntartása
A szállító fehérjék alapvetőek a homeosztázis, azaz a belső környezet állandóságának fenntartásában. Az ioncsatornák és pumpák, mint a Na+/K+-ATPáz, precízen szabályozzák az intracelluláris és extracelluláris ionkoncentrációkat (Na+, K+, Ca2+, Cl-, H+). Ez létfontosságú a sejt térfogatának, a membránpotenciálnak és a pH-nak a szabályozásához. Bármilyen zavar ezekben a mechanizmusokban súlyos következményekkel járhat, például sejtek duzzadásához vagy zsugorodásához, vagy a sejt működésének összeomlásához vezethet.
Tápanyagfelvétel és kiválasztás
A bélrendszerben a szállító fehérjék felelősek a táplálékból származó glükóz, aminosavak, vitaminok és ásványi anyagok felszívódásáért. A vesékben pedig ezek a fehérjék biztosítják a vér szűrését, a hasznos anyagok (glükóz, aminosavak, ionok, víz) visszaszívását és a salakanyagok kiválasztását a vizeletbe. A májban szintén számos transzporter vesz részt a metabolitok és a gyógyszerek feldolgozásában és kiválasztásában. Ezen rendszerek hibás működése tápanyaghiányhoz, elektrolit-egyensúly zavarokhoz vagy toxikus anyagok felhalmozódásához vezethet.
Jelátvitel és idegrendszeri működés
Az ioncsatornák a jelátvitel alapkövei, különösen az idegrendszerben. Az akciós potenciál generálása és terjedése a feszültségfüggő Na+ és K+ csatornák koordinált működésén alapul. A szinapszisokban a ligandfüggő ioncsatornák és a neurotranszmitter transzporterek (pl. szerotonin, dopamin, noradrenalin visszavételét végző transzporterek) szabályozzák a jelátvitelt. Ezeknek a transzportereknek a diszfunkciója számos neurológiai és pszichiátriai betegséghez (pl. epilepszia, depresszió, Parkinson-kór) köthető.
Gyógyszerhatások és toxikológia
A szállító fehérjék rendkívül fontosak a gyógyszerek farmakokinetikájában, azaz a gyógyszerek felszívódásában (Absorption), eloszlásában (Distribution), metabolizmusában (Metabolism) és kiválasztásában (Excretion) (ADME). Számos gyógyszer vagy a szállító fehérjéken keresztül jut be a sejtekbe, vagy éppen gátolja azok működését. Például a diuretikumok a vesetubulusokban lévő iontranszportereket gátolják, növelve a vizeletürítést. A protonpumpa-gátlók (PPI-k) a gyomor H+/K+-ATPázát gátolják, csökkentve a savtermelést. A gyógyszer-transzporter interakciók megértése elengedhetetlen a gyógyszerek hatékonyságának és biztonságosságának optimalizálásához.
A multidrog rezisztencia (MDR) jelensége, különösen a rákterápiában, szorosan kapcsolódik az ABC transzporterekhez. A rákos sejtek gyakran fokozottan expresszálják az olyan transzportereket, mint a P-glikoprotein (ABCB1), amely képes kipumpálni a sejtből számos kemoterápiás szert, csökkentve ezzel a kezelés hatékonyságát. Ez komoly kihívást jelent a gyógyszerfejlesztésben.
Betegségek és genetikai rendellenességek
Számos súlyos betegség hátterében a szállító fehérjék genetikai mutációi vagy diszfunkciói állnak:
- Cisztás fibrózis: A legklasszikusabb példa. A CFTR (Cystic Fibrosis Transmembrane Conductance Regulator) gén mutációja okozza, amely egy kloridion csatorna és egyben ABC transzporter. A hibás CFTR fehérje elégtelen kloridtranszportot eredményez, ami sűrű, viszkózus váladék termelődéséhez vezet a tüdőben, hasnyálmirigyben és más szervekben.
- Csatornopátiák: Az ioncsatornák genetikai hibái számos betegséget okozhatnak, melyeket összefoglalóan csatornopátiáknak neveznek. Ide tartoznak bizonyos típusú epilepsziák (pl. feszültségfüggő Na+ csatorna mutációk), szívritmuszavarok (pl. K+ csatorna mutációk, hosszú QT-szindróma), izombetegségek (pl. periodikus paralízis) és neurológiai rendellenességek (pl. migrénes formák).
- Vesebetegségek: A vese tubulusaiban lévő transzporterek hibái specifikus rendellenességekhez vezethetnek. Például a Fanconi-szindróma a prokszimális tubulusok transzporterfehérjéinek széles körű diszfunkciója, ami aminosavak, glükóz és foszfát vizeletbe ürülését okozza. A renális glikozúria a glükóz transzporterek (SGLT) hibájából eredő glükózürítést jelenti a vizeletben, normális vércukorszint mellett.
- Metabolikus betegségek: A glükóz transzporterek, mint a GLUT1 és GLUT4, mutációi ritka, de súlyos metabolikus rendellenességeket okozhatnak, befolyásolva a glükóz felvételét az agyban vagy az izmokban.
- Malignus hipertermia: Ez egy súlyos, potenciálisan halálos genetikai betegség, amelyet a ryanodin receptor (egy Ca2+ csatorna a szarkoplazmatikus retikulumban) mutációja okoz. Bizonyos anesztetikumok hatására az izomsejtekben kontrollálatlan Ca2+ felszabadulás és izomkontrakció lép fel, ami hipertermia (testhőmérséklet emelkedés) és metabolikus zavarokhoz vezet.
Kutatási irányok és jövőbeli perspektívák
A szállító fehérjék kutatása az elmúlt évtizedekben robbanásszerűen fejlődött, és továbbra is az élvonalban van a molekuláris biológia, biokémia és gyógyszerfejlesztés területén. Az új technológiák és a mélyebb megértés új lehetőségeket nyit meg a betegségek kezelésében és a biológiai folyamatok manipulálásában.
Strukturális biológia
A szállító fehérjék térbeli szerkezetének felderítése kulcsfontosságú működésük megértéséhez és új gyógyszerek tervezéséhez. Az olyan technikák, mint a krioelektronmikroszkópia (Cryo-EM) és a röntgenkrisztallográfia, lehetővé tették számos komplex transzporter (pl. különböző ABC transzporterek, ioncsatornák, glükóz transzporterek) nagy felbontású szerkezetének meghatározását. Ez a strukturális információ felbecsülhetetlen értékű abban, hogy pontosan megértsük, hogyan kötik meg a szubsztrátokat, hogyan mennek keresztül konformációs változásokon, és hogyan szabályozódnak.
Gyógyszerfejlesztés
A szállító fehérjék kiváló gyógyszercélpontok. A jövőbeli gyógyszerfejlesztés egyik ígéretes iránya a specifikus transzporter gátlók vagy aktivátorok tervezése. Például az SGLT2 gátlók, amelyek a vesében lévő Na+/glükóz kotranszportert blokkolják, már alkalmazásra kerültek a 2-es típusú cukorbetegség kezelésében, segítve a glükóz vizelettel történő kiválasztását. Az ABC transzporterek gátlása a rákterápiában is ígéretes lehet a multidrog rezisztencia leküzdésére. Emellett a neurológiai és pszichiátriai betegségek kezelésére is fejlesztenek célzott ioncsatorna modulátorokat.
Génterápia
A genetikai rendellenességek, mint például a cisztás fibrózis, ahol egy hibás szállító fehérje (CFTR) a probléma gyökere, ideális célpontjai a génterápiának. A cél az, hogy a hibás gén másolása helyett a működőképes gént juttassák be a sejtekbe, helyreállítva ezzel a normális transzporter funkciót. Bár még számos kihívás áll a technológia előtt, a kutatások ígéretesek.
Precíziós orvoslás
A szállító fehérjék genetikai variációi befolyásolhatják az egyének válaszát a gyógyszerekre és a betegségekre való hajlamát. A precíziós orvoslás, amely az egyén genetikai profiljára szabott kezeléseket alkalmaz, egyre inkább figyelembe veszi a transzporter gének polimorfizmusait. Ez lehetővé teheti a gyógyszeradagok személyre szabását, a mellékhatások minimalizálását és a terápia hatékonyságának maximalizálását.
A szállító fehérjék megértése és manipulálása az egyik legizgalmasabb és legfontosabb terület a modern biológiában és orvostudományban. Az elkövetkező években várhatóan további áttörések születnek ezen a téren, amelyek alapvetően változtathatják meg a betegségek kezelésének módját és az emberi egészségről alkotott képünket.










