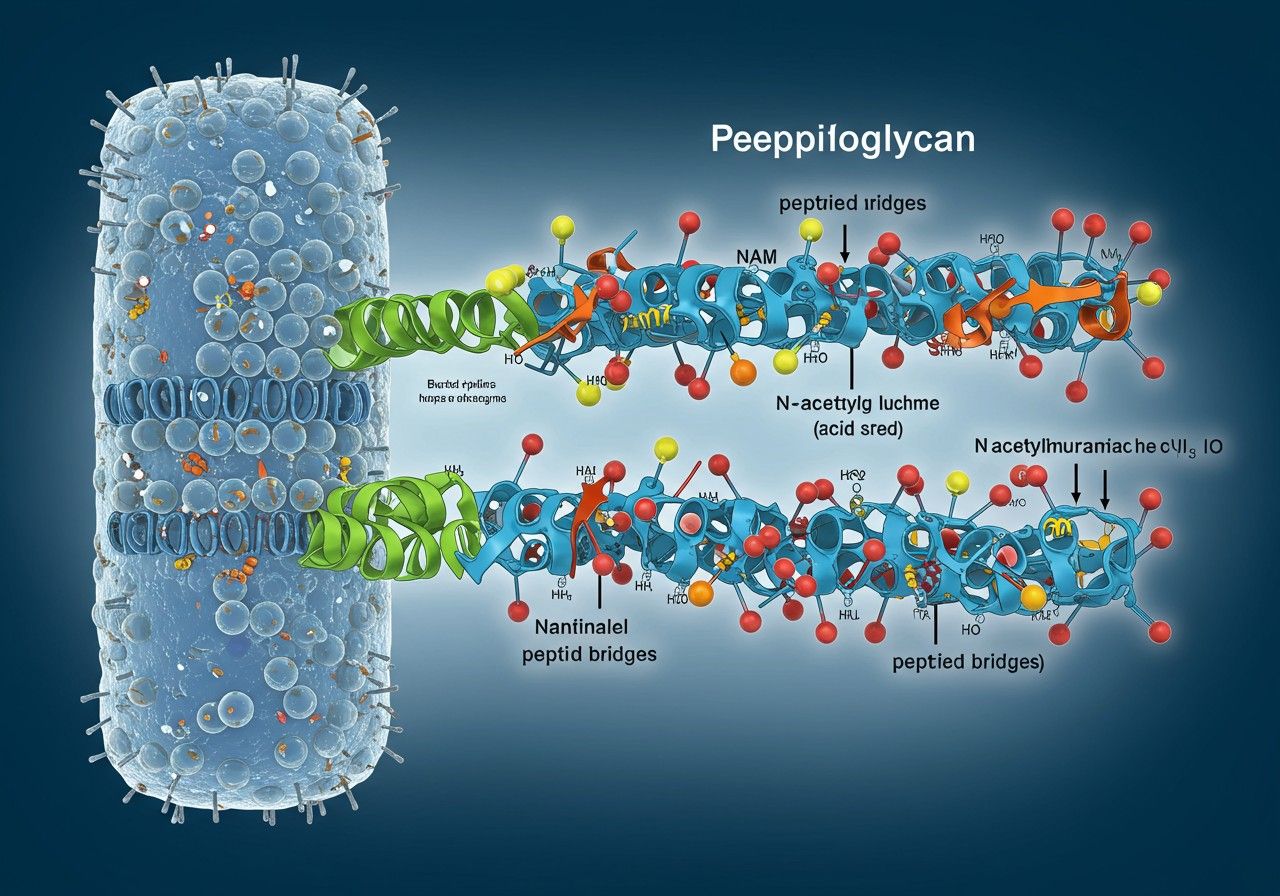
A peptidoglikán, más néven murein, egyedülálló és alapvető polimer, amely a legtöbb baktérium sejtfalának létfontosságú alkotóeleme. Ez a komplex makromolekula nem csupán egy merev váz, amely megadja a baktériumok jellegzetes formáját, hanem kritikus szerepet játszik a sejtek integritásának fenntartásában is, védelmet nyújtva az ozmotikus stressz ellen. Nélküle a baktériumok nem lennének képesek túlélni a változatos környezeti feltételeket, és szétesnének a belső turgornyomás hatására. A peptidoglikán szerkezete rendkívül konzervált az evolúció során, ami aláhúzza biológiai jelentőségét és nélkülözhetetlenségét a bakteriális élet számára.
A peptidoglikán egy hálózatos polimer, amely két fő komponensből épül fel: glikánláncokból és rövid peptidláncokból. Ezek a kétféle egység váltakozva ismétlődik, létrehozva egy erős, térhálós szerkezetet. A glikánláncok lineáris poliszacharidok, míg a peptidláncok ezeket a glikánláncokat kötik össze egymással, egyfajta molekuláris rácsot alkotva. Ez a különleges felépítés teszi lehetővé, hogy a baktériumok ellenálljanak a környezeti erőknek, és stabilan fenntartsák belső környezetüket. A szerkezet részletes megértése kulcsfontosságú ahhoz, hogy felfedezzük a baktériumok elleni küzdelem új stratégiáit, különösen az antibiotikum-rezisztencia korában.
A peptidoglikán alapvető szerkezete: a glikánlánc
A peptidoglikán szerkezetének alapját a lineáris glikánláncok adják, amelyek kétfajta módosított cukormolekula ismétlődéséből állnak. Ezek az egységek az N-acetilglükózamin (NAG) és az N-acetilmuraminsav (NAM). Ezek a diszacharid egységek egymással váltakozva, erős β-1,4-glikozidos kötésekkel kapcsolódnak, hosszú, fonalszerű polimereket képezve. Ez a kötésmód adja a glikánláncok gerincének stabilitását.
Az N-acetilglükózamin egy széles körben elterjedt aminoszármazék cukor, amely számos más biológiai polimerben is megtalálható, például a kitinben. Azonban az N-acetilmuraminsav egyedülálló a peptidoglikánra nézve. Ez a molekula az N-acetilglükózamin egy származéka, amely egy tejsavcsoportot (laktátot) tartalmaz éterkötésben a C3 szénatomhoz kapcsolódva. Ez a tejsavcsoport biztosítja azt a kapcsolódási pontot, amelyhez a peptidláncok rögzülnek, és ezáltal kulcsszerepet játszik a peptidoglikán térhálós szerkezetének kialakításában. A NAM jelenléte az egyik legfontosabb megkülönböztető jegye a bakteriális sejtfalnak, és egyben kiváló célpontot is jelent az antibiotikumok számára, mivel az eukarióta sejtekben nem fordul elő.
A glikánláncok hossza fajonként és növekedési fázisonként változhat, de általában több száz vagy akár több ezer diszacharid egységből állhatnak. A β-1,4-glikozidos kötések ellenállóak a legtöbb enzim hatásával szemben, kivéve a lizozimot, amely képes hidrolizálni ezeket a kötéseket, ezáltal károsítva a bakteriális sejtfalat. Ez a lizozim által biztosított védekező mechanizmus az immunrendszerünk egyik alapvető fegyvere a baktériumok ellen, megtalálható például a könnyben, nyálban és más testnedvekben.
A peptidkomponens: aminosavak és keresztkötések
A peptidoglikán erejét és rugalmasságát nemcsak a glikánláncok adják, hanem a hozzájuk kapcsolódó és azokat összekötő peptidláncok rendszere is. Minden N-acetilmuraminsav (NAM) egységhez egy rövid, általában négy aminosavból álló peptidlánc kapcsolódik kovalens kötéssel a tejsavcsoport karboxilcsoportjához. Ez a peptidlánc gyakran nevezett tetrapeptid, és összetétele bár némileg változhat a különböző baktériumfajok között, számos konzervált tulajdonsággal rendelkezik.
A tipikus peptidlánc a következő aminosavakat tartalmazza (N-terminálisról C-terminálisra haladva):
- Az első aminosav általában L-alanin.
- A második aminosav szinte mindig D-glutaminsav.
- A harmadik aminosav változatosabb lehet: Gram-pozitív baktériumokban gyakran L-lizin, míg Gram-negatív baktériumokban jellemzően mezo-diaminopimelinsav (DAP). Mindkét aminosav egy extra aminocsoportot tartalmaz, ami kulcsfontosságú a keresztkötések kialakításához.
- A negyedik aminosav általában D-alanin. Ez a D-alanin gyakran egy másik D-alaninnal van összekapcsolódva a prekurzor molekulákban (D-Ala-D-Ala dipeptid), de a végső keresztkötés során az egyik D-alanin lehasad.
A D-aminosavak jelenléte (D-glutaminsav, D-alanin) különösen figyelemre méltó, mivel az eukarióta fehérjék szinte kizárólag L-aminosavakból épülnek fel. Ez a különbség jelentős védelmet biztosít a bakteriális peptidoglikán számára, mivel a gazdaszervezet proteázai, amelyek az L-aminosavakat bontják, nem képesek hatékonyan lebontani a peptidoglikán peptidláncait. Ez a tényező is hozzájárul a bakteriális sejtfal stabilitásához és ellenállóképességéhez.
A keresztkötések mechanizmusa
A peptidoglikán térhálós szerkezetét a szomszédos glikánláncokhoz kapcsolódó peptidláncok közötti keresztkötések hozzák létre. Ezek a kötések kovalensek és rendkívül erősek, biztosítva a sejtfal mechanikai integritását. A keresztkötés kialakulásának mechanizmusa a transzpeptidáció nevű enzimreakció révén történik, amelyet penicillin-kötő fehérjék (PBP-k) katalizálnak.
A transzpeptidáció során az egyik peptidlánc negyedik aminosavának (D-alanin) karboxilcsoportja reakcióba lép egy szomszédos peptidlánc harmadik aminosavának (L-lizin vagy DAP) aminocsoportjával. Ez a reakció egy peptidkötést hoz létre, miközben a kiindulási peptidlánc ötödik D-alaninja lehasad. A keresztkötések lehetnek:
- Direkt keresztkötés: Jellemzően Gram-negatív baktériumokban fordul elő, ahol a DAP aminocsoportja közvetlenül kapcsolódik a D-alanin karboxilcsoportjához.
- Indirekt keresztkötés (interpeptid híd): Jellemzően Gram-pozitív baktériumokban található, ahol a harmadik aminosav (L-lizin) és a negyedik aminosav (D-alanin) között egy vagy több aminosavból álló „híd” (pl. pentaglicin híd a Staphylococcus aureus esetében) épül be. Ez a híd további rugalmasságot adhat a peptidoglikán szerkezetének.
A keresztkötések sűrűsége és típusa nagyban befolyásolja a peptidoglikán réteg merevségét és pórusméretét. A vastagabb és sűrűbben keresztkötött peptidoglikán réteg nagyobb mechanikai stabilitást biztosít, de lassabb anyagcserét tesz lehetővé, míg a lazább szerkezet rugalmasabb, de potenciálisan sérülékenyebb lehet.
A peptidoglikán a bakteriális sejtfal kulcsfontosságú alkotóeleme, melynek egyedi szerkezete, különösen a D-aminosavak és a speciális keresztkötések, nemcsak mechanikai stabilitást nyújtanak, hanem kiváló célpontot is jelentenek számos antibiotikum számára.
Különbségek Gram-pozitív és Gram-negatív baktériumok között
A bakteriális sejtek két nagy csoportra oszthatók a sejtfaluk szerkezeti különbségei alapján, amelyeket a Gram-festés során mutatott reakciójuk is tükröz. Ez a megkülönböztetés, amelyet Hans Christian Gram dán orvos fejlesztett ki a 19. században, alapvető fontosságú a mikrobiológiában, és mélyrehatóan kapcsolódik a peptidoglikán réteg felépítéséhez és elhelyezkedéséhez.
Gram-pozitív baktériumok
A Gram-pozitív baktériumok jellemzője egy rendkívül vastag peptidoglikán réteg, amely a sejtfaluk domináns alkotóeleme. Ez a réteg a teljes sejtfal 50-90%-át is kiteheti, vastagsága elérheti a 20-80 nanométert. A vastag peptidoglikán réteg számos rétegből áll, amelyek sűrűn keresztkötöttek, rendkívül erős és merev struktúrát biztosítva a sejt számára.
A peptidoglikánon kívül a Gram-pozitív sejtfalak további, egyedi komponenseket is tartalmaznak, mint például a teikolsavak és a lipoteikolsavak. A teikolsavak foszfátokkal polimerizált glicerol- vagy ribitol egységekből állnak, és kovalensen kapcsolódnak a peptidoglikánhoz. A lipoteikolsavak hasonlóak, de egy lipidrésszel is rendelkeznek, amely beágyazódik a citoplazma membránba, áthidalva a membránt és a peptidoglikán réteget. Ezek a savak számos fontos funkciót töltenek be:
- Hozzájárulnak a sejtfal integritásához és stabilitásához.
- Szerepet játszanak a kationok megkötésében és szállításában.
- Antigénként működnek, befolyásolva a gazdaszervezet immunválaszát.
- Segítik a baktériumok tapadását a gazdaszervezet sejtjeihez.
A Gram-pozitív baktériumoknak nincs külső membránjuk, a peptidoglikán réteg közvetlenül a citoplazma membrán felett helyezkedik el. Ez a szerkezet teszi lehetővé, hogy a Gram-festés során a kristályibolya-jód komplex a vastag peptidoglikán rétegben maradjon, és az alkoholos mosás után is megőrizze lila színét.
Gram-negatív baktériumok
Ezzel szemben a Gram-negatív baktériumok sejtfala sokkal komplexebb, és jelentősen eltérő szerkezetet mutat. A peptidoglikán rétegük sokkal vékonyabb, mindössze 2-7 nanométer vastagságú, és gyakran csak egy vagy néhány rétegből áll. Ez a vékony peptidoglikán réteg a periplazmatikus térben található, amely a belső citoplazma membrán és a külső membrán között helyezkedik el.
A külső membrán a Gram-negatív baktériumok sejtfalának egyik legjellegzetesebb és legfontosabb alkotóeleme. Ez a membrán aszimmetrikus, belső felén foszfolipideket, külső felén pedig lipopoliszacharidokat (LPS) tartalmaz. Az LPS, más néven endotoxin, egy erős immunválaszt kiváltó molekula, amely a baktériumok patogenitásában is szerepet játszik. Az LPS három fő részből áll:
- Lipid A: A membránba ágyazott lipidrész, amely a toxikus hatásokért felelős.
- Magpoliszacharid: Egy rövid, konzervált cukorlánc.
- O-specifikus lánc (O-antigén): Egy változatos, hosszú poliszacharid lánc, amely a baktériumfajok közötti különbségeket jelöli, és fontos az immunrendszer felismerésében.
A külső membrán átjárhatóságát porin fehérjék szabályozzák, amelyek csatornákat képeznek, lehetővé téve a kis molekulák bejutását, de gátolva a nagyobb molekulák, például egyes antibiotikumok bejutását. Ez a tényező hozzájárul a Gram-negatív baktériumok természetes antibiotikum-rezisztenciájához.
A periplazmatikus térben, a vékony peptidoglikán réteg körül, számos enzim (pl. béta-laktamázok, amelyek lebontják az antibiotikumokat), transzportfehérjék és más faktorok találhatók, amelyek fontosak a baktériumok anyagcseréjében és túlélésében. A Gram-negatív baktériumok nem tartják meg a kristályibolya-jód komplexet az alkoholos mosás után, mivel a külső membrán és a vékony peptidoglikán réteg nem képes visszatartani azt, ezért a szafraninnal rózsaszínre vagy pirosra festődnek.
| Jellemző | Gram-pozitív baktériumok | Gram-negatív baktériumok |
|---|---|---|
| Peptidoglikán réteg vastagsága | Vastag (20-80 nm, többrétegű) | Vékony (2-7 nm, egy-két réteg) |
| Elhelyezkedés | Közvetlenül a citoplazma membrán felett | Periplazmatikus térben, a külső és belső membrán között |
| Külső membrán | Nincs | Van, lipopoliszacharidokkal (LPS) |
| További komponensek | Teikolsavak, lipoteikolsavak | LPS, porinok, lipoprotein (Braun-lipoprotein) |
| Gram-festés eredménye | Lila | Rózsaszín/Piros |
| Antibiotikum érzékenység | Általában érzékenyebb (pl. penicillinre) | Gyakran ellenállóbb (külső membrán, efflux pumpák) |
Ezek a szerkezeti különbségek alapvetően befolyásolják a baktériumok fiziológiáját, patogenitását és az antibiotikumokkal szembeni érzékenységét, ami kritikus fontosságú a klinikai diagnosztikában és terápiában.
A peptidoglikán bioszintézise: lépésről lépésre
A peptidoglikán szintézise egy rendkívül komplex és energiaigényes folyamat, amely több lépésben, különböző celluláris kompartmentekben zajlik. Ez a folyamat nélkülözhetetlen a baktériumok növekedéséhez és szaporodásához, és éppen ezért kiváló célpontot jelent számos antibiotikum számára. A szintézis három fő fázisra osztható: citoplazmatikus, membránhoz kötött és extracelluláris fázis.
1. Citoplazmatikus fázis
Ez a fázis a baktérium citoplazmájában zajlik, és magában foglalja a peptidoglikán építőköveinek, a prekurzor molekuláknak az előállítását. A főbb lépések:
- UDP-NAG szintézise: Glükóz-6-foszfátból kiindulva, több enzimreakció során N-acetilglükózamin-1-foszfát (NAG-1-P) képződik. Ezután az N-acetilglükózamin-1-foszfát UDP-vel (uridindifoszfát) reagál, létrehozva az UDP-N-acetilglükózamint (UDP-NAG).
- UDP-NAM-pentapeptid szintézise: Az UDP-NAG-ból speciális enzimek (pl. MurA, MurB) segítségével UDP-N-acetilmuraminsav (UDP-NAM) képződik. Ezt követően a NAM-hoz egyenként kapcsolódnak az aminosavak, létrehozva a teljes UDP-NAM-pentapeptidet. Az aminosavak kapcsolódása ATP-függő folyamat, és specifikus ligáz enzimek végzik (pl. MurC, MurD, MurE, MurF). Fontos megjegyezni, hogy az utolsó lépésben két D-alanin molekula kapcsolódik egymáshoz, majd ez a D-Ala-D-Ala dipeptid kapcsolódik a tetrapeptidhez, így alakul ki a pentapeptid.
Ezek a citoplazmatikus prekurzorok a membránhoz kötött fázisban kerülnek felhasználásra.
2. Membránhoz kötött fázis
Ebben a fázisban a citoplazmában szintetizált prekurzorok a citoplazma membránhoz transzferálódnak, és további módosításokon esnek át. A kulcsszereplő egy lipid vivőmolekula, a bactoprenol-foszfát (más néven undekaprenil-foszfát).
- Transzfer a bactoprenolra: Az UDP-NAM-pentapeptid N-acetilmuraminsav-pentapeptid része átkerül a bactoprenol-foszfátra, létrehozva a bactoprenol-PP-NAM-pentapeptidet. Ezt a reakciót a MraY enzim katalizálja.
- NAG hozzáadása: Ezt követően az UDP-NAG N-acetilglükózamin része is átkerül a bactoprenol-PP-NAM-pentapeptidhez, létrehozva a teljes diszacharid-pentapeptid egységet, a bactoprenol-PP-NAG-NAM-pentapeptidet. Ezt a reakciót a MurG enzim katalizálja.
- Interpeptid híd kialakítása (Gram-pozitívoknál): Amennyiben a baktérium interpeptid hidat használ (pl. pentaglicin híd), az aminosavak hozzáadása is a bactoprenolhoz kötött prekurzorhoz történik ebben a fázisban, specifikus enzimek segítségével.
- Transzlokáció: A teljes bactoprenolhoz kötött diszacharid-pentapeptid egység átkerül a citoplazma membrán külső oldalára, a periplazmatikus térbe (Gram-negatívoknál) vagy a sejtfal külső felületére (Gram-pozitívoknál).
3. Extracelluláris fázis (Transzpeptidáció és Transzglikoziláció)
Ez a fázis a citoplazma membrán külső felületén vagy a periplazmatikus térben zajlik, és magában foglalja az új diszacharid-pentapeptid egységek beépítését a növekvő peptidoglikán rétegbe.
- Transzglikoziláció: A transzglikoziláz enzimek (amelyek szintén PBP-khez tartozhatnak) katalizálják az új diszacharid egység glikozidos kötésének létrehozását egy meglévő glikánlánc végéhez. Ezáltal a glikánláncok meghosszabbodnak.
- Transzpeptidáció: Ezzel párhuzamosan a transzpeptidáz enzimek (a legfontosabb PBP-k) létrehozzák a keresztkötéseket a szomszédos peptidláncok között. Mint korábban említettük, ez a reakció a D-Ala-D-Ala dipeptid lehasadásával jár, és új peptidkötést hoz létre az egyik peptidlánc D-alaninja és a másik peptidlánc harmadik aminosava (L-lizin vagy DAP) között.
- Bactoprenol-foszfát regenerációja: A diszacharid-pentapeptid egység átadása után a bactoprenol-difoszfát marad vissza. Ezt a difoszfátot egy foszfatáz enzim de-foszforilálja, visszaállítva a bactoprenol-foszfátot, amely újra felhasználható a szintézis következő ciklusában. Ennek a regenerációnak a gátlása súlyosan befolyásolja a peptidoglikán szintézisét.
A penicillin-kötő fehérjék (PBP-k) kulcsfontosságúak az extracelluláris fázisban, mivel ők végzik a transzglikoziláz és transzpeptidáz aktivitásokat. Ezek az enzimek a sejtfal növekedésének és átalakításának fő motorjai, és éppen ezért ők az elsődleges célpontjai a béta-laktám antibiotikumoknak.
A peptidoglikán szintézisének precíz koordinációja biztosítja, hogy a sejt növekedése és osztódása során a sejtfal integritása folyamatosan fenntartható legyen. Bármilyen zavar ebben a komplex folyamatban végzetes lehet a baktériumra nézve, ami magyarázza, miért olyan hatékonyak a peptidoglikán szintézist gátló antibiotikumok.
A peptidoglikán funkciói: stabilitás és védelem
A peptidoglikán nem csupán egy passzív szerkezeti elem, hanem aktívan hozzájárul a baktériumok túléléséhez és virulenciájához. Funkciói messze túlmutatnak a puszta mechanikai támogatáson, alapvető fontosságúak a sejtélet minden aspektusában.
Mechanikai stabilitás és ozmotikus védelem
A peptidoglikán legfontosabb és legnyilvánvalóbb funkciója a mechanikai stabilitás biztosítása. Ez a merev, hálózatos polimer adja a baktériumsejt jellegzetes formáját (pl. gömb alakú kokkusz, pálcika alakú bacillus, spirális spirillum). A sejtfal merevsége ellenáll a külső fizikai erőknek, és megakadályozza a sejt deformálódását vagy szétesését.
Ennél is kritikusabb az ozmotikus stressz elleni védelem. A baktériumok citoplazmája általában sokkal magasabb koncentrációjú oldott anyagokat tartalmaz, mint a környezetük. Ez a koncentrációkülönbség egy jelentős ozmotikus nyomást hoz létre, amely folyamatosan vizet próbál beáramoltatni a sejtbe. Egy membránnal körülvett sejt, amelynek nincs erős sejtfala (pl. az állati sejtek), ilyen körülmények között gyorsan megduzzadna és szétpukkanna (lízingálódna). A peptidoglikán sejtfal egy erős, rugalmatlan burkot képez, amely ellenáll ennek a belső turgornyomásnak, és megakadályozza a sejt szétrepedését. Ez a képesség teszi lehetővé a baktériumok számára, hogy széles körű környezeti feltételek között, akár híg oldatokban is túléljenek.
Sejtosztódás és septum képzés
A baktériumok bináris hasadással szaporodnak, ami azt jelenti, hogy egy anyasejt két azonos leánysejtre osztódik. Ehhez a folyamathoz elengedhetetlen a sejtfal pontos és szabályozott növekedése és osztódása. A peptidoglikán kulcsszerepet játszik a septum (válaszfal) képzésében, amely elválasztja a két leánysejtet. Az osztódás során a peptidoglikán hidrolázok (autolizinek) helyi bontást végeznek a sejtfalban, lehetővé téve az új peptidoglikán szintézisét a septum területén. Ez a precízen szabályozott bontás és szintézis biztosítja, hogy a leánysejtek megfelelően elkülönüljenek, és mindegyikük teljes, funkcionális sejtfalral rendelkezzen.
Immunitás elkerülése és virulencia faktor
Bár a peptidoglikán, mint PAMP (Pathogen-Associated Molecular Pattern), aktiválja a gazdaszervezet immunrendszerét, bizonyos mértékig szerepet játszhat az immunitás elkerülésében is. A vastag és sűrűn keresztkötött peptidoglikán réteg fizikai akadályt képezhet az immunsejtek és molekulák számára, gátolva azok hozzáférését a citoplazma membránhoz vagy más bakteriális komponensekhez.
Egyes baktériumok esetében a peptidoglikán, vagy annak egyes részei, közvetlenül hozzájárulhatnak a virulenciához. Például a peptidoglikán fragmentumok gyulladásos választ válthatnak ki, ami a gazdaszervezet károsodásához vezethet. Ezenkívül a peptidoglikán szerkezetének módosításai befolyásolhatják a baktériumok tapadását a gazdaszervezet sejtjeihez, vagy védelmet nyújthatnak az antimikrobiális peptidekkel szemben. A Mycobacterium tuberculosis például egy rendkívül komplex, viaszos sejtfalréteggel rendelkezik, amely a peptidoglikánon alapul, és hozzájárul a baktérium ellenállóképességéhez a gazdaszervezet immunválaszával és az antibiotikumokkal szemben.
Sejtforma fenntartása és motilitás
A peptidoglikán nemcsak a sejt általános alakját határozza meg, hanem a sejtforma fenntartásában is kulcsszerepet játszik a növekedés és osztódás során. A speciális peptidoglikán-szintetizáló és -modifikáló enzimek (pl. MreB, RodA) irányítják az új peptidoglikán egységek beépülését, biztosítva a henger alakú baktériumok (bacillusok) elongációját anélkül, hogy elveszítenék formájukat. A kokkuszok (gömb alakú baktériumok) esetében a peptidoglikán növekedése egyenletesen zajlik a sejt teljes felületén.
Bár a peptidoglikán alapvetően merev szerkezet, bizonyos baktériumok, mint például a spirochéták (pl. a Lyme-kórt okozó Borrelia burgdorferi), a periplazmatikus térben elhelyezkedő flagellumok (endoflagellumok) segítségével mozognak. Ezek a flagellumok a sejtfal és a külső membrán között helyezkednek el, és a peptidoglikán réteghez rögzülnek. A flagellumok forgása a peptidoglikán réteggel kölcsönhatásban hozza létre a jellegzetes csavaró, fúró mozgást, amely lehetővé teszi számukra, hogy viszkózus közegekben, például szövetekben is hatékonyan haladjanak.
Összességében a peptidoglikán funkciói túlmutatnak egy egyszerű vázszerkezeten. Ez a molekula a bakteriális élet alapköve, amely biztosítja a sejtek integritását, növekedését, osztódását, és gyakran még a patogenitásukhoz is hozzájárul. Éppen ezért a peptidoglikán szintézisének vagy szerkezetének megzavarása az egyik leghatékonyabb stratégia a bakteriális fertőzések elleni küzdelemben.
A peptidoglikán, mint gyógyszercélpont: az antibiotikumok harca
A peptidoglikán egyedisége és nélkülözhetetlensége a baktériumok számára kiváló célponttá teszi az antibiotikumok széles skálája számára. Mivel ez a molekula az eukarióta sejtekben nem fordul elő, az azt célzó gyógyszerek szelektíven toxikusak a baktériumokra, minimális mellékhatással a gazdaszervezetre. Az antibiotikumok, amelyek a peptidoglikán szintézisét vagy integritását támadják, a leghatékonyabb és leggyakrabban használt antimikrobiális szerek közé tartoznak.
Béta-laktám antibiotikumok
A béta-laktám antibiotikumok, mint a penicillinek, cefalosporinok, karbapenemek és monobaktámok, a legszélesebb körben alkalmazott antibiotikumcsalád. Nevüket a kémiai szerkezetükben található jellegzetes béta-laktám gyűrűről kapták. Hatásmechanizmusuk a peptidoglikán szintézis extracelluláris fázisának gátlásán alapul.
A béta-laktámok a bakteriális sejtfal szintézisében kulcsszerepet játszó penicillin-kötő fehérjékhez (PBP-k) kötődnek. Mint korábban említettük, a PBP-k transzpeptidáz és transzglikoziláz aktivitással rendelkeznek, amelyek a peptidoglikán keresztkötéseinek kialakításáért és a glikánláncok meghosszabbításáért felelősek. A béta-laktámok szerkezete rendkívül hasonló a D-Ala-D-Ala dipeptidhez, amelyet a PBP-k normális szubsztrátként ismernek fel. Az antibiotikumok azonban irreverzibilisen kötődnek a PBP-k aktív helyéhez, gátolva azok működését. Ez a gátlás megakadályozza a peptidoglikán réteg megfelelő keresztkötését, ami gyenge, instabil sejtfalat eredményez. Az instabil sejtfalú baktériumok nem képesek ellenállni az ozmotikus nyomásnak, és szétesnek (lízingálódnak).
A béta-laktámok baktericid (baktériumölő) hatásúak, és a legtöbb Gram-pozitív és számos Gram-negatív baktérium ellen hatékonyak. Azonban a béta-laktamáz enzimek termelése, amelyek képesek lebontani a béta-laktám gyűrűt, az egyik legelterjedtebb rezisztencia mechanizmus ellenük.
Glikopeptid antibiotikumok
A glikopeptid antibiotikumok, mint például a vancomycin és a teicoplanin, szintén a peptidoglikán szintézist célozzák, de eltérő mechanizmussal. Ezek az antibiotikumok nagy, komplex molekulák, amelyek közvetlenül a peptidoglikán prekurzorokhoz, pontosabban a D-Ala-D-Ala terminálishoz kötődnek a citoplazma membrán külső felületén.
A vancomycin kötődése fizikai akadályt képez, megakadályozva a transzpeptidáz enzimek (PBP-k) hozzáférését a szubsztráthoz. Ezáltal gátolja a keresztkötések kialakulását, és másodlagosan a transzglikozilációt is. A végeredmény hasonló a béta-laktámok hatásához: gyenge, instabil sejtfal, amely lízishez vezet. A vancomycint elsősorban multirezisztens Gram-pozitív baktériumok, például MRSA (Meticillin-rezisztens Staphylococcus aureus) fertőzései ellen alkalmazzák, amikor a béta-laktámok már hatástalanok.
Bacitracin
A bacitracin egy másik antibiotikum, amely a peptidoglikán szintézis membránhoz kötött fázisát gátolja. Specifikusan megakadályozza a bactoprenol-difoszfát de-foszforilációját bactoprenol-foszfáttá. Ez a lépés elengedhetetlen a bactoprenol-foszfát regenerációjához és újrahasznosításához, amely a peptidoglikán prekurzorok membránon keresztüli transzportjához szükséges. A bactoprenol-foszfát hiányában a peptidoglikán építőkövei nem jutnak ki a citoplazmából a sejtfal szintézis helyére, így a sejtfal növekedése leáll. A bacitracint gyakran lokálisan alkalmazzák, például bőrfertőzések kezelésére, mivel szisztémásan toxikus lehet a vesére.
Foszfomicin
A foszfomicin egy széles spektrumú antibiotikum, amely a peptidoglikán szintézis citoplazmatikus fázisát gátolja. Célpontja a MurA enzim, amely az első lépést katalizálja az UDP-NAG-ból UDP-NAM-pentapeptid szintézisében. A foszfomicin irreverzibilisen gátolja a MurA enzimet, megakadályozva a N-acetilmuraminsav prekurzor kialakulását. Ennek eredményeként a baktérium nem tudja előállítani a peptidoglikán építőköveit, és a sejtfal szintézise leáll. A foszfomicint gyakran alkalmazzák húgyúti fertőzések kezelésére.
Cikloszerin
A cikloszerin egy szerkezeti analógja a D-alaninnak, és a peptidoglikán szintézis citoplazmatikus fázisában hat. Gátolja a D-Ala-D-Ala ligáz enzimet, amely a két D-alanin molekula összekapcsolásáért felelős, valamint a alanin racémáz enzimet, amely az L-alanint D-alaninná alakítja. Ezen enzimek gátlásával a cikloszerin megakadályozza a D-Ala-D-Ala dipeptid képződését, amely elengedhetetlen a peptidoglikán pentapeptid prekurzorának kialakításához. A cikloszerint főként másodvonalbeli gyógyszerként alkalmazzák multirezisztens tuberkulózis (MDR-TB) kezelésére.
A peptidoglikán szintézisének gátlása a bakteriális fertőzések elleni küzdelem egyik legsikeresebb stratégiája. Az antibiotikumok, mint a béta-laktámok vagy a vancomycin, specifikusan ezen egyedi bakteriális struktúrát célozzák, minimalizálva a gazdaszervezetre gyakorolt káros hatásokat.
Az antibiotikumok ezen széles választéka, amelyek a peptidoglikán különböző szintézisfázisait támadják, aláhúzza ennek a molekulának a kritikus fontosságát a bakteriális életben. Azonban az antibiotikum-rezisztencia terjedése folyamatosan új kihívásokat jelent, és új gyógyszerek fejlesztését teszi szükségessé, amelyek képesek felülmúlni a baktériumok védekező mechanizmusait.
Antibiotikum rezisztencia mechanizmusai
Az antibiotikum-rezisztencia az egyik legsúlyosabb globális közegészségügyi probléma. A baktériumok rendkívüli alkalmazkodóképességük révén képesek ellenállóvá válni az antibiotikumokkal szemben, ami megnehezíti a fertőzések kezelését és növeli a morbiditást és mortalitást. A peptidoglikán-célzó antibiotikumokkal szembeni rezisztencia kialakulása számos mechanizmuson keresztül történhet.
1. Célpont módosítása
Ez a mechanizmus akkor fordul elő, amikor a baktérium módosítja az antibiotikum célpontját, így az már nem képes hatékonyan kötődni. A peptidoglikán szintézist gátló antibiotikumok esetében ez gyakran a penicillin-kötő fehérjék (PBP-k) módosítását jelenti.
- PBP-k szerkezeti változásai: A metillin-rezisztens Staphylococcus aureus (MRSA) a legismertebb példa erre. Az MRSA egy speciális PBP-t (PBP2a vagy PBP2′) termel, amelyet a mecA gén kódol. Ez a módosított PBP alacsony affinitással rendelkezik a béta-laktám antibiotikumokhoz, így a baktérium képes folytatni a sejtfal szintézisét még az antibiotikum jelenlétében is.
- D-Ala-D-Ala terminális módosítása: A vancomycin-rezisztens enterococcusok (VRE) és a vancomycin-rezisztens Staphylococcus aureus (VRSA) a peptidoglikán prekurzor terminálisának módosításával válnak rezisztenssé. A D-Ala-D-Ala dipeptid helyett a baktériumok D-Ala-D-Lac (D-laktát) vagy D-Ala-D-Ser (D-szerin) terminálist szintetizálnak. Mivel a vancomycin sokkal gyengébben kötődik ezekhez a módosított terminálisokhoz, elveszíti hatékonyságát. Ezt a változást a vanA, vanB, stb. gének kódolják.
2. Enzimális inaktiváció
Ez a mechanizmus magában foglalja az antibiotikum lebontását vagy inaktiválását a baktérium által termelt enzimek segítségével. A béta-laktám antibiotikumok esetében ez a leggyakoribb rezisztencia mechanizmus.
- Béta-laktamázok termelése: A béta-laktamázok olyan enzimek, amelyek hidrolizálják a béta-laktám gyűrűt, inaktiválva az antibiotikumot. Számos különböző típusú béta-laktamáz létezik, amelyek különböző béta-laktám antibiotikumok ellen hatékonyak (pl. penicillinázok, széles spektrumú béta-laktamázok (ESBL), karbapenemázok). Ezek az enzimek lehetnek kromoszomálisak vagy plazmidon kódoltak, ami lehetővé teszi a rezisztencia gének horizontális géntranszferrel történő gyors terjedését a baktériumok között.
3. Csökkent permeabilitás
Ez a mechanizmus elsősorban Gram-negatív baktériumokra jellemző, és magában foglalja az antibiotikum bejutásának gátlását a sejtbe.
- Porinok módosulása vagy hiánya: A Gram-negatív baktériumok külső membránján lévő porinok olyan csatornákat képeznek, amelyeken keresztül a hidrofil antibiotikumok, mint például a béta-laktámok, bejutnak a periplazmatikus térbe. A porinok szerkezetének módosulása vagy azok termelődésének csökkenése csökkentheti az antibiotikumok bejutását, ezzel rezisztenciát eredményezve.
4. Efflux pumpák
Az efflux pumpák olyan membránfehérjék, amelyek aktívan pumpálják ki az antibiotikumokat a sejtből, mielőtt azok elérhetnék a célpontjukat és kifejthetnék hatásukat. Ezek a pumpák széles spektrumúak lehetnek, és több különböző típusú antibiotikumot is képesek eltávolítani. Bár nem specifikusan a peptidoglikán-célzó antibiotikumokhoz kapcsolódnak, hozzájárulhatnak a Gram-negatív baktériumok általános rezisztenciájához.
5. Alternatív útvonalak vagy túlzott termelés
Ritkábban, de előfordulhat, hogy a baktériumok alternatív metabolikus útvonalakat fejlesztenek ki, amelyek megkerülik az antibiotikum által gátolt lépést, vagy túlzott mennyiségben termelik a célenzimet, így az antibiotikum nem tudja az összeset gátolni. Például a peptidoglikán prekurzorok túlzott termelése elméletileg „telítheti” az antibiotikumot, csökkentve annak hatékonyságát.
Az antibiotikum-rezisztencia mechanizmusainak megértése elengedhetetlen az új gyógyszerek és terápiás stratégiák fejlesztéséhez. A rezisztencia elleni küzdelem magában foglalja az antibiotikumok felelősségteljes használatát, az új antibiotikumok felfedezését, valamint a rezisztencia terjedésének monitorozását és megelőzését.
Az immunrendszer válasza a peptidoglikánra
Az immunrendszerünk kifinomult mechanizmusokkal rendelkezik a patogének felismerésére és eliminálására. A baktériumok esetében a peptidoglikán kulcsfontosságú molekula, amelyet a gazdaszervezet immunrendszere képes felismerni, és amely ennek következtében immunválaszt vált ki. A peptidoglikán egy tipikus PAMP (Pathogen-Associated Molecular Pattern), azaz patogénhez kapcsolódó molekuláris minta, amely nem fordul elő a gazdaszervezet sejtjeiben, így könnyen megkülönböztethető „saját”-tól és „idegen”-től.
PAMP-ok és PRR-ek
Az immunrendszer sejtjei speciális receptorokkal rendelkeznek, amelyeket PRR-eknek (Pattern Recognition Receptors) neveznek. Ezek a receptorok képesek felismerni a PAMP-okat. A peptidoglikán felismerésében számos PRR játszik szerepet:
- NOD-szerű receptorok (NLR-ek): Ezek intracelluláris receptorok, amelyek a citoplazmában találhatóak. A NOD1 és NOD2 receptorok specifikusan felismerik a peptidoglikán lebontási termékeit.
- NOD1 a diaminopimelinsav (DAP) tartalmú peptidoglikán fragmentumokat ismeri fel, amelyek jellemzően Gram-negatív baktériumokból származnak.
- NOD2 a muramil-dipeptidet (MDP) ismeri fel, amely mind Gram-pozitív, mind Gram-negatív baktériumok peptidoglikánjában megtalálható.
A NOD receptorok aktiválódása intracelluláris jelátviteli útvonalakat indít el, amelyek gyulladásos citokinek (pl. TNF-alfa, IL-6) és kemokinek termelődéséhez vezetnek, elősegítve a gyulladásos választ és az immunsejtek toborzását a fertőzés helyére.
- Toll-szerű receptorok (TLR-ek): Ezek membránkötött receptorok, amelyek a sejt felszínén vagy az endoszómák membránján találhatók.
- TLR2 a peptidoglikán és a lipoteikolsav (LTA) felismerésében játszik kulcsszerepet, különösen a Gram-pozitív baktériumok esetében. A TLR2 gyakran heterodimereket képez más TLR-ekkel (pl. TLR1, TLR6), hogy specifikusan felismerje a különböző peptidoglikán-szerkezeteket.
A TLR2 aktiválódása szintén gyulladásos citokinek és antimikrobiális peptidek termelődéséhez vezet, amelyek hozzájárulnak a bakteriális fertőzés leküzdéséhez.
Citokin termelés és gyulladásos válasz
A peptidoglikán PRR-ek általi felismerése egy erőteljes gyulladásos válaszhoz vezet. Ennek során az immunsejtek, mint a makrofágok, dendritikus sejtek és neutrofilek, aktiválódnak, és gyulladásos mediátorokat, például citokineket (pl. IL-1β, IL-6, TNF-α) és kemokineket bocsátanak ki. Ezek a molekulák elősegítik a gyulladás klasszikus tüneteit (vörösség, melegség, duzzanat, fájdalom), és kulcsszerepet játszanak az immunsejtek toborzásában és a fertőzés helyére irányításában.
A gyulladásos válasz célja a patogén lokalizálása és eliminálása, de túlzott mértékben károsíthatja a gazdaszervezet szöveteit is. A peptidoglikán, különösen a Gram-negatív baktériumok LPS-ével együtt, kiválthatja a szeptikus sokkot, egy életveszélyes állapotot, amelyet a szisztémás gyulladásos válasz szindróma (SIRS) jellemez.
Lizozim: a peptidoglikán hidrolitikus bontása
Az immunrendszer egyik közvetlen fegyvere a peptidoglikán ellen a lizozim. Ez az enzim széles körben elterjedt a testnedvekben (könny, nyál, orrváladék, vér, fagociták lizoszómái), és képes hidrolizálni a peptidoglikán glikánláncait. A lizozim specifikusan a β-1,4-glikozidos kötéseket bontja az N-acetilmuraminsav és az N-acetilglükózamin között. Ez a bontás gyengíti a sejtfalat, ami a baktérium ozmotikus líziséhez vezet, különösen Gram-pozitív baktériumok esetében, amelyek vastag, közvetlenül hozzáférhető peptidoglikán réteggel rendelkeznek.
Opsonizáció és fagocitózis
Bár nem közvetlenül a peptidoglikánhoz kapcsolódik, az immunrendszer a baktériumokat, beleértve a peptidoglikánnal rendelkezőket is, opsonizáció révén is eliminálja. Az opsoninok, mint az antitestek és a komplementrendszer fehérjéi, bevonják a baktériumok felszínét, megjelölve azokat a fagociták (pl. makrofágok, neutrofilek) számára. A fagociták receptorai felismerik az opsoninokat, és bekebelezik (fagocitálják) a baktériumokat, majd intracellulárisan lebontják azokat. A peptidoglikán fragmentumok, amelyek a fagocitózis során keletkeznek, tovább aktiválhatják a NOD-receptorokat a fagociták belsejében.
A peptidoglikán tehát nemcsak a baktériumok túléléséért felelős, hanem az immunrendszer számára is egy kulcsfontosságú „riasztó jel”, amely elindítja a védekező mechanizmusok sorát. Ezen kölcsönhatások megértése alapvető a fertőző betegségek patogenezisének és az immunterápiás stratégiák fejlesztésének szempontjából.
A peptidoglikán szerepe a biotechnológiában és az iparban
A peptidoglikán, mint egyedi bakteriális polimer, nem csupán a mikrobiológia és a gyógyászat érdeklődését kelti fel, hanem számos potenciális alkalmazási lehetőséget kínál a biotechnológiában és az iparban is. Egyedülálló szerkezete és biológiai aktivitása miatt egyre inkább a kutatások fókuszába kerül.
Vakcinafejlesztés: adjuvánsok és immunmodulátorok
A peptidoglikán fragmentumok, különösen a muramil-dipeptid (MDP), régóta ismertek immunmoduláló tulajdonságaikról. Képesek stimulálni a veleszületett immunrendszert, különösen a NOD2 receptorokon keresztül. Ez a tulajdonság teszi őket potenciális adjuvánsokká a vakcinafejlesztésben.
- Az adjuvánsok olyan anyagok, amelyeket vakcinákhoz adnak, hogy fokozzák az immunválaszt az antigénre, és javítsák a vakcina hatékonyságát. Az MDP és szintetikus analógjai, mint például a muramil-tripeptid (MTP-PE), már klinikailag is vizsgáltak adjuvánsként rákvakcinákban és más betegségek elleni vakcinákban.
- Az immunrendszer stimulálásával az peptidoglikán-származékok segíthetnek erősebb és tartósabb immunitás kialakításában az antigénekkel szemben, csökkentve az adagolási igényt és növelve a vakcinák védőhatását.
Diagnosztika: bakteriális fertőzések kimutatása
Mivel a peptidoglikán specifikus a baktériumokra, lebontási termékei vagy specifikus antigénjei felhasználhatók a bakteriális fertőzések diagnosztizálására.
- Például a muramil-dipeptid (MDP) kimutatása a vérben vagy más testnedvekben jelezheti a bakteriális fertőzés jelenlétét, különösen abban az esetben, ha a hagyományos tenyésztés nehézkes vagy lassú.
- A peptidoglikán-specifikus antitestek vagy antigének kimutatására szolgáló immunoassay módszerek segíthetnek a gyors és pontos diagnózis felállításában, ami kulcsfontosságú a korai és célzott kezelés megkezdéséhez.
Probiotikumok kutatása és a bélflóra modulációja
A bélflóra (mikrobiom) egészségünk alapja, és a benne élő baktériumok peptidoglikánja folyamatosan kölcsönhatásba lép a bélnyálkahártya immunrendszerével.
- A probiotikumok, amelyek jótékony baktériumokat tartalmaznak, szintén termelnek peptidoglikánt. Ennek a peptidoglikánnak a szerkezete és a gazdaszervezettel való interakciója befolyásolhatja a bél immunrendszerét, elősegítve a homeosztázist vagy modulálva a gyulladásos válaszokat.
- A kutatók vizsgálják, hogyan befolyásolják a különböző probiotikus törzsek peptidoglikánjai a bélrendszer immunitását, és hogyan lehet ezeket az ismereteket felhasználni a bélbetegségek, allergiák vagy autoimmun állapotok kezelésében.
- A peptidoglikán fragmentumok szerepe a bélflóra-gazdaszervezet keresztbeszélgetésben egyre inkább előtérbe kerül, mint a mikrobiom-alapú terápiák lehetséges célpontja.
Anyagtudomány és biokompatibilis anyagok fejlesztése
A peptidoglikán egyedülálló biopolimer, amely inspirációt adhat az anyagtudományban.
- Kutatások folynak a peptidoglikán vagy annak szintetikus analógjainak felhasználására biokompatibilis anyagok, például implantátumok vagy szövetmérnöki mátrixok fejlesztésében.
- A peptidoglikán merev, de porózus szerkezete alkalmassá teheti például szűrőanyagok, bioszenzorok vagy gyógyszerhordozó rendszerek alapanyagául.
- A bakteriális sejtfalakból izolált peptidoglikán nanoméretű részecskéi ígéretesek lehetnek nanomedicinális alkalmazásokban, például célzott gyógyszerszállításban vagy képalkotásban.
Antimikrobiális felületek
A peptidoglikán szintézisét gátló molekulák beépítése különböző felületekbe, például orvosi eszközökbe vagy kórházi berendezésekbe, hozzájárulhat az antimikrobiális felületek kialakításához. Ez segíthet csökkenteni a nosocomiális (kórházban szerzett) fertőzések kockázatát.
A peptidoglikán és származékai tehát nemcsak biológiai jelentőséggel bírnak, hanem a modern biotechnológia és ipar számos területén is ígéretes lehetőségeket rejtenek magukban, a gyógyászattól az anyagtudományig.
Peptidoglikán-analógok és új terápiás stratégiák
Az antibiotikum-rezisztencia növekedésével sürgetővé vált az új antimikrobiális szerek és terápiás stratégiák fejlesztése. A peptidoglikán továbbra is kiemelt célpont, és a kutatók különböző megközelítésekkel próbálják felhasználni a szerkezetével és szintézisével kapcsolatos ismereteket az új generációs gyógyszerek megalkotására.
Peptidomimetikumok
A peptidomimetikumok olyan szintetikus molekulák, amelyek utánozzák a természetes peptidek, például a peptidoglikán építőkövei vagy az antibiotikumok szerkezetét, de javított farmakológiai tulajdonságokkal rendelkeznek (pl. stabilitás, biológiai hozzáférhetőség).
- A peptidoglikán prekurzorainak, mint például a D-Ala-D-Ala-nak a mimetikumai fejleszthetők, amelyek kompetitíven gátolják a sejtfal szintézisét, vagy olyan szerkezeti analógok, amelyek a PBP-khez kötődnek, de rezisztensebbek a béta-laktamázokkal szemben.
- Ezek a vegyületek célzottan blokkolhatják a peptidoglikán szintézisének kulcsfontosságú enzimeit, új utakat nyitva a rezisztens baktériumok elleni küzdelemben.
Antimikrobiális peptidek (AMP-k) és a peptidoglikán integritására gyakorolt hatásuk
Az antimikrobiális peptidek (AMP-k), más néven gazda védekező peptidek, a veleszületett immunrendszer alapvető komponensei. Számos AMP közvetlenül károsítja a bakteriális membránt, de vannak olyanok is, amelyek a peptidoglikán szintézisét vagy integritását célozzák.
- Bizonyos AMP-k képesek behatolni a sejtfalba, és gátolni a peptidoglikán-szintetizáló enzimeket, vagy destabilizálni a peptidoglikán szerkezetét.
- Más AMP-k a peptidoglikánhoz kötődve megváltoztathatják annak konformációját, ami a sejtfal gyengüléséhez és líziséhez vezet.
- Az AMP-k előnye, hogy gyakran széles spektrumúak, és a baktériumok nehezebben fejlesztenek ki rezisztenciát ellenük, mivel többféle célpontot is támadhatnak egyszerre.
Fágterápia és a peptidoglikán célzása
A bakteriofágok (fágok) olyan vírusok, amelyek specifikusan baktériumokat fertőznek és líziselnek. A fágterápia, amely a szovjetunióban és Kelet-Európában régóta alkalmazott módszer, reneszánszát éli a rezisztencia problémája miatt.
- A fágok gyakran termelnek lizineket (endolizineket), amelyek a fág replikációs ciklusának végén szabadulnak fel, és hidrolizálják a bakteriális peptidoglikánt a sejt lízisének előidézésével.
- Ezeket a lizineket önmagukban is lehet vizsgálni, mint potenciális antimikrobiális szereket. A rekombináns lizin enzimek rendkívül specifikusak és hatékonyak lehetnek a rezisztens baktériumok ellen, mivel közvetlenül a sejtfalat bontják, anélkül, hogy a baktériumok aktív metabolikus állapotára lenne szükség.
CRISPR/Cas rendszerek alkalmazása baktériumok ellen
A CRISPR/Cas rendszerek, amelyek eredetileg a baktériumok adaptív immunrendszerét alkotják, forradalmasították a génszerkesztést. Ezeket a rendszereket már arra is vizsgálják, hogy specifikusan inaktiválják a rezisztencia géneket a baktériumokban.
- Egyes megközelítésekben a CRISPR/Cas rendszereket úgy tervezik, hogy célzottan elpusztítsák azokat a géneket (pl. mecA, vanA), amelyek a peptidoglikán-célzó antibiotikumokkal szembeni rezisztenciát kódolják.
- Ez a stratégia lehetővé tenné a „rezisztencia-mentesítés” elérését, visszaállítva a régi antibiotikumok hatékonyságát.
Kombinált terápiák
A kombinált terápiák, amelyek több antibiotikumot vagy antibiotikumot és más antimikrobiális szert alkalmaznak együtt, gyakran hatékonyabbak a rezisztens baktériumok ellen.
- Például egy peptidoglikán szintézist gátló antibiotikumot kombinálhatnak egy béta-laktamáz gátlóval (pl. amoxicillin/klavulánsav), hogy megvédjék az antibiotikumot az enzimális lebontástól.
- Más kombinációk magukban foglalhatják a peptidoglikán szintézist gátló szereket olyan vegyületekkel, amelyek a baktériumok virulencia faktorait célozzák, vagy amelyek modulálják a gazdaszervezet immunválaszát.
Ezek az új megközelítések reményt adnak az antibiotikum-rezisztencia válságának leküzdésében, és aláhúzzák a peptidoglikán, mint alapvető bakteriális célpont folyamatos relevanciáját a gyógyszerfejlesztésben.
Kutatási irányok és jövőbeli perspektívák
A peptidoglikán, mint a bakteriális élet fundamentuma, továbbra is intenzív kutatások tárgya. A mélyebb megértés nemcsak az alapvető biológiai folyamatokra derít fényt, hanem új utakat nyit meg az antimikrobiális stratégiák és a biotechnológiai alkalmazások fejlesztésében is. A jövőbeli kutatások számos izgalmas irányba mutatnak.
A peptidoglikán szintézis új gátlóinak felfedezése
Az antibiotikum-rezisztencia terjedése miatt folyamatosan szükség van új antimikrobiális szerekre. A kutatók aktívan keresik a peptidoglikán szintézisének eddig ismeretlen vagy kihasználatlan lépéseit, amelyek potenciális célpontot jelenthetnek.
- Ez magában foglalja a magas áteresztőképességű szűrési módszerek (high-throughput screening) alkalmazását új vegyületek azonosítására.
- A kombinatoriális kémia és a számítógépes gyógyszertervezés segíthet olyan molekulák megalkotásában, amelyek specifikusan és hatékonyan gátolják a peptidoglikán bioszintézisének kulcsenzimeit, miközben elkerülik a rezisztencia mechanizmusait.
- Különös figyelmet kapnak azok a vegyületek, amelyek a Gram-negatív baktériumok külső membránján is képesek áthatolni, leküzdve a permeabilitási akadályt.
Rezisztencia mechanizmusok mélyebb megértése
A baktériumok rezisztencia mechanizmusainak részletesebb feltárása elengedhetetlen az új gyógyszerek tervezéséhez és a rezisztencia terjedésének monitorozásához.
- A genomikai és proteomikai módszerek segítségével a kutatók azonosítják a rezisztenciáért felelős géneket és fehérjéket, valamint azokat a molekuláris útvonalakat, amelyek a rezisztencia kialakulásához vezetnek.
- A rezisztens törzsek evolúciójának és terjedésének nyomon követése segíthet a járványügyi előrejelzésekben és a közegészségügyi beavatkozások tervezésében.
- A cél a rezisztencia mechanizmusainak megkerülése vagy blokkolása olyan vegyületekkel, amelyek helyreállítják a meglévő antibiotikumok hatékonyságát (pl. béta-laktamáz gátlók új generációi).
A gazdaszervezet-baktérium interakciók vizsgálata
A peptidoglikán kulcsszerepet játszik a gazdaszervezet immunrendszerével való kölcsönhatásban. A kutatások célja ezen interakciók részletesebb megértése.
- Hogyan modulálja a peptidoglikán a veleszületett és adaptív immunválaszt?
- Milyen szerepet játszanak a peptidoglikán fragmentumok a krónikus gyulladásos betegségekben vagy az autoimmun állapotokban?
- Az immunrendszer modulálásával, például a peptidoglikán-származékok adjuvánsként történő alkalmazásával, javítható a vakcinák hatékonysága vagy kezelhetők az immunrendszer diszfunkciói.
Szintetikus biológia és a peptidoglikán
A szintetikus biológia lehetővé teszi a biológiai rendszerek tervezését és megépítését. Ennek keretében a kutatók vizsgálják, hogyan lehet módosítani vagy újraépíteni a peptidoglikán szintézis útvonalait.
- Ez magában foglalhatja a mesterséges baktériumok létrehozását, amelyek módosított peptidoglikánnal rendelkeznek, és ezáltal rezisztensebbek vagy érzékenyebbek bizonyos antibiotikumokkal szemben.
- Az ilyen kutatások hozzájárulhatnak a szintetikus vakcinák vagy az újgenerációs probiotikumok fejlesztéséhez.
A mikrobiom és a peptidoglikán metabolitok
A bélmikrobiom, amely milliárdnyi baktériumot tartalmaz, folyamatosan termel és bont le peptidoglikánt. Ennek a folyamatnak a metabolitjai jelentős hatással lehetnek a gazdaszervezet fiziológiájára és egészségére.
- A kutatások vizsgálják, hogyan befolyásolják a peptidoglikán lebontási termékei a bélrendszer immunitását, a gyulladásos folyamatokat, sőt még az agy-bél tengelyt is.
- A mikrobiom peptidoglikán-profiljának megértése új diagnosztikai és terápiás lehetőségeket nyithat meg a bélrendszeri betegségek, mint például az IBS vagy az IBD kezelésében.
A peptidoglikán tehát nem csupán egy régi, jól ismert bakteriális struktúra, hanem egy dinamikus molekula, amely folyamatosan új felfedezések forrása. A jövőbeli kutatások várhatóan tovább mélyítik ismereteinket a szerepéről a bakteriális életben, a gazdaszervezet-patogén interakciókban, és új, innovatív megoldásokat kínálnak a globális egészségügyi kihívásokra.