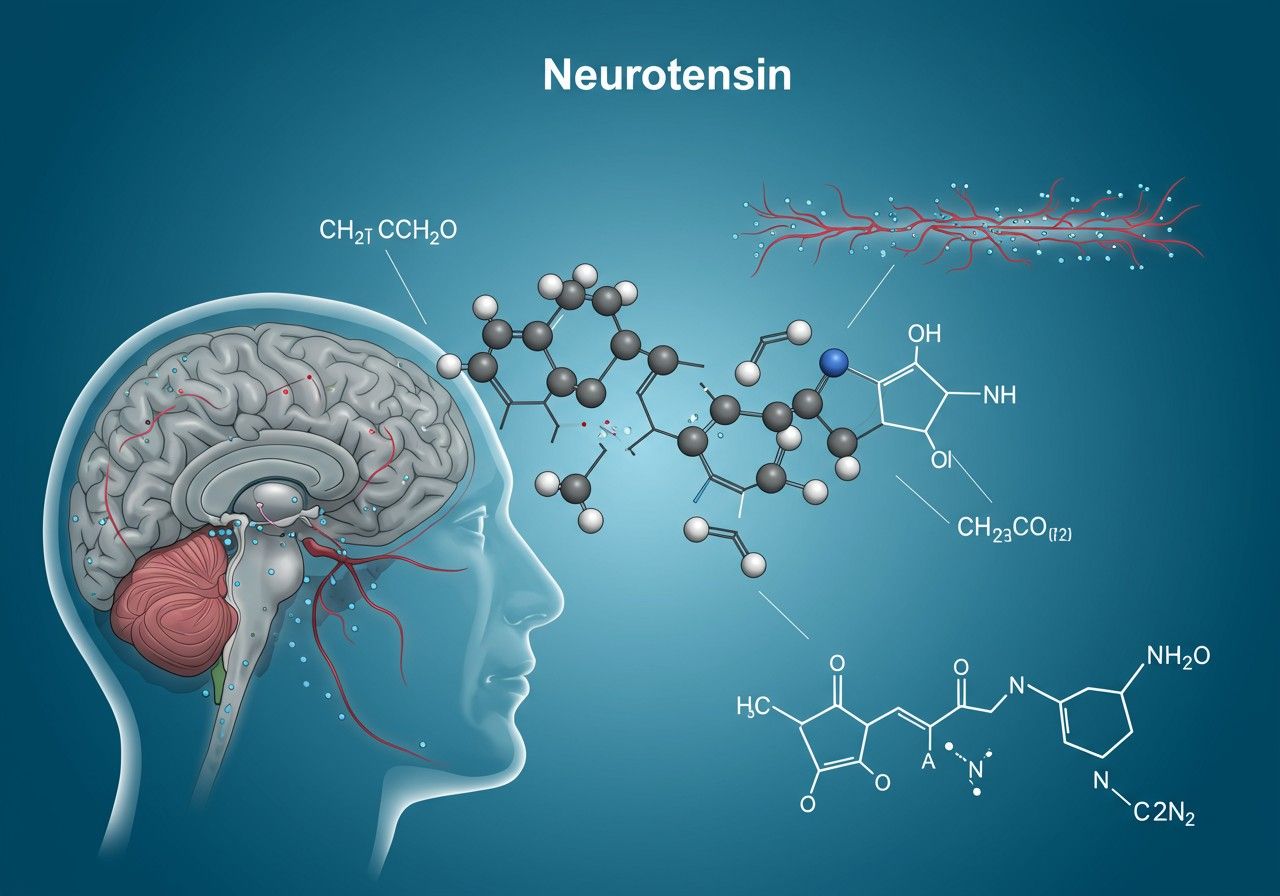
A neurotenzin egy, a szervezetben természetesen előforduló neuropeptid, amely a központi idegrendszerben és a gyomor-bél traktusban egyaránt kifejti hatásait. Ez a mindössze tizenhárom aminosavból álló molekula rendkívül sokrétű biológiai funkcióval rendelkezik, befolyásolva a fájdalomérzékelést, a testhőmérséklet-szabályozást, a dopaminerg rendszert, valamint számos emésztési és metabolikus folyamatot. Felfedezése az 1970-es évek elejére tehető, amikor Susan Leeman és munkatársai izolálták marha hipotalamuszból, és azóta intenzív kutatások tárgyát képezi, feltárva komplex szerepét mind az egészség, mind a betegségek patofiziológiájában. Ez a cikk részletesen bemutatja a neurotenzin kémiai szerkezetét, a receptorait, valamint azokat a kulcsfontosságú biológiai hatásokat, amelyek révén ez a kis peptid oly jelentős szerepet játszik szervezetünk működésében.
A neurotenzin kémiai szerkezete és bioszintézise
A neurotenzin egy tridekapeptid, ami azt jelenti, hogy 13 aminosavból épül fel. Pontos szekvenciája: pGlu-Leu-Tyr-Glu-Asn-Lys-Pro-Arg-Arg-Pro-Tyr-Ile-Leu-OH. Ez a specifikus aminosavsorrend kulcsfontosságú a peptid biológiai aktivitásához, különösen az N-terminális piroglutaminsav (pGlu) és a C-terminális Leu-Ile-Leu hármas, amelyek a receptorokhoz való kötődésben és az enzimális lebontással szembeni ellenállásban játszanak szerepet. A molekula viszonylag stabil, de számos peptidáz képes lebontani, ami korlátozza a biológiai felezési idejét és hatásának időtartamát.
A neurotenzin bioszintézise egy nagyobb prekurzor fehérjéből, az úgynevezett proneurotenzin/neuromedin N (pro-NT/NMN) prekurzorból indul ki. Ez a prekurzor fehérje nemcsak a neurotenzint, hanem egy másik bioaktív peptidet, a neuromedin N-t is tartalmazza. A szintézis során a prekurzor a riboszómákon képződik, majd a durva endoplazmatikus retikulumba kerül, ahol a jelpeptid levágása után a prohormon feldolgozása megkezdődik. A Golgi-készülékben és a szekréciós vezikulákban speciális endopeptidázok, például a prohormon konvertázok (PC1/3 és PC2) hasítják a prekurzort a megfelelő helyeken, felszabadítva a biológiailag aktív neurotenzint és neuromedin N-t. Ez a mechanizmus biztosítja, hogy a peptid pontosan a megfelelő helyen és időben termelődjön, a szervezet igényeinek megfelelően.
A neurotenzin expressziója és szintézise nem egyenletes a szervezetben. A központi idegrendszerben, különösen a hipotalamuszban, az amygdalában, a nucleus accumbensben, a ventrális tegmentális területen és az agytörzsben található neuronokban mutatható ki magas koncentrációban. Ezen kívül jelentős mennyiségben termelődik a gyomor-bél traktusban, specifikus enteroendokrin sejtekben, az úgynevezett N-sejtekben. Az emésztés során, különösen zsíros ételek fogyasztása után, a bélből felszabaduló neurotenzin fontos szerepet játszik a táplálékfeldolgozásban és a metabolikus szabályozásban. Ez a kettős lokalizáció – az agyban és a bélben – is aláhúzza a peptid sokoldalú szerepét.
Receptorok: a neurotenzin hatásmechanizmusának kulcsa
A neurotenzin biológiai hatásait specifikus receptorokon keresztül fejti ki, amelyek a sejtek felszínén helyezkednek el. Jelenleg három fő neurotenzin receptor (NTSR) típust ismerünk: az NTSR1, az NTSR2 és az NTSR3. Ezek a receptorok eltérő affinitással kötődnek a neurotenzinhez, különböző jelátviteli utakat aktiválnak, és változatos szöveti eloszlással rendelkeznek, ami hozzájárul a neurotenzin komplex és sokrétű biológiai szerepéhez.
NTSR1: a nagy affinitású, klasszikus receptor
Az NTSR1 egy G-protein-kapcsolt receptor (GPCR), amely a neurotenzinhez nagy affinitással kötődik. Ez a receptor felelős a neurotenzin legtöbb ismert biológiai hatásáért, beleértve a fájdalom modulációját, a testhőmérséklet szabályozását és a dopaminerg rendszerre gyakorolt hatásokat. Az NTSR1 széles körben elterjedt a központi idegrendszerben (különösen a dopaminerg neuronokban és az agykéregben), valamint a perifériás szövetekben, például a gyomor-bél traktusban és a hasnyálmirigyben. Aktiválódása a Gq/11 proteinen keresztül a foszfolipáz C (PLC) aktiválásához vezet, ami inozitol-trifoszfát (IP3) és diacilglicerol (DAG) termelődését eredményezi. Ezek másodlagos hírvivőként működnek, növelve az intracelluláris kalcium szintjét és aktiválva a protein kináz C-t (PKC). Ezen kívül az NTSR1 képes aktiválni a MAPK (mitogén-aktivált protein kináz) útvonalakat is, amelyek a sejtproliferációban, differenciációban és túlélésben játszanak szerepet. Az NTSR1 agonista aktiválása gyakran sejtszintű depolarizációt és excitációt vált ki.
NTSR2: a kis affinitású, atipikus receptor
Az NTSR2 szintén egy G-protein-kapcsolt receptor, azonban a neurotenzinhez lényegesen kisebb affinitással kötődik, mint az NTSR1. Eloszlása részben átfed az NTSR1-ével, de vannak egyedi expressziós területei is. Jelátviteli mechanizmusa összetettebb és kontextusfüggőbb. Bár képes G-proteinekkel is kapcsolódni, gyakran nem a klasszikus Gq/11 útvonalat aktiválja. Kimutatták, hogy az NTSR2 szerepet játszhat a fájdalom modulációjában, de hatása néha ellentétes az NTSR1 által kiváltott hatásokkal, vagyis pro-nociceptív hatásokat is kiválthat bizonyos körülmények között. Emellett szerepet tulajdonítanak neki a gyulladásos folyamatokban és a sejtek apoptózisában. Az NTSR2-nek az NTSR1-től eltérő farmakológiai profilja és jelátviteli útvonala ígéretes célponttá teszi a specifikus terápiás beavatkozások számára.
NTSR3/Sortilin: a multifunkcionális receptor
Az NTSR3, más néven sortilin, egy egyedi receptor, amely szerkezetileg eltér az NTSR1 és NTSR2 GPCR-ekről. A sortilin egy egyszerű transzmembrán doménnel rendelkező fehérje, amely eredetileg a fehérjék intracelluláris transzportjában és válogatásában játszott szerepéről volt ismert. A neurotenzinhez nagy affinitással kötődik, és nemcsak a neurotenzin felvételében és lebontásában vesz részt (mint egy „clearance” receptor), hanem jelátviteli funkciókkal is rendelkezik. Az NTSR3/sortilin aktiválása komplex intracelluláris útvonalakat indíthat el, amelyek befolyásolják a sejt túlélését, migrációját és differenciációját. Különösen fontos szerepe lehet a neurodegeneratív betegségekben, a rákban és a gyulladásos folyamatokban. A sortilin képes kölcsönhatásba lépni más receptorokkal és jelátviteli molekulákkal, tovább bonyolítva a neurotenzin hatásmechanizmusát és új terápiás lehetőségeket kínálva.
A három receptor típus közötti finom egyensúly és a különböző szövettípusokban való eltérő expresszió magyarázza a neurotenzin rendkívül sokrétű biológiai hatásait. A jövőbeli kutatások egyik fő célja ezen receptorok pontosabb farmakológiai profiljának feltérképezése és szelektív agonisták vagy antagonisták fejlesztése, amelyek lehetővé tennék a neurotenzin rendszer célzott modulálását terápiás célokra.
A neurotenzin szerepe a fájdalom modulációjában
A neurotenzin az egyik legfontosabb endogén fájdalomcsillapító (antinociceptív) peptid a szervezetben. Számos kutatás igazolta, hogy a neurotenzin központi adagolása, vagy a szervezet saját neurotenzin szintjének növelése jelentősen csökkenti a fájdalomérzékelést különböző típusú fájdalommodellekben, beleértve az akut, krónikus és neuropátiás fájdalmat is. Ez a hatás elsősorban az NTSR1 receptoron keresztül mediálódik, mely a gerincvelőben és az agytörzsben, a fájdalom feldolgozásában kulcsfontosságú területeken is nagy sűrűségben található.
A neurotenzin antinociceptív hatása többféle mechanizmuson keresztül valósul meg. Az egyik legfontosabb, hogy képes gátolni a fájdalomingerületet továbbító neurotranszmitterek, például a P-anyag (Substance P) felszabadulását a gerincvelő hátsó szarvában. A P-anyag egy pro-nociceptív neuropeptid, amely a fájdalomjelek perifériáról a központi idegrendszerbe történő továbbításában játszik kulcsszerepet. A neurotenzin gátló hatása révén csökkenti a fájdalomingerület afferens neuronokról a másodlagos neuronokra való átvitelét.
Emellett a neurotenzin modulálja a leszálló fájdalomgátló pályákat is, amelyek az agytörzsből indulnak ki és a gerincvelőbe vetülnek. Kölcsönhatásba lép az opioid rendszerrel is, bár a pontos mechanizmusok még részben tisztázatlanok. Kimutatták, hogy a neurotenzin képes fokozni az endogén opioidok, például az enkefalinok felszabadulását, vagy közvetlenül befolyásolni az opioid receptorok működését, ami szinergikus fájdalomcsillapító hatást eredményezhet. Ez a kölcsönhatás különösen ígéretes a fájdalomterápia szempontjából, mivel a neurotenzin agonisták potenciálisan opioid-spóroló hatással rendelkezhetnek, csökkentve az opioidok mellékhatásait és függőségi kockázatát.
A krónikus fájdalom állapotában, például neuropátiás fájdalomban, ahol a hagyományos fájdalomcsillapítók gyakran hatástalanok, a neurotenzin rendszert célzó terápiák új utat nyithatnak. A kutatások arra utalnak, hogy a neurotenzin szintje és receptorainak expressziója változhat krónikus fájdalom esetén, ami arra enged következtetni, hogy a neurotenzin rendszer modulálása jelentős terápiás potenciállal bírhat. Az NTSR1 agonisták fejlesztése, amelyek képesek átjutni a vér-agy gáton, ígéretes megközelítés lehet új, nem addiktív fájdalomcsillapító gyógyszerek előállítására.
„A neurotenzin nem csupán egy fájdalomcsillapító, hanem egy endogén modulátor, amely finoman hangolja a fájdalomérzetünket, és új távlatokat nyit a krónikus fájdalom kezelésében.”
Termoreguláció és a neurotenzin

A neurotenzin jelentős szerepet játszik a testhőmérséklet-szabályozásban, különösen a hipotermia (testhőmérséklet csökkenés) kiváltásában, amennyiben közvetlenül az agyba juttatják. Ez a hatás az egyik legkorábban felismert funkciója volt a peptidnek. Amikor a neurotenzint intracerebroventrikulárisan (az agykamrákba) vagy közvetlenül a hipotalamuszba adagolják, az állatok testhőmérséklete jelentősen csökken. Ez a hipotermikus hatás dózisfüggő, és elsősorban az NTSR1 receptoron keresztül mediálódik a hipotalamusz preoptikus régiójában, amely az agy termoregulációs központja.
A neurotenzin hipotermikus hatásának mechanizmusa komplex, és számos neurotranszmitter rendszerrel kölcsönhat. Kimutatták, hogy a neurotenzin befolyásolja a dopamin, szerotonin és noradrenalin rendszerek aktivitását a hipotalamuszban. Például, a dopamin felszabadulásának módosítása a hipotalamuszban hozzájárulhat a neurotenzin által kiváltott hőmérsékletcsökkenéshez. Ezen kívül befolyásolhatja a hőt leadó mechanizmusokat, mint például a vazodilatációt (érintágulatot) és a verejtékezést, illetve gátolhatja a hőtermelő folyamatokat, mint a remegés. A neurotenzin endogén felszabadulása a hipotalamuszban vélhetően egy természetes mechanizmus, amely segít fenntartani a testhőmérsékletet, különösen stresszre vagy külső hőmérsékleti változásokra adott válaszként.
A termoregulációra gyakorolt hatása miatt a neurotenzin és receptorai potenciális terápiás célpontot jelenthetnek olyan állapotokban, ahol a testhőmérséklet szabályozása zavart szenved, például lázas állapotokban, hőgutában, vagy akár bizonyos neurológiai betegségekhez társuló hőmérséklet-diszreguláció esetén. Azonban a hipotermia mellékhatásként is jelentkezhet, amennyiben a neurotenzin rendszert célzó gyógyszereket alkalmaznak más célból, például fájdalomcsillapításra vagy pszichiátriai kórképek kezelésére. Ezért a szelektív receptor modulátorok fejlesztése kulcsfontosságú a nem kívánt mellékhatások minimalizálásában.
A dopaminerg rendszer és a neurotenzin kölcsönhatása
A neurotenzin az egyik legszorosabban kapcsolódó neuropeptid a dopaminerg rendszerrel, amely kulcsszerepet játszik a jutalmazásban, motivációban, motoros kontrollban és a kognitív funkciókban. A neurotenzin és receptorai, különösen az NTSR1, nagy sűrűségben expresszálódnak a dopaminerg neuronokban és azok vetülési területein, mint például a nucleus accumbensben, a ventrális tegmentális területen (VTA) és a prefrontális kéregben.
A neurotenzin képes potenciálni a dopamin felszabadulását és hatásait ezeken a kulcsfontosságú agyterületeken. Kimutatták, hogy a neurotenzin közvetlenül befolyásolja a dopaminerg neuronok tüzelési mintázatát, növelve a dopaminerg aktivitást. Ez a kölcsönhatás magyarázza a neurotenzin szerepét olyan folyamatokban, mint a drogfüggőség kialakulása, ahol a dopaminerg jutalmazási útvonalak túlaktiválódnak. A neurotenzin fokozhatja a pszichostimulánsok, például az amfetamin és a kokain által kiváltott dopamin felszabadulást és viselkedési hatásokat.
A neurotenzin és a dopamin kapcsolatának klinikai jelentősége különösen kiemelkedő a skizofrénia kutatásában. A skizofrénia patofiziológiájában a dopaminerg hiperaktivitás, különösen a mezolimbikus dopaminerg pályán, központi szerepet játszik. Érdekes módon a neurotenzin agonisták antipszichotikus-szerű hatásokat mutatnak állatkísérletekben, és képesek gátolni a dopamin agonisták által kiváltott viselkedési szenzitizációt, ami a pszichózis modelljének tekinthető. Ez a megfigyelés arra utal, hogy a neurotenzin agonisták, vagy a neurotenzin lebontását gátló szerek potenciálisan új antipszichotikus gyógyszerek alapjául szolgálhatnak, kevesebb mellékhatással, mint a jelenlegi dopamin receptor blokkolók.
A neurotenzin képes modulálni a dopamin D2 receptorok funkcióját is, amelyek a jelenlegi antipszichotikumok fő célpontjai. Néhány kutatás szerint a neurotenzin képes csökkenteni a D2 receptorok számát vagy affinitását, vagy közvetlenül befolyásolni a D2 receptor által mediált jelátvitelt. Ez a komplex kölcsönhatás teszi a neurotenzint ígéretes célponttá a neurológiai és pszichiátriai rendellenességek, különösen a skizofrénia és a Parkinson-kór kezelésében. A Parkinson-kórban, ahol a dopaminerg neuronok degenerációja figyelhető meg, a neurotenzin neuroprotektív hatásai is relevánsak lehetnek, bár ezen a területen még további kutatásokra van szükség.
A dopaminerg rendszer és a neurotenzin közötti szoros kapcsolat tehát kulcsfontosságú a központi idegrendszer normális működésében és számos neurológiai, valamint pszichiátriai betegség patogenezisében. A neurotenzin rendszer célzott modulálása új terápiás stratégiákat kínálhat ezen komplex rendellenességek kezelésére.
A neurotenzin és a stresszválasz
A stresszválasz egy komplex fiziológiai és viselkedési reakció, amelyet a szervezet a homeosztázisát fenyegető ingerekre ad. A neurotenzin aktívan részt vesz ezen válasz modulálásában, mind a központi idegrendszerben, mind a periférián. Számos kutatás utal arra, hogy a neurotenzin anxiolitikus-szerű (szorongáscsökkentő) és stresszcsökkentő hatásokkal rendelkezhet, bár a pontos mechanizmusok és a kontextusfüggő szerepe még vizsgálat tárgyát képezi.
A neurotenzin expressziója és felszabadulása változik stresszhatás alatt. Például akut stressz esetén a neurotenzin szintje emelkedhet bizonyos agyterületeken, mint az amygdala és a hipotalamusz, amelyek a stresszválasz és az érzelmi szabályozás kulcsfontosságú központjai. Ez a megfigyelés arra utal, hogy a neurotenzin egy endogén mechanizmus része lehet, amely segít enyhíteni a stressz negatív hatásait.
A neurotenzin befolyásolja a hipotalamusz-hipofízis-mellékvese (HPA) tengely aktivitását, amely a stresszválasz központi szabályozója. Bár a pontos hatásirány és mechanizmus még vita tárgyát képezi, egyes tanulmányok szerint a neurotenzin gátolhatja a kortikotropin-felszabadító hormon (CRH) felszabadulását vagy hatását, ezáltal csökkentve a stresszhormonok, például a kortizol szintjét. Ez a hatás hozzájárulhat a szorongás és a stressz tüneteinek enyhítéséhez.
Viselkedési szinten is megfigyelték a neurotenzin anxiolitikus hatásait. Állatkísérletekben a neurotenzin adagolása csökkentette a szorongásos viselkedést különböző stresszmodellekben, például a nyitott tér tesztben vagy az emelt plusz labirintusban. Ez a hatás valószínűleg az NTSR1 receptoron keresztül mediálódik, és magában foglalja a neurotenzin kölcsönhatását más neurotranszmitter rendszerekkel, mint például a szerotoninnal és a GABA-val, amelyek szintén szorosan kapcsolódnak a szorongás szabályozásához.
A neurotenzin szerepe a stresszválaszban tehát kettős: egyrészt egyfajta pufferként működhet a túlzott stresszhatásokkal szemben, másrészt a stressz által kiváltott változások befolyásolhatják a neurotenzin rendszer aktivitását. Ez a komplex interakció rávilágít a neurotenzin rendszer potenciális terápiás jelentőségére a stresszel kapcsolatos rendellenességek, mint például a generalizált szorongás, a pánikbetegség vagy a poszttraumás stressz zavar (PTSD) kezelésében. A neurotenzin rendszer modulálása új, innovatív megközelítéseket kínálhat ezen állapotok kezelésére, a hagyományos anxiolitikumok mellékhatásainak elkerülésével.
Gyulladás és immunválasz: a neurotenzin rejtett kapcsolatai
A neurotenzin nem csupán az idegrendszerben és az emésztőrendszerben fejti ki hatását, hanem egyre inkább felismerik szerepét a gyulladásos folyamatokban és az immunválasz modulálásában is. A neurotenzin receptorok, különösen az NTSR1 és az NTSR3/sortilin, expresszálódnak különböző immunsejteken, mint például makrofágokon, mastocitákon és limfocitákon, ami arra utal, hogy a peptid közvetlenül befolyásolhatja ezeknek a sejteknek a működését.
Egyes tanulmányok szerint a neurotenzin pro-inflammatorikus hatásokkal rendelkezhet. Például képes kiváltani a mastociták degranulációját, ami hisztamin és más gyulladásos mediátorok felszabadulásához vezet. Ez a folyamat hozzájárulhat allergiás reakciókhoz és gyulladásos állapotokhoz. Ezen kívül a neurotenzin növelheti a gyulladásos citokinek, például az IL-6 és a TNF-α termelését és felszabadulását makrofágokból, fokozva ezzel a gyulladásos válasz súlyosságát.
Más kutatások azonban anti-inflammatorikus vagy immunmoduláló szerepet is tulajdonítanak a neurotenzinnek, ami a kontextusfüggő hatásmechanizmusra utal. Például bizonyos gyulladásos betegségekben, mint az irritábilis bél szindróma (IBS) vagy a gyulladásos bélbetegségek (IBD), a neurotenzin szintje és receptorainak expressziója megváltozik. Itt a neurotenzin a bélmozgás és a szekréció modulálásán keresztül befolyásolhatja a gyulladást, vagy közvetlenül hatva az immunsejtekre. Az NTSR3/sortilin receptoron keresztül a neurotenzin befolyásolhatja a sejtek túlélését és apoptózisát, ami szintén releváns a gyulladásos folyamatokban, ahol a sejtek elhalása és regenerációja kulcsfontosságú.
A neuroinflammáció területén is egyre inkább felismerik a neurotenzin szerepét. A központi idegrendszer gyulladásos folyamatai számos neurológiai és neurodegeneratív betegségben, mint például az Alzheimer-kór, a Parkinson-kór vagy a sclerosis multiplex, kulcsfontosságúak. A neurotenzin az agyi immunsejtekre (mikrogliákra és asztrocitákra) gyakorolt hatásán keresztül modulálhatja a neuroinflammatorikus választ, potenciálisan befolyásolva a betegségek progresszióját. Az NTSR1 és NTSR2 agonisták vagy antagonisták fejlesztése ezért ígéretes terápiás célpontot jelenthet a gyulladásos és autoimmun betegségek kezelésében, ahol a neurotenzin rendszer diszregulációja hozzájárul a patológiához.
A neurotenzin tehát egy komplex immunmodulátor, amely a gyulladásos válasz mind pro-, mind anti-inflammatorikus ágait befolyásolhatja a szöveti környezettől és a receptor expressziótól függően. Ennek a kettős szerepnek a pontosabb megértése kulcsfontosságú a célzott terápiás stratégiák kidolgozásában.
A neurotenzin szerepe a gyomor-bél rendszerben

A neurotenzin a központi idegrendszeren kívül az emésztőrendszerben is jelentős szerepet játszik, ahol hormonként és neurotranszmitterként is funkcionál. Főként a vékonybélben található enteroendokrin N-sejtek termelik és bocsátják ki, különösen zsírban gazdag ételek fogyasztása után. A bélből felszabadulva a neurotenzin bekerül a véráramba, és hormonális úton is kifejti hatásait, de lokálisan, parakrin módon is befolyásolja a bélműködést.
A neurotenzin számos fontos funkciót lát el a gyomor-bél traktusban:
- Motilitás szabályozása: Befolyásolja a gyomorürülést és a bélperisztaltikát. Általában lassítja a gyomorürülést és modulálja a bélmozgásokat, ami hozzájárul a táplálék lassabb áthaladásához és a jobb emésztéshez, abszorpcióhoz. Ez a hatás az NTSR1 receptoron keresztül mediálódik, mely a bél simaizomsejtjein és az enterális idegrendszer neuronjain is expresszálódik.
- Szekréció szabályozása: A neurotenzin befolyásolja a különböző emésztőnedvek, például a hasnyálmirigy enzimjeinek és a vékonybél nyálkahártyájának szekrécióját. Egyes kutatások szerint serkenti a hasnyálmirigy exokrin szekrécióját és a bikarbonát kiválasztását, ami fontos az emésztési folyamatok optimális pH-jának fenntartásában.
- Véráramlás modulálása: Növelheti a bél véráramlását, ami kulcsfontosságú a tápanyagok felszívódásához és a bél megfelelő működéséhez. Ez a vazodilatátor hatás segíti a bél nyálkahártyájának oxigén- és tápanyagellátását az emésztés során.
- Tápanyag felszívódás: Különösen a zsírok felszívódásában játszik szerepet. A zsírban gazdag ételek stimulálják a neurotenzin felszabadulását, amely hozzájárul a lipid emésztéshez és abszorpcióhoz.
- Trófikus hatások: A neurotenzin trófikus hatásokkal is rendelkezik a bél nyálkahártyájára, azaz serkenti a sejtek növekedését és differenciációját. Ez a hatás különösen fontos a bélnyálkahártya integritásának fenntartásában és a sérült szövetek regenerációjában, például gyulladásos bélbetegségek esetén.
A neurotenzin diszregulációja a gyomor-bél rendszerben számos emésztőrendszeri betegséghez kapcsolódhat. Például az irritábilis bél szindróma (IBS) egyes alaptípusaiban, ahol a bélmozgás és az érzékenység zavart szenved, a neurotenzin szintje és/vagy receptorainak expressziója megváltozhat. Hasonlóképpen, a gyulladásos bélbetegségek (IBD), mint a Crohn-betegség és a fekélyes vastagbélgyulladás, szintén összefüggésbe hozhatók a neurotenzin rendszer diszfunkciójával, különösen a peptid gyulladásmoduláló és trófikus hatásai révén.
A neurotenzin és receptorai tehát ígéretes terápiás célpontot jelentenek a gyomor-bél traktus rendellenességeinek kezelésében. A neurotenzin agonisták vagy antagonisták fejlesztése segíthet a bélmozgás, a szekréció és a gyulladás szabályozásában, javítva ezzel a betegek életminőségét.
Metabolikus funkciók és a neurotenzin
A neurotenzin nem csupán az idegrendszer és az emésztőrendszer funkcióit befolyásolja, hanem egyre inkább felismerik jelentős szerepét a metabolikus szabályozásban is. Különösen a glükóz-homeosztázis, az inzulinérzékenység és az energiaegyensúly modulálásában mutatkozik meg a peptid potenciális relevanciája, ami új perspektívákat nyit az elhízás és a 2-es típusú cukorbetegség kutatásában és kezelésében.
A neurotenzin, különösen a bélből felszabaduló formája, étkezés után emelkedett szinteken kering a vérben. Ez a cirkuláló neurotenzin hormonális úton befolyásolhatja a metabolikus szerveket. Kimutatták, hogy a neurotenzin képes serkenteni az inzulinszekréciót a hasnyálmirigy béta-sejtjeiből, bár ennek pontos mechanizmusa még vizsgálat alatt áll. Ez a hatás hozzájárulhat a vércukorszint étkezés utáni szabályozásához. Ezen kívül befolyásolhatja az inzulinérzékenységet is, bár ennek iránya és mértéke kontextusfüggő lehet.
Egyes kutatások arra utalnak, hogy a neurotenzin szerepet játszhat a lipidmetabolizmusban. Ahogy korábban említettük, a zsírban gazdag ételek fogyasztása stimulálja a neurotenzin felszabadulását a bélből. Ez a peptid hozzájárulhat a zsírok emésztéséhez és felszívódásához, és befolyásolhatja a lipidek raktározását és felhasználását a szervezetben. A neurotenzin emelkedett szintje összefüggésbe hozható az elhízással és a metabolikus szindrómával is. Elhízott egyénekben gyakran magasabb a cirkuláló neurotenzin szintje, ami arra utalhat, hogy a peptid diszregulációja hozzájárulhat az energiaegyensúly zavarához és a zsírraktározás fokozásához.
A neurotenzin központi hatásai is relevánsak a metabolizmus szempontjából. Az agyban a neurotenzin befolyásolhatja az étvágyat és a jóllakottság érzését. Bár a pontos hatásirány még nem teljesen tisztázott, egyes tanulmányok szerint a neurotenzin gátolhatja az étvágyat, míg mások szerint modulálhatja az evési viselkedést a dopaminerg jutalmazási rendszeren keresztül. Ez a komplex interakció aláhúzza a neurotenzin potenciális szerepét a testsúly-szabályozásban és az étkezési rendellenességekben.
A neurotenzin metabolikus szerepének mélyebb megértése új terápiás stratégiákat kínálhat az elhízás, a 2-es típusú cukorbetegség és a metabolikus szindróma kezelésében. A neurotenzin rendszer célzott modulálása, például szelektív receptor agonisták vagy antagonisták alkalmazásával, segíthet a glükóz-homeosztázis helyreállításában, az inzulinérzékenység javításában és a testsúly szabályozásában. Azonban további kutatásokra van szükség ahhoz, hogy teljes mértékben feltárjuk a neurotenzin komplex metabolikus hálózatba való integrációját és annak klinikai relevanciáját.
A neurotenzin és a kardiovaszkuláris rendszer
A neurotenzin biológiai hatásai nem korlátozódnak az idegrendszerre és az emésztőrendszerre; a kardiovaszkuláris rendszer működésében is szerepet játszik, bár ezen a területen még kevesebb kutatás történt, mint más funkciók esetében. A neurotenzin elsősorban vazodilatátor (értágító) hatásairól ismert, ami a vérnyomás csökkenéséhez vezethet.
Amikor a neurotenzint intravénásan adagolják, az perifériás vazodilatációt okoz, ami a vérnyomás átmeneti esését eredményezi. Ez a hatás valószínűleg a vérerek simaizomsejtjein expresszálódó NTSR1 receptorokon keresztül mediálódik. Az NTSR1 aktiválása az érrendszerben nitrogén-monoxid (NO) felszabadulását serkentheti, ami a simaizom relaxációját és értágulatot okoz. Ezen kívül a neurotenzin közvetlenül is befolyásolhatja a vaszkuláris tónust más mechanizmusokon keresztül, például a prosztaglandinok vagy más vazodilatátor mediátorok felszabadulásának módosításával.
A neurotenzin keringési hatásai azonban komplexek és dózisfüggőek lehetnek. Magasabb koncentrációkban vagy bizonyos körülmények között más effektorok is beléphetnek a képbe. A peptid befolyásolhatja a szívfrekvenciát és a szívizom kontraktilitását is, bár ezeknek a hatásoknak a klinikai relevanciája még nem teljesen tisztázott.
A neurotenzin endogén felszabadulása a véráramba étkezés után, különösen zsíros ételek fogyasztása esetén, utalhat arra, hogy a peptid szerepet játszik az étkezés utáni véráramlás szabályozásában, beleértve a splanchnikus (zsigeri) véráramlás növelését is, ami segíti az emésztést és a tápanyagok felszívódását. Ez a lokális vazodilatáció hozzájárulhat a bél megfelelő működéséhez.
Bár a neurotenzin közvetlen terápiás alkalmazása a kardiovaszkuláris betegségekben még nem terjedt el, a peptidrendszer modulálása elméletileg hasznos lehet olyan állapotokban, mint a magas vérnyomás (hipertónia) vagy az ischaemiás betegségek, ahol az értágulat előnyös lehet. Azonban a hipotenzív hatás, mint mellékhatás, figyelembe veendő a neurotenzin rendszert célzó gyógyszerek fejlesztésekor más indikációk esetén. A kardiovaszkuláris rendszerre gyakorolt hatásainak mélyebb megértése hozzájárulhat a neurotenzin teljes biológiai profiljának feltárásához és új terápiás lehetőségek azonosításához.
A neurotenzin és a neurológiai betegségek
A neurotenzin központi idegrendszeri eloszlása és a dopaminerg rendszerrel való szoros kapcsolata miatt számos neurológiai és pszichiátriai betegség patogenezisében potenciálisan fontos szerepet játszik. A neurotenzin rendszer diszfunkciója hozzájárulhat ezen állapotok kialakulásához vagy progressziójához, és ígéretes terápiás célpontot kínálhat.
Skizofrénia
A skizofrénia egy komplex pszichiátriai rendellenesség, amelyet a dopaminerg rendszer diszregulációjával hoznak összefüggésbe. Ahogy korábban említettük, a neurotenzin szorosan modulálja a dopamin felszabadulását és hatásait. A skizofréniás betegek agyában gyakran megfigyelhető a neurotenzin szintjének vagy receptorainak változása. Érdekes módon az antipszichotikus gyógyszerek, amelyek a dopamin D2 receptorokat blokkolják, gyakran növelik a neurotenzin expresszióját bizonyos agyterületeken, ami arra utal, hogy a neurotenzin egy endogén mechanizmus része lehet, amely kompenzálja a dopaminerg túlműködést. A neurotenzin agonisták antipszichotikus-szerű hatásai állatkísérletekben felvetik annak lehetőségét, hogy a neurotenzin rendszer modulálása új, hatékonyabb és kevesebb mellékhatással járó antipszichotikus terápiákat eredményezhet.
Parkinson-kór
A Parkinson-kór a dopaminerg neuronok progresszív degenerációjával járó neurodegeneratív betegség. Mivel a neurotenzin szorosan kapcsolódik a dopaminerg rendszerhez, szerepe a Parkinson-kórban is vizsgálat tárgyát képezi. Bár a direkt összefüggés még nem teljesen tisztázott, a neurotenzin neuroprotektív hatásokkal rendelkezhet, és befolyásolhatja a dopaminerg neuronok túlélését. Az NTSR1 agonisták potenciálisan enyhíthetik a motoros tüneteket, vagy lassíthatják a dopaminerg degenerációt, bár ezen a területen további kutatásokra van szükség. A neurotenzin szintje és receptorainak expressziója változhat a Parkinson-kóros betegek agyában, ami a betegség progressziójával vagy a gyógyszeres kezeléssel is összefüggésben állhat.
Alzheimer-kór és egyéb neurodegeneratív betegségek
Az Alzheimer-kór, amely a kognitív funkciók progresszív romlásával jár, a neuroinflammációval és az amiloid-béta (Aβ) plakkok lerakódásával is összefügg. A neurotenzin gyulladásmoduláló és neuroprotektív hatásai miatt potenciálisan releváns lehet az Alzheimer-kór patogenezisében. Az NTSR3/sortilin receptor, amely részt vesz a neurotenzin clearance-ében és a jelátvitelben, szintén szerepet játszhat az Aβ peptid feldolgozásában és clearance-ében. A neurotenzin agonista kezelés állatkísérletekben javította a kognitív funkciókat és csökkentette a neuroinflammációt Alzheimer-kór modellekben, ami ígéretes terápiás utat jelenthet.
A neurotenzin szerepét vizsgálják más neurodegeneratív betegségekben, mint például a Huntington-kórban és az amytrophiás laterális szklerózisban (ALS) is, ahol a peptid neuroprotektív hatásai és a gyulladásos folyamatokra gyakorolt moduláló képessége releváns lehet. A neurotenzin rendszert célzó terápiák tehát széles körű alkalmazást nyerhetnek a neurológiai betegségek kezelésében, amelyek gyakran komplex patofiziológiával rendelkeznek.
A neurotenzin potenciális terápiás alkalmazásai
A neurotenzin rendkívül sokrétű biológiai hatásai miatt jelentős terápiás potenciállal rendelkezik számos betegség kezelésében. A kutatók és gyógyszerfejlesztők nagy érdeklődéssel vizsgálják a neurotenzin rendszer modulálásának lehetőségeit, különösen szelektív receptor agonisták és antagonisták, valamint a peptid lebontását gátló enziminhibítorok fejlesztésén keresztül. Az alábbiakban bemutatjuk a legígéretesebb terápiás alkalmazási területeket.
Fájdalomcsillapítás
A neurotenzin egyik legmarkánsabb hatása a fájdalomcsillapítás. Az NTSR1 receptor szelektív agonistái rendkívül hatékony fájdalomcsillapítóként működhetnek, különösen krónikus és neuropátiás fájdalom esetén, ahol a jelenlegi terápiák gyakran elégtelenek vagy súlyos mellékhatásokkal járnak. Mivel a neurotenzin nem opioid mechanizmuson keresztül fejti ki fájdalomcsillapító hatását, potenciálisan kevesebb függőségi kockázattal és mellékhatással (pl. légzésdepresszió, székrekedés) járhat, mint az opioidok. A kihívást a vér-agy gáton való átjutás jelenti, ami a peptid alapú gyógyszereknél gyakori probléma. Kis molekulatömegű, orálisan is adható NTSR1 agonisták fejlesztése jelenti a jövőt ezen a területen.
Antipszichotikus kezelés
A neurotenzin és a dopaminerg rendszer közötti szoros kapcsolat miatt a neurotenzin agonisták ígéretes jelöltek a skizofrénia új generációs antipszichotikus gyógyszereinek fejlesztésére. Az NTSR1 agonisták képesek lehetnek a dopaminerg hiperaktivitás normalizálására anélkül, hogy a dopamin D2 receptorokat blokkolnák, ami a jelenlegi antipszichotikumok extrapyramidális mellékhatásaiért (pl. parkinsonizmus) felelős. Ez a megközelítés potenciálisan hatékonyabb és jobban tolerálható antipszichotikus terápiákat eredményezhet.
Metabolikus rendellenességek
A neurotenzin szerepe a glükóz-homeosztázisban, az inzulinérzékenységben és a lipidmetabolizmusban felveti a lehetőséget, hogy a neurotenzin rendszert célzó terápiák alkalmazhatók legyenek az elhízás, a 2-es típusú cukorbetegség és a metabolikus szindróma kezelésében. Az étvágyat és a jóllakottságot befolyásoló neurotenzin agonisták segíthetnek a testsúlycsökkentésben, míg az inzulinérzékenységet javító vegyületek a vércukorszint szabályozásában. Azonban a neurotenzin komplex metabolikus hatásai miatt további alapos kutatásokra van szükség a célzott terápiák kifejlesztéséhez.
Gyulladásos és autoimmun betegségek
A neurotenzin gyulladásmoduláló hatásai miatt releváns lehet a gyulladásos bélbetegségek (IBD), az irritábilis bél szindróma (IBS) és más gyulladásos állapotok kezelésében. Az NTSR1 és NTSR3/sortilin receptorokat célzó vegyületek segíthetnek a gyulladásos válasz szabályozásában és a szöveti károsodás csökkentésében. A neuroinflammációban betöltött szerepe miatt potenciálisan alkalmazható lehet neurodegeneratív betegségek, mint az Alzheimer-kór kiegészítő terápiájában is.
Rákterápia
Egyre több bizonyíték utal arra, hogy a neurotenzin és receptorai, különösen az NTSR1 és az NTSR3/sortilin, szerepet játszanak bizonyos rákos megbetegedések, például a hasnyálmirigyrák, a vastagbélrák és az emlőrák progressziójában. A neurotenzin serkentheti a rákos sejtek proliferációját, migrációját és invazivitását. Ennek megfelelően az NTSR antagonisták potenciális rákellenes gyógyszerekként vizsgálhatók, amelyek gátolhatják a daganat növekedését és metasztázisát.
„A neurotenzin, mint egy endogén mesterkapcsoló, rendkívüli lehetőségeket rejt magában a modern gyógyászat számára, a fájdalomtól a pszichózisig, a metabolikus zavaroktól a daganatos betegségekig.”
Kihívások és jövőbeli irányok
Bár a neurotenzin terápiás potenciálja jelentős, számos kihívással is szembe kell nézni. A peptid jellegű molekulák rövid felezési ideje, a vér-agy gáton való nehéz átjutása és a szelektív szállítás problémái korlátozzák a közvetlen alkalmazásukat. Ezért a kutatások a kis molekulatömegű, nem peptid jellegű agonisták és antagonisták, valamint a peptidáz-inhibítorok fejlesztésére összpontosítanak, amelyek stabilabbak és jobb biohasznosulással rendelkeznek. Emellett a neurotenzin receptorok komplex jelátviteli mechanizmusainak és a különböző receptorok közötti finom egyensúlynak a pontosabb megértése kulcsfontosságú a specifikus és hatékony terápiás stratégiák kidolgozásában.
A jövőbeli kutatások várhatóan mélyebben feltárják a neurotenzin és más neuropeptidek közötti kölcsönhatásokat, valamint a peptid szerepét az egyéni genetikai és környezeti tényezők által befolyásolt betegségekben. A célzott neurotenzin moduláció révén remélhetőleg új és hatékonyabb kezelési lehetőségek válnak elérhetővé számos súlyos betegségben.
Jövőbeli kutatási irányok és kihívások
A neurotenzin kutatása az elmúlt évtizedekben jelentős előrelépéseket hozott, feltárva e sokoldalú neuropeptid szerkezetét, funkcióit és biológiai hatásait. Mindazonáltal még számos tisztázatlan kérdés van, és a jövőbeli kutatási irányok a mélyebb megértésre és a terápiás potenciál teljes kiaknázására összpontosítanak. A neurotenzin rendszerrel kapcsolatos kihívások és lehetőségek a következőkben foglalhatók össze.
Szelektív receptor modulátorok fejlesztése
Az egyik legnagyobb kihívás és egyben lehetőség a szelektív NTSR1, NTSR2 és NTSR3/sortilin agonisták és antagonisták fejlesztése. Mivel a neurotenzin különböző receptorokon keresztül eltérő, sőt néha ellentétes hatásokat is kiválthat, a receptor-szelektív vegyületek elengedhetetlenek a célzott terápiás beavatkozásokhoz, minimalizálva a nem kívánt mellékhatásokat. Különösen fontos a kis molekulatömegű, nem peptid jellegű vegyületek azonosítása, amelyek képesek átjutni a vér-agy gáton, és orálisan is hatékonyak. Ez a terület a gyógyszerkémia és a farmakológia egyik legaktívabb része.
A neurotenzin komplex jelátviteli útvonalainak feltárása
Bár az NTSR1 és NTSR2 G-protein-kapcsolt receptorokként ismertek, a pontos downstream jelátviteli útvonalaik, különösen különböző sejttípusokban és fiziológiai állapotokban, még nem teljesen tisztázottak. Az NTSR3/sortilin, mint egyedi szerkezetű receptor, még inkább megköveteli a jelátviteli mechanizmusainak részletes feltárását. A receptorok dimerizációja, a G-protein-független jelátvitel (pl. béta-arrestin útvonalak), valamint a más receptorokkal és intracelluláris fehérjékkel való kölcsönhatásainak megértése kulcsfontosságú lesz a neurotenzin hatásmechanizmusának teljes feltárásához.
A neurotenzin és más neuropeptidek/neurotranszmitterek kölcsönhatásai
A neurotenzin nem izoláltan működik a szervezetben, hanem egy komplex hálózat része, amely számos más neuropeptiddel, neurotranszmitterrel és hormonnal interakcióban áll. A dopaminerg rendszerrel való kölcsönhatása jól ismert, de a szerotoninnal, opioidokkal, GABA-val és glutamáttal való interakciói még további kutatást igényelnek. Ezen interakciók feltárása segíthet megérteni a neurotenzin rendkívül sokrétű biológiai hatásait, és új kombinált terápiás stratégiákat eredményezhet.
A neurotenzin szerepe a betegségek progressziójában és biomarker potenciálja
A neurotenzin szintjének és receptorainak expressziójának változásai számos betegségben megfigyelhetők, mint például a skizofrénia, Parkinson-kór, Alzheimer-kór, gyulladásos bélbetegségek és rák. A jövőbeli kutatásoknak arra kell fókuszálniuk, hogy a neurotenzin biomarkerént is alkalmazható-e ezen betegségek diagnózisában, prognózisában vagy a terápiás válasz monitorozásában. A cirkuláló neurotenzin prekurzorok vagy metabolitok mérése egyszerű és nem invazív módszert kínálhat erre.
Genetikai és epigenetikai tényezők
A neurotenzin rendszer működését befolyásoló genetikai polimorfizmusok és epigenetikai módosulások vizsgálata új betekintést nyújthat a betegségekre való hajlamosságba és a terápiás válasz egyéni eltéréseibe. A személyre szabott orvoslás szempontjából kulcsfontosságú lehet annak megértése, hogy egyes egyének miért reagálnak eltérően a neurotenzin rendszert célzó terápiákra.
Összességében a neurotenzin egy rendkívül izgalmas és ígéretes kutatási terület marad. A jövőbeli kutatások várhatóan nemcsak elméleti tudásunkat mélyítik el, hanem új, innovatív terápiás lehetőségeket is kínálnak számos súlyos betegség kezelésére, javítva a betegek életminőségét szerte a világon.