A modern hordozható elektronikai eszközök világában a felhasználók gyakran szembesülnek a legkülönfélébb elemekkel és akkumulátorokkal. Bár ma már a lítium-ion technológia dominál, és az alkáli elemek is széles körben elterjedtek, érdemes visszatekinteni a múltba, ahol egykor egy különleges elem, a higany-oxidos szárazelem töltött be kulcsszerepet. Ez a kémiai áramforrás, amely stabil feszültségével és hosszú élettartamával forradalmasította a miniatűr elektronika területét, mára szinte teljesen eltűnt a piacról a benne található higany rendkívüli toxicitása miatt. Ennek ellenére technológiai öröksége jelentős, és megértése alapvető ahhoz, hogy felfogjuk az elemek fejlődését és a környezetvédelmi szempontok fontosságát az iparban.
A higany-oxidos elem története a második világháború idejére nyúlik vissza, amikor a hordozható rádiók, fémkeresők és más katonai eszközök megbízható, kompakt áramforrásaira óriási igény mutatkozott. Ekkor, 1942-ben fejlesztette ki Samuel Ruben a ma Ruben-cella néven is ismert elektrokémiai rendszert, amely a higany(II)-oxidot használta katódként, a cinket anódként, és lúgos elektrolitban működött. Az elemek gyorsan népszerűvé váltak a civil szférában is, különösen a hallókészülékekben, fényképezőgépekben és karórákban, ahol a stabil feszültség és a kis méret kritikus fontosságú volt.
A higany-oxidos szárazelem alapjai és történelmi kontextusa
A higany-oxidos szárazelem, vagy egyszerűen higanyelem, egy primer galvánelem, ami azt jelenti, hogy nem újratölthető. Működése során a kémiai energiát közvetlenül elektromos energiává alakítja, és a kémiai reakciók visszafordíthatatlanok. Az elemet elsősorban a folyamatos és stabil feszültség jellemezte a kisülés nagy részében, ami 1,35 V vagy 1,4 V volt, típustól és elektrolittól függően. Ez a tulajdonság különösen értékessé tette az olyan precíziós eszközökben, mint a fénymérők és az orvosi implantátumok, ahol a feszültségesés torzította volna a méréseket vagy a működést.
A Samuel Ruben által kifejlesztett cella forradalmi volt, mert az akkori szén-cink elemekhez képest sokkal nagyobb energiasűrűséggel rendelkezett, hosszabb ideig tartotta a feszültséget, és sokkal jobban ellenállt a hőmérséklet-ingadozásoknak és a tárolásnak. A Ruben-cella gyorsan szabványos ipari termékké vált, és évtizedekig meghatározó szerepet játszott a miniatűr energiaellátásban. A design alapvetően a gombelem formátumra épült, amely lehetővé tette a rendkívül kompakt eszközök, például a hallókészülékek elterjedését.
„A higany-oxidos elem stabilitása és megbízhatósága a korabeli miniatűr elektronika sarokkövévé tette, lehetővé téve olyan eszközök fejlesztését, amelyek korábban elképzelhetetlenek lettek volna.”
Az elemek népszerűségét az is növelte, hogy a folyamatos, alacsony áramú kisülésre optimalizálták őket, ami tökéletesen megfelelt a legtöbb hordozható elektronikai eszköz igényeinek. A feszültség stabilitása abból adódott, hogy a kisülési reakciók során az elektrolit koncentrációja és a pH-érték viszonylag állandó maradt, ellentétben például a szén-cink elemekkel, ahol a savas elektrolit elhasználódásával a feszültség folyamatosan csökkent.
A higany-oxidos szárazelem részletes felépítése
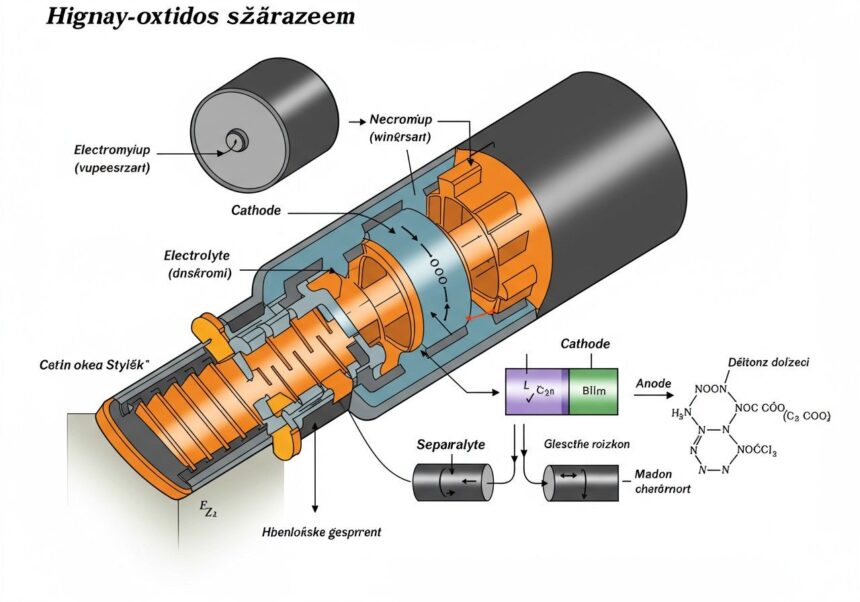
A higany-oxidos elem felépítése viszonylag egyszerű, de rendkívül funkcionális, különösen a miniatürizálás szempontjából. A legtöbb ilyen elem gombelem formájában készült, de léteztek hengeres és prizmatikus változatok is. Nézzük meg a főbb komponenseket:
Az anód: a cink elektróda
A higany-oxidos elem anódja nagytisztaságú, porózus cinkből készült. A cinkporral megnövelték az elektróda felületét, ami hozzájárult a nagyobb áramleadó képességhez és a hatékonyabb reakcióhoz. A cinket gyakran amalgamálták, azaz kis mennyiségű higannyal ötvözték. Ez a higany adalék két fő célt szolgált:
- Korrózióvédelem: Megakadályozta a cink spontán korrózióját, azaz a hidrogéngáz képződését az elektrolitban, ami az elem önkisüléséhez vezetne. A higany egy védőréteget képezett a cink felületén, gátolva a nem kívánt mellékreakciókat.
- Egyenletes reakció: Segítette a cink egyenletes oldódását a kisülés során, ezzel biztosítva a stabil feszültséget.
Az anód jellemzően az elem felső, negatív pólusát képezte, és egy fém burkolat, általában nikkelezett acél fedte.
A katód: a higany(II)-oxid
A katód anyaga a névadó higany(II)-oxid (HgO) volt, általában grafitporral keverve. A grafit nem csak vezetőképes adalékanyagként szolgált, hanem a higany-oxid reakciójának felgyorsításában is szerepet játszott. A higany(II)-oxidot általában egy sűrű paszta formájában préselték az elem alsó részébe, amely a pozitív pólust képezte. A katód reakciója során a higany(II)-oxid redukálódott fémhigannyá, ami a cella működésének egyik fő velejárója volt.
A katód anyaga a kémiai reakciók során nem változtatja meg jelentősen a térfogatát, ami hozzájárult az elem mechanikai stabilitásához és hosszú élettartamához.
Az elektrolit: lúgos oldat
A higany-oxidos elem elektrolitja egy lúgos oldat volt, leggyakrabban kálium-hidroxid (KOH) vagy nátrium-hidroxid (NaOH). A kálium-hidroxid elektrolittal készült elemek jobb teljesítményt nyújtottak alacsony hőmérsékleten és nagyobb áramleadásra voltak képesek, míg a nátrium-hidroxid elektrolit olcsóbb volt és hosszabb tárolási élettartamot biztosított. Az elektrolit feladata az ionok szállítása az anód és a katód között, lehetővé téve az elektrokémiai reakciók lejátszódását.
Az elektrolitot egy abszorbens anyagba, például cellulózba vagy más szintetikus anyagszálakba itatták, hogy szilárdabb, „szárazabb” cellát kapjanak, ami csökkentette a szivárgás kockázatát és növelte a mechanikai stabilitást.
A szeparátor és a burkolat
A szeparátor egy vékony, porózus anyagból készült membrán volt, amely fizikailag elválasztotta az anódot a katódtól, de lehetővé tette az ionok áthaladását. Ez megakadályozta a rövidzárlatot az elektródák között. Anyaga általában cellulóz, nejlon vagy más szintetikus polimer volt, amelyet az elektrolitba itattak.
Az elem külső burkolata általában nikkelezett acélból készült, ami mechanikai védelmet nyújtott és egyben az egyik elektromos pólust is képezte. A burkolat szigetelését műanyag gyűrűk és tömítések biztosították, amelyek megakadályozták az elektrolit szivárgását és a rövidzárlatot. A gombelemek esetében a burkolat alsó része a pozitív pólus (katód), a felső része pedig a negatív pólus (anód) volt.
A működési elv: elektrokémia a gyakorlatban
A higany-oxidos szárazelem működése egy sor elektrokémiai reakción alapul, amelyek a cink anód és a higany(II)-oxid katód felületén mennek végbe a lúgos elektrolit jelenlétében. A cella célja a kémiai energia elektromos energiává alakítása.
Az anód reakciója
Az anódon, a negatív elektródán, a cink (Zn) oxidálódik, azaz elektronokat ad le, és cink-hidroxiddá alakul a lúgos elektrolitban. Ez a cink-hidroxid tovább reagál, és végül cink-oxid (ZnO) képződik:
Zn + 2OH– → ZnO + H2O + 2e–
Ez a reakció szolgáltatja az elektronokat az áramkör számára. A cink-oxid szilárd anyag, amely az anód felületén marad, de nem gátolja a további reakciót.
A katód reakciója
A katódon, a pozitív elektródán, a higany(II)-oxid (HgO) redukálódik. Ez felveszi az anódról érkező elektronokat, és vízzel reagálva fémhiganyt (Hg) és hidroxidionokat (OH–) képez:
HgO + H2O + 2e– → Hg + 2OH–
Ez a reakció fogyasztja az elektronokat az áramkörből, és közben regenerálja a hidroxidionokat, amelyek visszatérnek az anódhoz, fenntartva az elektrolit lúgosságát. A fémhigany folyékony halmazállapotú, és a katód masszájában gyűlik össze.
Az összetett cellareakció és a feszültség stabilitása
Az anód- és katódreakciók összegezve adják a teljes cellareakciót:
Zn + HgO → ZnO + Hg
Ez a reakció mutatja, hogy a cink és a higany(II)-oxid fogy, míg cink-oxid és fémhigany képződik. A legfontosabb megfigyelés, hogy a teljes reakció során sem az elektrolit komponensei (OH–, H2O), sem a pH-érték nem változik jelentősen. Ez az oka a higany-oxidos elemek rendkívül stabil feszültségének a kisülés nagy részében. Amíg van elegendő aktív anyag (cink és higany-oxid), az elem közel állandó feszültséget ad le, jellemzően 1,35 V-ot (KOH elektrolit esetén) vagy 1,4 V-ot (NaOH elektrolit esetén). Csak a kisülés legvégén, amikor az egyik reagens elfogy, kezd el hirtelen esni a feszültség.
Ez a lapos kisülési görbe volt az egyik fő ok, amiért az elemeket olyan széles körben alkalmazták precíziós eszközökben, ahol a feszültségingadozás hibákat okozhatott. Más elemek, mint például az alkáli vagy a szén-cink elemek, folyamatosan csökkenő feszültséget mutatnak a kisülés során, ami kevésbé ideális bizonyos alkalmazásokhoz.
Hőmérsékletfüggés és önkisülés
A higany-oxidos elemek viszonylag jól teljesítettek a különböző hőmérsékleti tartományokban. A KOH elektrolittal készült változatok jobban bírták az alacsony hőmérsékletet, mint a NaOH-s társaik, de általánosan elmondható, hogy a teljesítményük stabilabb volt, mint sok más primer elemnek. Az önkisülés mértéke is alacsony volt, ami hosszú tárolási élettartamot eredményezett. Egy higanyelem akár 5-10 évig is megőrizte töltésének jelentős részét, ami különösen előnyös volt az olyan eszközökben, amelyeket ritkán használtak, de mindig üzemkész állapotban kellett lenniük, mint például a vészvilágítás vagy bizonyos orvosi eszközök.
A higany-oxidos elemek típusai és változatai

Bár a „higany-oxidos szárazelem” egy specifikus kémiai rendszerre utal, ezen belül is léteztek variációk, illetve fontos megkülönböztetni őket más primer elemtípusoktól, amelyekkel versenyeztek, vagy amelyeket felváltottak.
Elektrolit szerinti megkülönböztetés
Mint említettük, a két leggyakoribb elektrolit a kálium-hidroxid (KOH) és a nátrium-hidroxid (NaOH) volt. Ez a különbség finom, de jelentős hatással volt az elem teljesítményére:
- KOH elektrolitos elemek (1,35 V): Ezeket a változatokat jellemzően magasabb áramigényű, vagy alacsonyabb hőmérsékleten működő alkalmazásokhoz tervezték. Jobb teljesítményt nyújtottak hidegben és nagyobb terhelés alatt, de rövidebb tárolási élettartammal rendelkeztek. Gyakran használták hallókészülékekben és bizonyos katonai eszközökben.
- NaOH elektrolitos elemek (1,4 V): Ezek az elemek hosszabb tárolási élettartamot kínáltak, de alacsonyabb áramleadásra voltak képesek és kevésbé teljesítettek jól alacsony hőmérsékleten. Tipikus alkalmazási területük a karórák és a számológépek voltak, ahol az áramfelvétel minimális, de a hosszú élettartam kulcsfontosságú.
Formátumok és elnevezések
A higany-oxidos elemek leggyakrabban gombelem formájában készültek, de léteztek hengeres (pl. AA méretű, de már nem higanyos) és prizmatikus változatok is speciális alkalmazásokhoz. A gombelemek sokféle méretben elérhetőek voltak, és gyakran egyedi gyártói kódokkal jelölték őket, mint például PX625, PX13, MR9, RM400, amelyek mind higany-oxid cellákat jelöltek. Ezek a kódok gyakran az eredeti készülékekhez való illeszkedést jelezték, nem feltétlenül az elektrokémiai különbségeket.
Összehasonlítás más primer elemekkel
Fontos megérteni, miben különbözött a higany-oxidos elem a kortárs és utód primer elemektől:
| Jellemző | Higany-oxidos elem | Alkáli elem (pl. AA, AAA) | Ezüst-oxid elem | Cink-levegő elem |
|---|---|---|---|---|
| Névleges feszültség | 1,35 V / 1,4 V (nagyon stabil) | 1,5 V (feszültség esik a kisülés során) | 1,55 V (stabil) | 1,4 V (stabil) |
| Energiasűrűség | Magas | Közepes-magas | Magas | Nagyon magas |
| Élettartam | Hosszú (alacsony önkisülés) | Közepes (magasabb önkisülés) | Hosszú | Rövid (levegővel érintkezve) |
| Alkalmazás | Precíz eszközök (fénymérő, hallókészülék) | Általános célú eszközök | Gombelemek órákhoz, orvosi eszközökhöz | Hallókészülékek (ma) |
| Környezeti hatás | Nagyon mérgező (higany) | Környezetbarátabb (de hulladék) | Környezetbarátabb (ezüst értékes) | Környezetbarátabb |
Látható, hogy a higany-oxidos elem feszültségstabilitása az ezüst-oxid és a cink-levegő elemekhez hasonló volt, de az 1,35 V-os feszültsége jelentősen eltért az 1,5 V-os standardtól, ami később problémákat okozott az utódok bevezetésekor.
Alkalmazási területek és népszerűsége a múltban
A higany-oxidos elemek széles körben elterjedtek a hordozható elektronikai eszközökben a 20. század második felében. A stabil feszültség, a hosszú élettartam és a kompakt méret ideálissá tette őket számos alkalmazáshoz.
Hallókészülékek
Talán a hallókészülékek voltak az egyik legfontosabb alkalmazási terület. A hallókészülékeknek folyamatos, stabil feszültségre volt szükségük a tiszta hangvisszaadás érdekében. A higanyelemek hosszú üzemidőt biztosítottak kis méretben, ami elengedhetetlen volt a diszkrét és kényelmes viselethez. A hallókészülékekben használt gombelemek évtizedekig higany-oxid alapúak voltak, mielőtt a cink-levegő elemek felváltották volna őket.
Fényképezőgépek és fénymérők
Sok klasszikus fényképezőgép beépített fénymérője higany-oxidos elemmel működött. A fénymérők rendkívül érzékenyek a feszültség ingadozására, mivel az befolyásolja a mérési eredmények pontosságát. Az 1,35 V-os stabil feszültségű higanyelemek biztosították a pontos expozíciómérést a filmfotózás hőskorában. Amikor ezek az elemek eltűntek a piacról, sok régi fényképezőgép tulajdonosnak kellett alternatív megoldásokat keresnie, például feszültségkonvertereket vagy az eszköz átalakítását.
Órák és számológépek
A karórák és a korai elektronikus számológépek szintén gyakran használtak higanyelemeket. Ezek az eszközök alacsony áramfelvétellel működtek, de hosszú élettartamot igényeltek a gyakori elemcsere elkerülése érdekében. A higanyelemek alacsony önkisülése és stabil feszültsége ideális volt ezekhez az alkalmazásokhoz.
Orvosi eszközök és implantátumok
Bizonyos orvosi eszközökben és implantátumokban, ahol a megbízhatóság és a hosszú élettartam kritikus volt, szintén alkalmaztak higanyelemeket. Ezekben az esetekben a higany toxicitása ellenére a technológia előnyei felülmúlták a kockázatokat, különösen zárt rendszerekben.
Katonai és ipari alkalmazások
A kezdetektől fogva a katonai alkalmazások (pl. rádiók, adóvevők, éjjellátó készülékek) jelentős piacot jelentettek a higanyelemek számára a megbízhatóság és a széles hőmérsékleti tartományban való működés miatt. Az iparban is használták őket különböző érzékelőkben és mérőműszerekben.
A higany környezeti hatásai és a betiltás
A higany-oxidos elemek technológiai előnyei ellenére a bennük lévő higany jelentős környezetvédelmi és egészségügyi kockázatot jelentett. Ez a kockázat végül az elemek betiltásához vezetett világszerte.
Miért veszélyes a higany?
A higany egy neurotoxin, ami azt jelenti, hogy károsíthatja az idegrendszert. Különösen veszélyes a fejlődésben lévő magzatokra és kisgyermekekre. A higany bejuthat a szervezetbe belégzés, lenyelés vagy bőrön keresztül. A környezetbe kerülve a higany különböző formákban létezhet, de a legveszélyesebb a metil-higany, amely a vízi ökoszisztémákban keletkezik, és felhalmozódik a táplálékláncban (biomagnifikáció). A halakban lévő metil-higany különösen nagy kockázatot jelent az emberi fogyasztásra.
Egyetlen, eldobott higanyelem is jelentős mennyiségű higanyt tartalmazhatott, amely a hulladéklerakókba kerülve a talajba és a vizekbe szivároghatott, hosszú távú szennyezést okozva.
A környezetvédelmi aggályok növekedése
Az 1970-es és 80-as években egyre nagyobb figyelem irányult a környezetvédelemre és a veszélyes anyagok szabályozására. A higany globális szennyezőanyagként való felismerése sürgetővé tette a higanytartalmú termékek kivonását a forgalomból. Az elemekből származó higanyszennyezés jelentős problémát jelentett, különösen a nem szelektíven gyűjtött hulladékok esetében.
„A higany-oxidos elemek betiltása nem csupán egy technológiai váltás volt, hanem a környezetvédelem győzelme az ipari gyakorlat felett, egyértelmű üzenettel: az emberi egészség és a bolygó védelme elsődleges.”
Nemzetközi egyezmények és jogszabályok
Számos ország és nemzetközi szervezet hozott intézkedéseket a higanytartalmú elemek gyártásának és forgalmazásának korlátozására. Az Egyesült Államokban már az 1990-es években megkezdődött a kivonás, majd az Európai Unió is hasonlóan járt el. A Minamata egyezmény a higanyról, amelyet 2013-ban fogadtak el, egy globális megállapodás, amelynek célja a higany kibocsátásának csökkentése és a higanytartalmú termékek fázisos kivonása. Ez az egyezmény kimondta a higanyelemek gyártásának és forgalmazásának teljes tilalmát 2020-tól, bár a legtöbb országban már sokkal korábban megszűnt a kereskedelmi forgalmuk.
A betiltás következtében a gyártóknak alternatív, higanymentes elemeket kellett fejleszteniük, amelyek hasonló teljesítményt nyújtanak anélkül, hogy a környezetet veszélyeztetnék.
Alternatívák és utódok
A higany-oxidos elemek kivonása a piacról szükségessé tette, hogy a gyártók alternatív, környezetbarátabb technológiákat kínáljanak. Ezek az utódok különböző mértékben tudták pótolni a higanyelemek egyedi tulajdonságait.
Ezüst-oxid elemek (Silver-oxide cells)
Az ezüst-oxid elemek (Ag2O) az egyik legközvetlenebb utódnak tekinthetők. Ezek az elemek 1,55 V-os stabil feszültséget biztosítanak, és kiválóan alkalmasak az olyan precíziós eszközökbe, mint az órák és a modern fénymérők. Az ezüst-oxid elemek energiasűrűsége hasonló a higanyelemekéhez, és hosszú élettartammal rendelkeznek. Fő hátrányuk a viszonylag magas ár az ezüsttartalom miatt. Sok régi eszköz, amely 1,35 V-os higanyelemeket használt, nem működött megfelelően 1,55 V-os ezüst-oxid elemekkel a feszültségkülönbség miatt.
Alkáli elemek (Alkaline cells)
Az alkáli elemek (cink-mangán-dioxid) a legelterjedtebb primer elemek ma. Névleges feszültségük 1,5 V, de ez a feszültség a kisülés során folyamatosan csökken. Bár sok eszköz képes működni velük, a feszültségesés problémát jelenthet a feszültségre érzékeny berendezések, például a régi fénymérők esetében. Az alkáli elemek olcsók és széles körben elérhetőek, de általában nem rendelkeznek olyan hosszú tárolási élettartammal, mint a higany- vagy ezüst-oxid elemek.
Cink-levegő elemek (Zinc-air cells)
A cink-levegő elemek a mai hallókészülékek standard áramforrásai. Ezek az elemek a levegő oxigénjét használják katódként, ami rendkívül magas energiasűrűséget eredményez. Feszültségük 1,4 V körül van, és viszonylag stabil. Fő hátrányuk, hogy aktiválás után (amikor eltávolítják a védőfóliát, és a levegő bejut a cellába) gyorsan kisülnek, még akkor is, ha nem használják őket. Ezért csak akkor érdemes aktiválni őket, ha azonnal fel is használják.
Lítium elemek (Lithium cells)
A lítium elemek (pl. lítium-mangán-dioxid, lítium-vas-diszulfid) a legmodernebb primer elemek közé tartoznak. Magas, 3 V vagy 1,5 V feszültséget biztosítanak (kémiától függően), rendkívül hosszú élettartammal és széles hőmérsékleti tartományban való működéssel. Kiváló energiasűrűséggel rendelkeznek, és egyre inkább felváltják a régebbi technológiákat számos alkalmazásban, például autókulcsokban, orvosi eszközökben és intelligens otthoni szenzorokban. A lítium elemek azonban nem közvetlenül helyettesíthetők a régi 1,35 V-os higanyelemekkel a jelentős feszültségkülönbség miatt.
Kompatibilitási problémák és megoldások
A higany-oxidos elemek eltűnése komoly problémát jelentett sok régi, értékes elektronikai eszköz tulajdonosának. A 1,35 V-os feszültség egyedi volt, és a legtöbb utód elem (1,5 V vagy 1,55 V) magasabb feszültsége károsíthatta az érzékeny áramköröket vagy pontatlan mérésekhez vezethetett, különösen a fénymérőknél. Erre a problémára több megoldás született:
- Feszültségkonverterek: Különleges adapterek, amelyek beépített diódákkal vagy feszültségszabályzó áramkörökkel csökkentik az 1,55 V-os ezüst-oxid elem feszültségét 1,35 V-ra. Ezek a konverterek gyakran drágák, de lehetővé teszik a régi eszközök eredeti pontosságának megőrzését.
- Cink-levegő elemek átalakítása: Bár a cink-levegő elemek 1,4 V-os feszültsége közel áll az 1,35 V-hoz, a méretük gyakran eltér. Egyes felhasználók apró módosításokkal (pl. O-gyűrűkkel) illesztik be ezeket a régi készülékekbe. Azonban a cink-levegő elemek rövid élettartama aktiválás után korlátozza alkalmazhatóságukat.
- Eszközök átkalibrálása: Néhány esetben lehetséges volt a régi eszközök fénymérőjét átkalibrálni az 1,5 V-os elemekhez, de ez szakértelmet igényelt.
A gyűjtés és újrahasznosítás fontossága

Bár a higany-oxidos elemek már nem kaphatók a kereskedelmi forgalomban, még mindig előfordulhatnak régi háztartásokban, pincékben vagy padlásokon. Rendkívül fontos, hogy ezeket az elemeket felelősségteljesen kezeljük, és ne dobjuk a háztartási szemétbe.
Miért fontos a szelektív gyűjtés?
A higany rendkívül mérgező nehézfém, amely komoly környezeti és egészségügyi kockázatot jelent. Ha egy higanyelem a kommunális hulladékba kerül, a hulladéklerakóban szivárogni kezdhet, és a higany a talajvízbe, majd a táplálékláncba juthat. Ezért elengedhetetlen, hogy minden használt elemet, különösen a higanytartalmúakat, szelektíven gyűjtsünk.
A szelektív gyűjtés lehetővé teszi a higany biztonságos kezelését és visszanyerését. Az elemeket speciális gyűjtőpontokon, például elektronikai üzletekben, bevásárlóközpontokban vagy hulladékudvarokban lehet leadni, ahol gondoskodnak a szakszerű ártalmatlanításukról vagy újrahasznosításukról.
A higany visszanyerése
A korszerű újrahasznosító üzemek képesek a higanyelemekből a higanyt visszanyerni. Ez a folyamat általában desztillációval történik, ahol a higanyt felmelegítik, elpárologtatják, majd lehűtve tiszta fémhiganyként kondenzálják. A visszanyert higanyt ezután biztonságosan tárolják vagy újrahasznosítják zárt ipari folyamatokban, ahol a környezetbe jutás kockázata minimális. Az elem többi komponensét, mint például a cinket vagy az acélt, szintén újrahasznosítják, csökkentve ezzel a nyersanyagigényt és a környezeti terhelést.
A környezetvédelem szerepe
A higany-oxidos elemek története kiváló példája annak, hogyan változnak a technológiai prioritások a környezetvédelmi szempontok előtérbe kerülésével. Bár egykor forradalmiak voltak, a bennük rejlő veszélyek miatt mára szinte teljesen eltűntek. Ez a folyamat rávilágít arra, hogy a fenntarthatóság és a környezeti felelősségvállalás elengedhetetlen a modern iparban. A fogyasztóknak is fontos szerepük van ebben azáltal, hogy tudatosan kezelik az elemeket, és részt vesznek a szelektív gyűjtési programokban.
A higany-oxidos szárazelem öröksége
Bár a higany-oxidos szárazelem korszaka leáldozott, technológiai öröksége vitathatatlan. Helye az elektrokémia és a hordozható elektronika történetében megkérdőjelezhetetlen, és tanulságai ma is relevánsak.
Helye az elektrokémia történetében
A higany-oxidos elem a primer elemek fejlődésének egyik kulcsfontosságú állomása volt. Bebizonyította, hogy lehetséges stabil feszültségű, nagy energiasűrűségű, hosszú élettartamú miniatűr áramforrásokat készíteni. Ez a felismerés utat nyitott a későbbi ezüst-oxid és cink-levegő elemek, majd a modern lítium alapú technológiák fejlesztése előtt. Samuel Ruben munkája a higanyelemek terén alapozta meg a modern gombelemek elterjedését, amelyek nélkül ma már el sem tudnánk képzelni számos apró elektronikai eszközt.
Technológiai fejlődés inspirációja
A higanyelemek által támasztott kihívások – különösen a 1,35 V-os feszültség és a környezeti aggályok – inspirálták a mérnököket és vegyészeket új, jobb és biztonságosabb áramforrások fejlesztésére. Az alternatívák, mint az ezüst-oxid és a cink-levegő elemek, közvetlen válaszok voltak ezekre a kihívásokra, és tovább finomították a miniatűr elemek technológiáját.
Tanulságok a környezetvédelem szempontjából
A higany-oxidos elem története egy erőteljes emlékeztető arra, hogy a technológiai innovációnak kéz a kézben kell járnia a környezeti felelősségvállalással. Az elemek betiltása egyértelműen demonstrálta, hogy a tartós fenntarthatóság érdekében fel kell áldozni a múltbeli sikereket, ha azok hosszú távon károsak a bolygóra és az emberi egészségre. Ez a paradigmaváltás formálta azóta is az elemgyártás és az elektronikai ipar fejlődését, ösztönözve a környezetbarát anyagok és eljárások alkalmazását.
Összességében a higany-oxidos szárazelem nem csupán egy elfeledett technológia, hanem egy fontos fejezet az emberi találékonyság és a környezettudatosság fejlődésében. Megértése segít értékelni a mai modern elemeket, és emlékeztet a jövőbeni innovációk iránti felelősségünkre.