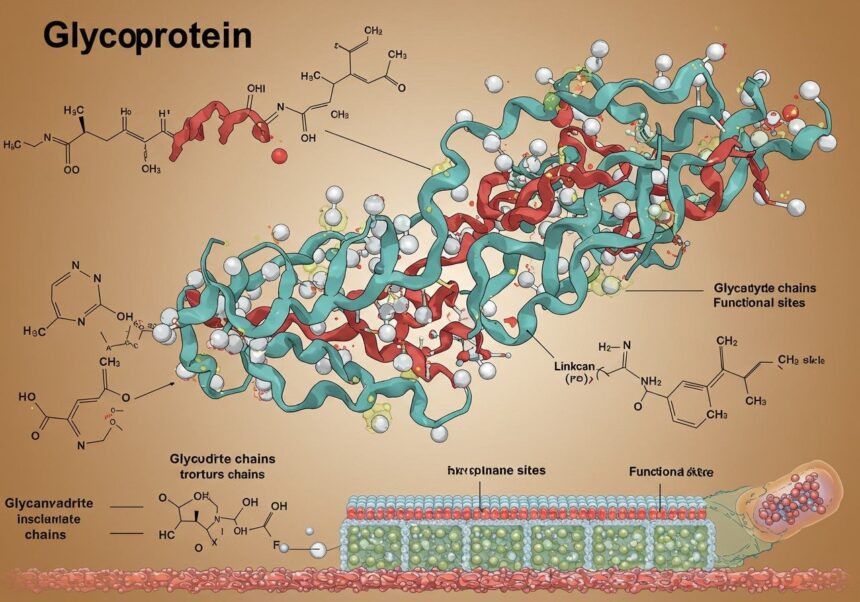
A biológiai rendszerek hihetetlenül összetettek, működésük alapját pedig a molekuláris szintű interakciók képezik. Ezen interakciók kulcsszereplői közé tartoznak a glükoproteidek, amelyek a fehérjék és szénhidrátok elegáns kombinációi. Ezek a molekulák nem csupán egyszerű építőkövek, hanem dinamikus struktúrák, melyek létfontosságú szerepet játszanak a sejtek felismerésében, a kommunikációban és a szervezet integritásának fenntartásában. A glükoproteidek kutatása az elmúlt évtizedekben robbanásszerűen fejlődött, feltárva sokrétű funkcióikat a normális fiziológiás folyamatoktól kezdve számos betegség patogeneziséig.
A glükoproteidek alapvetően olyan fehérjék, amelyekhez kovalensen kapcsolódnak egy vagy több oligoszacharid lánc, azaz glikán. Ez a kémiai módosítás, amelyet glikozilációnak nevezünk, jelentősen befolyásolja a fehérjék térbeli szerkezetét, stabilitását, oldhatóságát és biológiai aktivitását. A glikoziláció nem egy véletlenszerű folyamat, hanem egy erősen szabályozott mechanizmus, amely specifikus enzimek és szubsztrátok közreműködésével zajlik a sejten belül.
A szénhidrátláncok hozzáadása a fehérjékhez rendkívül sokféleséget eredményez. Ez a sokféleség a glikánok összetételében, elágazásában és kapcsolódási pontjaiban rejlik, ami lehetővé teszi, hogy a glükoproteidek rendkívül specifikus üzeneteket közvetítsenek és pontosan illeszkedjenek a különböző molekuláris partnerekhez. Éppen ez a komplexitás teszi őket nélkülözhetetlenné az életfolyamatok szinte minden területén.
A glükoproteidek szerkezeti felépítése
A glükoproteidek szerkezete két fő komponensre bontható: a fehérje magra és a hozzá kapcsolódó oligoszacharid láncokra, azaz glikánokra. A fehérje mag határozza meg a molekula alapvető funkcióját, míg a glikánok finomhangolják ezt a funkciót, és új tulajdonságokkal ruházzák fel a molekulát, például a sejt-sejt interakciókban vagy a molekuláris felismerésben.
A fehérje mag, más néven apoglikoprotein, a riboszómákon szintetizálódik a transzláció során, majd belép az endoplazmatikus retikulumba (ER), ahol megkezdi térbeli szerkezetének felvételét. Ez a fehérje lehet egyetlen polipeptidlánc vagy több alegységből álló komplex. A glikoziláció a fehérje szintézise után vagy azzal párhuzamosan indul meg, de mindig az ER-ben és a Golgi-készülékben zajlik.
Az oligoszacharid láncok kovalensen kapcsolódnak a fehérje maghoz, és ezek a láncok alkotják a glikán részt. Ezek a szénhidrátláncok jellemzően rövid, elágazó vagy lineáris polimerek, amelyek néhány monoszacharid egységből állnak. A leggyakrabban előforduló monoszacharidok közé tartozik a glükóz (Glc), galaktóz (Gal), mannóz (Man), N-acetilglükózamin (GlcNAc), N-acetilgalaktózamin (GalNAc), fukóz (Fuc) és a szialinsav (N-acetilneuraminsav, Neu5Ac).
A glükoproteidek sokfélesége a fehérje mag és a glikánok kombinációjából adódik, amelyek együttesen hozzák létre a biológiai információk gazdag tárházát.
A glikánok kapcsolódása a fehérje maghoz két fő típusra osztható: az N-glikozidikus és az O-glikozidikus kapcsolódásra. Ezek a kötések nemcsak kémiai természetükben, hanem a szintézisük helyében és mechanizmusában is eltérnek.
N-glikozidikus glükoproteidek
Az N-glikozidikus glikoziláció során az oligoszacharid lánc az aszparagin (Asn) aminosav oldalláncának nitrogénatomjához kapcsolódik. Ez a kapcsolódás mindig az -Asn-X-Ser/Thr- szekvencia részeként történik, ahol X bármilyen aminosav lehet, kivéve a prolint. Az N-glikoziláció az endoplazmatikus retikulumban kezdődik, és a Golgi-készülékben fejeződik be.
Az N-glikánok szerkezetük alapján három fő típusba sorolhatók:
- Magas mannóz tartalmú glikánok: Ezek a glikánok sok mannóz egységet tartalmaznak, és viszonylag egyszerűbb szerkezetűek. Gyakran az N-glikoziláció korai fázisában keletkeznek, és fontos szerepet játszanak a fehérje megfelelő feltekeredésében.
- Komplex glikánok: Ezek a glikánok sokféle monoszacharidot tartalmaznak, például GlcNAc-t, Gal-t, Fuc-t és szialinsavat. Elágazóbbak és változatosabbak, mint a magas mannóz tartalmú glikánok, és számos biológiai funkciót látnak el.
- Hibrid glikánok: A magas mannóz tartalmú és a komplex glikánok jellemzőit ötvözik. Egyik águk magas mannóz tartalmú, míg a másik komplex szerkezetű.
Az N-glikoziláció egy rendkívül komplex folyamat, amely egy közös, előregyártott oligoszacharid prekurzor (Glc3Man9GlcNAc2) átvitelével kezdődik a dolichol-foszfátról a fehérje aszparagin aminosavára. Ezt követően az ER-ben és a Golgi-ban enzimatikus módosítások sorozata zajlik, amelyek során glükóz és mannóz egységek távolítódnak el vagy adódnak hozzá, majd különböző monoszacharidok épülnek be, kialakítva a végső, érett N-glikán szerkezetet.
O-glikozidikus glükoproteidek
Az O-glikozidikus glikoziláció során az oligoszacharid lánc a szerin (Ser) vagy treonin (Thr) aminosavak hidroxilcsoportjához kapcsolódik. Ez a folyamat jellemzően a Golgi-készülékben zajlik, és közvetlenül a monoszacharidok hozzáadásával indul, nem pedig egy előregyártott prekurzor átvitelével.
Az O-glikánok szerkezete rendkívül változatos lehet, de a leggyakoribb típusok közé tartoznak a mucin típusú O-glikánok, amelyek a mucinokban, a nyálkahártyák fő komponenseiben találhatóak. Ezek a glikánok általában egy GalNAc molekulával kezdődnek, amely közvetlenül kapcsolódik a szerinhez vagy treoninhoz, majd erre épülnek rá további monoszacharidok.
Az O-glikoziláció további típusai közé tartozik a proteoglikánok glikozilációja, ahol hosszú, ismétlődő diszacharid egységekből álló glikozaminoglikán (GAG) láncok kapcsolódnak a fehérje maghoz. Ezek a GAG láncok, mint például a kondroitin-szulfát vagy a heparin-szulfát, nagy mennyiségű negatív töltést hordoznak, és fontos szerepet játszanak az extracelluláris mátrixban.
Egyéb glikozilációs típusok
Bár az N- és O-glikoziláció a leggyakoribb, léteznek más típusú glikozilációs mechanizmusok is:
- C-manoziláció: A mannóz egy triptofán (Trp) aminosavhoz kapcsolódik egy szén-szén kötéssel.
- Glikozilfoszfatidilinozitol (GPI) horgonyok: Ezek a komplex glikolipidek fehérjéket rögzítenek a sejtmembránhoz.
- O-GlcNAc glikoziláció: Egyetlen N-acetilglükózamin (GlcNAc) kapcsolódik szerinre vagy treoninra, gyakran citoplazmatikus és nukleáris fehérjéken. Ez a glikoziláció nem az ER-ben vagy a Golgi-ban zajlik, hanem a citoplazmában, és a foszforilációhoz hasonlóan szabályozza a fehérje aktivitását.
A glükoproteidek szerkezeti sokféleségének megértése alapvető fontosságú funkcióik feltárásához. Minden egyes glikán típus, sőt, minden egyes monoszacharid lánc egyedi információt hordoz, amelyet a sejt felismer és értelmez.
A glikoziláció mechanizmusai és szabályozása
A glikoziláció egy rendkívül összetett, szigorúan szabályozott poszttranszlációs módosítás, amely a fehérjékhez szénhidrátláncokat kapcsol. Ez a folyamat nem véletlenszerű, hanem specifikus enzimek (glikoziltranszferázok és glikozidázok) koordinált működésével zajlik, elsősorban az endoplazmatikus retikulumban (ER) és a Golgi-készülékben.
Az N-glikoziláció részletes mechanizmusa
Az N-glikoziláció az ER membránjában kezdődik egy speciális lipid hordozó, a dolichol-foszfát segítségével. A dolichol-foszfát egy hosszú láncú, izoprén egységekből álló lipid, amely a membránban horgonyozva tartja a szénhidrátláncot a szintézis során.
A folyamat lépései a következők:
- Oligoszacharid prekurzor szintézise: Egy nagy, elágazó oligoszacharid (Glc3Man9GlcNAc2) szintézise történik a dolichol-foszfáton. Ez a szintézis mind az ER citoplazmatikus oldalán, mind a lumen oldalán zajlik, a monoszacharidok egyesével adódnak hozzá a dolichol-foszfáthoz.
- Átvitel a fehérjére: Amint a fehérje mag belép az ER lumenébe és eléri az -Asn-X-Ser/Thr- szekvenciát, az oligoszacharid prekurzor egyetlen lépésben, egy oligoszacharidiltranszferáz enzim segítségével átkerül az aszparagin oldalláncának nitrogénatomjára.
- Trimming és folding: Az ER-ben a frissen glikozilált fehérje az ER chaperon fehérjék (pl. kalnexin, kalretikulin) segítségével kezdi meg a megfelelő térbeli szerkezetének felvételét. Ezen chaperonok felismerik a glükóz egységeket tartalmazó N-glikánokat. Glükozidáz enzimek eltávolítják a glükóz egységeket (trimming), ami kulcsfontosságú a fehérje minőség-ellenőrzésében. Ha a fehérje nem tekeredik fel megfelelően, ismételten glükozilálódhat, és újra bekerülhet a chaperon-ciklusba.
- Golgi módosítások: A megfelelően feltekeredett glikoproteid az ER-ből a Golgi-készülékbe kerül. Itt egy sor glikozidáz és glikoziltranszferáz enzim tovább módosítja az N-glikánt, eltávolítva mannóz egységeket, majd hozzáadva különböző monoszacharidokat (GlcNAc, Gal, Fuc, szialinsav), ami a komplex vagy hibrid N-glikánok kialakulásához vezet. Ezek a módosítások a Golgi különböző rekeszeiben, szekvenciális módon zajlanak.
A glikoziltranszferázok és glikozidázok szubsztrát-specifitása és elhelyezkedése a Golgi-készülékben rendkívül fontos a glikánok sokféleségének kialakításában. Minden egyes enzim egy specifikus monoszacharidot ad hozzá vagy távolít el egy adott kötésen keresztül, így alakul ki a végső, funkcionális glikán szerkezet.
Az O-glikoziláció részletes mechanizmusa
Az O-glikoziláció elsősorban a Golgi-készülékben zajlik, és eltér az N-glikozilációtól abban, hogy nem egy prekurzor oligoszacharid átvitelével kezdődik, hanem a monoszacharidok egyesével történő hozzáadásával.
A leggyakoribb O-glikozilációs típus, a mucin típusú O-glikoziláció, a következőképpen zajlik:
- Kezdő lépés: Az első monoszacharid, általában N-acetilgalaktózamin (GalNAc), közvetlenül kapcsolódik a fehérje szerin vagy treonin aminosavának hidroxilcsoportjához. Ezt a reakciót GalNAc-transzferázok katalizálják.
- Lánc meghosszabbítása: Ezt követően további monoszacharidok (pl. galaktóz, GlcNAc, fukóz, szialinsav) adódnak hozzá a GalNAc-hoz, különböző glikoziltranszferázok segítségével. A lánc meghosszabbítása és elágazása a Golgi különböző rekeszeiben, szekvenciális módon történik.
Az O-glikoziláció rendkívül heterogén, és számos különböző O-glikán szerkezetet eredményezhet, amelyek specifikus funkciókat látnak el. A mucinok esetében például ezek a glikánok hozzájárulnak a viszkózus, védőréteg kialakításához a nyálkahártyákon.
A glikoziláció szabályozása
A glikoziláció szabályozása kulcsfontosságú a sejtek normális működéséhez. Ezt a szabályozást számos tényező befolyásolja:
- Génexpresszió: A glikoziltranszferázok és glikozidázok génjeinek expressziója szigorúan szabályozott, ami meghatározza, hogy mely enzimek állnak rendelkezésre az adott sejtben.
- Enzimaktivitás: Az enzimek aktivitását poszttranszlációs módosítások (pl. foszforiláció) és alloszterikus szabályozás is befolyásolhatja.
- Szubsztrát elérhetősége: A monoszacharid donátorok koncentrációja is hatással van a glikozilációra.
- Sejttípus-specifikusság: Különböző sejttípusok eltérő glikozilációs mintázatokat mutatnak, ami hozzájárul a sejtek funkcionális specializációjához.
- Fejlődési állapot és betegségek: A glikozilációs mintázatok változhatnak a sejt fejlődése során, differenciációja során, valamint különböző betegségek, például rák esetén.
A glikoziláció bonyolult hálózata finomhangolja a fehérjék biológiai tulajdonságait, lehetővé téve a sejtek számára, hogy precízen reagáljanak környezetükre és részt vegyenek komplex biológiai folyamatokban.
A glikoziláció hibái súlyos következményekkel járhatnak, és számos veleszületett anyagcsere-betegség (CDG – Congenital Disorders of Glycosylation) hátterében állnak. Ezek a betegségek széles spektrumú klinikai tünetekkel járnak, amelyek a glikozilációban részt vevő specifikus enzimtől vagy transzportertől függenek.
A glükoproteidek előfordulása és elterjedése
A glükoproteidek rendkívül elterjedtek az élővilágban, a legegyszerűbb baktériumoktól kezdve a komplex többsejtű élőlényekig. Szinte minden sejtben és szövettípusban megtalálhatók, és elengedhetetlenek a normális fiziológiai funkciókhoz. Elhelyezkedésük és szerkezetük alapján betöltött szerepük is változatos.
Sejtfelszíni glükoproteidek
A sejtmembrán külső felszínén található glükoproteidek alkotják a sejt legkülső rétegét, a glikokalixet. Ez a szénhidrátban gazdag réteg kulcsszerepet játszik a sejt-sejt felismerésben, az adhézióban és a jelek továbbításában. Néhány fontos példa:
- Receptorok: Számos sejtmembrán receptor glikozilált. Ezek a receptorok specifikusan kötik a hormonokat, növekedési faktorokat, neurotranszmittereket és más jelzőmolekulákat, elindítva a sejten belüli jelátviteli útvonalakat. Például az inzulin receptor glikozilált, és a glikánok befolyásolhatják a receptor affinitását és jelátviteli képességét.
- Sejtadhéziós molekulák (CAMs): A CAMs, mint például a szelektinek, integrinek és kadherinek, gyakran glikoziláltak. Ezek a molekulák felelősek a sejtek közötti és a sejtek extracelluláris mátrixhoz való tapadásáért, ami alapvető fontosságú a szövetek integritásához, a sejtmigrációhoz és az immunválaszhoz. Például a szelektinek szénhidrátligandumokhoz kötődnek, lehetővé téve a leukociták tapadását az érfalhoz gyulladásos folyamatok során.
- Immunológiai azonosítók: A glükoproteidek fontosak az immunrendszer számára a „saját” és „nem saját” sejtek megkülönböztetésében.
- MHC (Major Histocompatibility Complex) molekulák: Ezek a glükoproteidek antigén peptideket mutatnak be a T-limfocitáknak, kulcsszerepet játszva az adaptív immunválaszban.
- Vércsoport antigének: Az ABO vércsoport antigének szénhidrátláncok, amelyek a vörösvértestek felszínén található glükoproteidekhez és glikolipidekhez kapcsolódnak. Ezek a glikánok határozzák meg a vércsoportot, és kritikusak a transzfúziós medicina szempontjából.
- CD markerek: Számos CD (Cluster of Differentiation) marker, amelyek a fehérvérsejtek azonosítására szolgálnak, glükoproteid természetű.
Extracelluláris mátrix (ECM) glükoproteidek
Az extracelluláris mátrix (ECM), a sejtek közötti térben található komplex hálózat, gazdag glükoproteidekben és proteoglikánokban. Ezek a molekulák strukturális támogatást nyújtanak, befolyásolják a sejt viselkedését, és részt vesznek a jelátvitelben.
- Kollagének: Bár a kollagén elsősorban egy fibrilláris fehérje, számos kollagén típus glikozilált, ami befolyásolja a fibrillák stabilitását és szerkezetét.
- Fibronektin: Ez a nagy glükoproteid kulcsszerepet játszik a sejtadhézióban, -migrációban és -differenciációban. Glikánjai befolyásolják a molekula kölcsönhatását az integrinekkel és más ECM komponensekkel.
- Laminin: A laminin egy másik nagy glükoproteid, amely a bazális membránok fő komponense. Fontos a sejtadhézióban, -differenciációban és a szöveti integritás fenntartásában.
- Proteoglikánok: Ezek a molekulák különleges glükoproteidek, amelyek nagyméretű glikozaminoglikán (GAG) láncokat tartalmaznak, amelyek kovalensen kapcsolódnak egy fehérje maghoz. Példák: aggrekán (porc), perlekán (bazális membrán), szindekánok (sejtmembrán). A proteoglikánok nagy mennyiségű vizet képesek megkötni, géleszerű mátrixot hozva létre, amely ellenáll a kompressziós erőknek.
Vérplazma glükoproteidek
A vérplazma tele van különböző funkciókat ellátó glükoproteidekkel. Ezek a molekulák részt vesznek a transzportban, immunitásban, véralvadásban és gyulladásos válaszokban.
- Antitestek (immunglobulinok): Az antitestek glükoproteidek, amelyek kulcsszerepet játszanak a humorális immunitásban. Glikozilációjuk befolyásolja az antitestek affinitását az antigénekhez, a komplement aktivációt és az antitest-függő sejtes citotoxicitást (ADCC).
- Transzportfehérjék: Számos transzportfehérje, mint például a transzferrin (vas), ceruloplazmin (réz) és alfa-1-antitripszin (proteáz inhibitor), glikozilált. A glikánok befolyásolhatják ezeknek a fehérjéknek a stabilitását és a clearance-ét a keringésből.
- Véralvadási faktorok: A véralvadási kaszkádban részt vevő számos faktor, például a protrombin és a faktor VIII, glükoproteid természetű. Glikozilációjuk elengedhetetlen a megfelelő működésükhöz és a véralvadás szabályozásához.
- Akut fázis fehérjék: Gyulladásos állapotokban a máj által termelt glükoproteidek, mint például a C-reaktív protein (CRP) vagy az alfa-1-savanyú glükoprotein, szintje megnő. Ezek a molekulák részt vesznek a gyulladásos válasz modulálásában.
Nyálka és szekrétumok
A mucinok nagy molekulatömegű, erősen glikozilált glükoproteidek, amelyek a nyálkahártyák fő komponensei. A légutakban, emésztőrendszerben, húgyutakban és a szemekben termelődnek, ahol védőréteget képeznek. Ez a viszkózus gélréteg véd a mechanikai sérülésektől, a patogénektől és a kémiai irritációtól. A mucinok O-glikoziláltak, és a szénhidrátláncok nagy száma adja a molekulák hidrofil jellegét és viszkoelasztikus tulajdonságait.
Vírusok és baktériumok glükoproteidjei
Nemcsak az eukarióta sejtek, hanem a patogén mikroorganizmusok is használnak glükoproteideket. Ezek gyakran kulcsszerepet játszanak a virulenciában, a gazdasejtek felismerésében és a fertőzés folyamatában.
- Vírusok: Számos vírus, például az influenza vírus (hemagglutinin és neuraminidáz) és a HIV (gp120 és gp41), a burkán lévő glükoproteidek segítségével tapad a gazdasejtekhez és jut be azokba. Ezek a glükoproteidek gyakran a vakcinafejlesztés célpontjai.
- Baktériumok: A baktériumok sejtfalában és felszínén is találhatók glükoproteidek, amelyek szerepet játszanak az adhézióban, a biofilm képzésben és az immunrendszer kijátszásában.
A glükoproteidek rendkívül széles körű előfordulása és sokfélesége aláhúzza alapvető fontosságukat a biológiai rendszerek működésében, a sejtszinttől az egész szervezet szintjéig.
A glükoproteidek sokrétű funkciói
A glükoproteidek nem csupán passzív molekulák, hanem aktív résztvevői szinte minden biológiai folyamatnak. Funkcióik rendkívül sokrétűek, a strukturális szerepektől kezdve a komplex jelátviteli útvonalak szabályozásáig. A glikánok sokfélesége és a fehérje maggal való kölcsönhatása teszi lehetővé ezt a széles spektrumú aktivitást.
Strukturális funkciók
Számos glükoproteid alapvető strukturális szerepet tölt be, hozzájárulva a sejtek és szövetek integritásához és stabilitásához.
- Sejtfal és extracelluláris mátrix (ECM): Az ECM-ben található glükoproteidek, mint például a kollagén, fibronektin és laminin, valamint a proteoglikánok, elengedhetetlenek a szövetek mechanikai ellenállásához és rugalmasságához. Ezek a molekulák hálózatot képeznek, amelyhez a sejtek tapadnak, és amely irányítja a sejtmigrációt, -növekedést és -differenciációt.
- Nyálkahártyák védelme: A mucinok, erősen glikozilált glükoproteidek, sűrű, viszkózus gélt képeznek a nyálkahártyák felületén. Ez a réteg fizikai akadályt képez a patogének, toxinok és mechanikai sérülések ellen, miközben hidratálja és védi a szöveteket.
Sejt-sejt felismerés és kommunikáció
Talán a glükoproteidek egyik legfontosabb funkciója a sejt-sejt felismerés és a kommunikáció. A glikánok egyedi mintázatai „azonosító kódként” működnek, amelyeket más sejtek specifikus receptorai (lektinek) felismernek.
- Immunválasz: Az immunrendszer glükoproteidek segítségével különbözteti meg a saját és az idegen sejteket. Az MHC molekulák bemutatják az antigéneket a T-sejteknek, míg a vércsoport antigének a vörösvértestek felszínén azonosítják a vércsoportot. Az antitestek maguk is glükoproteidek, amelyek specifikusan kötődnek az idegen antigénekhez.
- Fejlődésbiológia: A sejt-sejt felismerés elengedhetetlen a fejlődésbiológiai folyamatokban, mint például a sejtmigráció, a szöveti differenciáció és a szervfejlődés. A glükoproteidek irányítják a sejteket a megfelelő helyre, és biztosítják a megfelelő interakciókat a szövetek kialakulásához.
- Sejtadhézió: A sejtadhéziós molekulák (CAMs), mint például a szelektinek és integrinek, glikoziláltak, és lehetővé teszik a sejtek közötti és a sejtek ECM-hez való tapadását. Ez alapvető fontosságú a szövetek szerkezetének fenntartásához, a sebgyógyuláshoz és az immunsejtek mozgásához.
A glükoproteidek a sejtek nyelvét beszélik, lehetővé téve a komplex biológiai interakciókat és a szervezet harmonikus működését.
Receptor funkciók
Számos sejtmembránon lévő receptor glükoproteid természetű. Ezek a receptorok specifikusan felismernek és kötnek különböző jelzőmolekulákat, például hormonokat, növekedési faktorokat és neurotranszmittereket. A glikánok befolyásolhatják a receptor affinitását a ligandumhoz, a jelátvitel hatékonyságát és a receptor internalizációját.
Enzimaktivitás modulálása
Bizonyos enzimek glikoziláltak, és a glikánok befolyásolhatják az enzim stabilitását, oldhatóságát, szubsztrát-specifitását és aktivitását. A glikoziláció megvédheti az enzimet a proteolitikus lebontástól, vagy segíthet a megfelelő intracelluláris lokalizációjában.
Védelmi funkciók
A glükoproteidek kulcsszerepet játszanak a szervezet védelmi mechanizmusaiban.
- Immunrendszer: Az antitestek, a komplementrendszer komponensei és a sejtmembrán receptorok, amelyek felismerik a patogéneket, mind glükoproteidek.
- Patogén felismerés: A glükoproteidek a gazdasejtek felszínén gyakran szolgálnak belépési pontként vírusok és baktériumok számára. Ugyanakkor az immunrendszer is felismeri a patogének glükoproteidjeit, és célpontként használja őket az elpusztításukra.
Transzport funkciók
A vérplazmában számos transzport glükoproteid kering, amelyek specifikus molekulákat szállítanak a szervezetben. Ilyenek például a transzferrin (vas), a ceruloplazmin (réz) és az albuminszerű glükoproteidek.
Vércsoport antigének
Az ABO vércsoport antigének a vörösvértestek felszínén található glükoproteidek és glikolipidek szénhidrátláncai. Ezek a glikánok határozzák meg a vércsoportot, és elengedhetetlenek a biztonságos vérátömlesztéshez. A nem megfelelő vércsoportú vér transzfúziója súlyos immunreakciót válthat ki a recipiensben.
Immunitás és gyulladás
Az immunsejtek felszínén lévő glükoproteidek, mint például a szelektinek, elengedhetetlenek a gyulladásos válaszban. A szelektinek felismerik a gyulladt érfalon lévő szénhidrátligandumokat, lehetővé téve a fehérvérsejtek odatapadását és a gyulladás helyére történő migrációját. A citokinek és kemokinek, amelyek a gyulladásos válasz mediátorai, gyakran glikoziláltak, és glikánjaik befolyásolhatják stabilitásukat és receptor kötésüket.
Fejlődésbiológia
A glükoproteidek kritikus szerepet játszanak a sejtfejlődésben és differenciációban. A glikán mintázatok változásai irányítják a sejteket a megfelelő helyre, segítik a szövetek kialakulását és a szervek fejlődését. Például a neurális őssejtek differenciációját befolyásoló jelátviteli útvonalakban is részt vesznek glükoproteidek.
Patológiai szerep
A glükoproteidek diszfunkciója számos betegségben megfigyelhető, beleértve a rákot, autoimmun betegségeket, fertőző betegségeket és veleszületett anyagcsere-betegségeket (CDG). A glikozilációs mintázatok változásai gyakran betegségek biomarkereiként szolgálnak, és terápiás célpontokként is azonosíthatók.
A glükoproteidek rendkívüli funkcionális sokfélesége rávilágít arra, hogy a glikoziláció nem csupán egy poszttranszlációs módosítás, hanem egy alapvető mechanizmus, amely a biológiai komplexitás és a molekuláris információ átvitelének kulcsfontosságú eleme.
Glükoproteidek a betegségekben és a gyógyászatban
A glükoproteidek alapvető szerepe a normális fiziológiai folyamatokban azt is jelenti, hogy diszfunkciójuk számos betegség kialakulásában és progressziójában részt vesz. A glikozilációs mintázatok változásai, vagy a glikoproteidek kóros expressziója gyakran patológiai folyamatok jellemzői, ami diagnosztikai és terápiás lehetőségeket nyit meg.
Glükoproteidek a rákban
A rákos sejtek gyakran jelentősen megváltozott glikozilációs mintázatokat mutatnak a normális sejtekhez képest. Ezek a változások hozzájárulnak a tumor növekedéséhez, invazivitásához és metasztázisához.
- Tumor markerek: Számos glükoproteid szolgál tumor markerként, amelyek szintje emelkedik bizonyos rákos megbetegedések esetén. Példák:
- PSA (Prosztata Specifikus Antigén): Bár nem kizárólag prosztatarák specifikus, glikozilált glükoproteid, melynek szintje a prosztatarákban emelkedhet.
- CA-125 (Cancer Antigen 125): Petefészekrák és más nőgyógyászati rákok markere.
- CEA (Karcinoembrionális Antigén): Vastagbélrák és más emésztőrendszeri rákok markere.
- CA 19-9: Hasnyálmirigyrák és epeúti rákok markere.
Ezeknek a glükoproteideknek a glikozilációs állapota gyakran pontosabb diagnosztikai információt nyújthat, mint csupán a mennyiségük.
- Metasztázis: A rákos sejtek felszínén lévő glikánok változásai befolyásolják a sejtek adhézióját, migrációját és invazív képességét, elősegítve a metasztázis kialakulását. Például a szialinsavval dúsított glikánok gyakran összefüggésbe hozhatók a tumor progressziójával.
- Immunszupresszió: Egyes tumorsejtek olyan glükoproteideket expresszálnak, amelyek elnyomják az immunválaszt, segítve a tumort az immunrendszer kijátszásában.
Autoimmun betegségek
Az autoimmun betegségekben az immunrendszer tévesen támadja meg a szervezet saját szöveteit. A glükoproteidek ebben a folyamatban is szerepet játszhatnak:
- Autoantitestek: Bizonyos autoimmun betegségekben, mint például a rheumatoid arthritis, az autoantitestek (amelyek maguk is glükoproteidek) glikozilációs mintázata megváltozhat, ami befolyásolja gyulladáskeltő potenciáljukat.
- Saját antigének: A saját szövetek glükoproteidjei, mint például a thyroglobulin (pajzsmirigy betegségekben), autoantigénként működhetnek.
Fertőző betegségek
A patogének és a gazdasejtek közötti interakciókban a glükoproteidek kulcsszerepet játszanak:
- Vírusfertőzések: A vírusok, mint az influenza, HIV, SARS-CoV-2, glükoproteideket használnak a gazdasejtekhez való tapadáshoz és a bejutáshoz. Ezek a virális glükoproteidek a vakcinafejlesztés fő célpontjai. Az influenza vírus hemagglutininje a szialinsavhoz kötődik a gazdasejt felszínén.
- Bakteriális fertőzések: A baktériumok is használnak glükoproteideket (adhezineket) a gazdasejtekhez való tapadáshoz és a biofilm képzéshez. A gazdasejt felszínén lévő glükoproteidek pedig receptorokként szolgálhatnak a baktériumok számára.
Veleszületett glikozilációs zavarok (CDG)
A veleszületett glikozilációs zavarok (CDG) egy ritka genetikai betegségcsoport, amelyben a glikoziláció folyamatában részt vevő enzimek vagy transzporterek hibásak. Ezek a hibák a glikoproteidek és glikolipidek hibás glikozilációjához vezetnek, ami sokféle tünetet okozhat, a neurológiai problémáktól kezdve a fejlődési rendellenességekig és a belső szervek diszfunkciójáig. A diagnózis a glikoproteidek (pl. transzferrin) izoelektromos fókuszálásával történik, amely kimutatja a glikán láncok hiányát.
Klinikai diagnosztika és terápia
A glükoproteidek nemcsak betegségmarkerek, hanem diagnosztikai és terápiás célpontok is:
- Diagnosztikai markerek: A fent említett tumor markerek mellett más glükoproteidek is használhatók diagnosztikában. Például a CRP (C-reaktív protein), egy akut fázis glükoproteid, a gyulladásos állapotok és fertőzések általános markere.
- Gyógyszerfejlesztés:
- Rekombináns glükoproteidek: Számos modern gyógyszer rekombináns úton előállított glükoproteid. Például az eritropoetin (EPO), amely a vörösvértest-termelést stimulálja, glikozilált. A glikoziláció befolyásolja az EPO biológiai aktivitását és a keringésben való élettartamát. Hasonlóképpen, a rekombináns antitestek (monoklonális antitestek) glikozilációja is kulcsfontosságú a terápiás hatékonyságuk szempontjából.
- Vakcinák: Sok vakcina virális glükoproteideket használ antigénként az immunválasz kiváltására (pl. influenza, HPV vakcinák).
- Antivirális szerek: Néhány antivirális gyógyszer a virális glükoproteidek működését gátolja, megakadályozva a vírus bejutását a sejtekbe vagy a szaporodását. Például az influenza elleni gyógyszerek, mint a zanamivir és az oszeltamivir, a neuraminidáz (egy virális glükoproteid) aktivitását gátolják.
- Glikánterápia: A glikozilációs zavarok kezelésére új megközelítések, az úgynevezett glikánterápiák fejlődnek. Ezek magukban foglalhatják a hiányzó monoszacharidok pótlását, az enzimaktivitás modulálását vagy a glikozilációs útvonalak genetikai korrekcióját.
- Célzott gyógyszerszállítás: A glikánok felhasználhatók gyógyszerek célzott szállítására is. Bizonyos glikán mintázatokat felismerő receptorok expresszálódnak specifikus sejttípusokon (pl. tumorsejteken), lehetővé téve a gyógyszerek szelektív eljuttatását a beteg sejtekhez, csökkentve a mellékhatásokat.
Az alábbi táblázat néhány fontos glükoproteidet és azok klinikai relevanciáját mutatja be:
| Glükoproteid | Fő funkció | Klinikai relevancia |
|---|---|---|
| Inzulin receptor | Inzulin kötés, glükóz metabolizmus | 2-es típusú cukorbetegség, inzulin rezisztencia |
| MHC molekulák | Antigén prezentáció | Autoimmun betegségek, transzplantációs immunológia |
| Antitestek (IgG) | Immunválasz, patogének semlegesítése | Autoimmun betegségek, immundeficienciák, monoklonális antitest terápiák |
| PSA | Prosztata funkció, proteáz | Prosztatarák biomarker |
| CA-125 | Sejtadhézió, jelátvitel | Petefészekrák biomarker |
| Eritropoetin (EPO) | Vörösvértest-termelés stimulálása | Anémia kezelése (rekombináns EPO) |
| Faktor VIII | Véralvadás | Hemofília A (rekombináns Faktor VIII) |
| Hemagglutinin (influenza) | Vírus bejutás a sejtbe | Influenza vakcinák, antivirális szerek célpontja |
| MUC1 (mucin) | Nyálkahártya védelem | Rák (túl-expresszió tumorsejteken), cisztás fibrózis |
| Transzferrin | Vas transzport | Veleszületett glikozilációs zavarok (CDG diagnózis) |
A glükoproteidek és glikánjaik kutatása egyre inkább a modern orvostudomány fókuszába kerül. A glikánok komplexitásának feltárása új diagnosztikai eszközökhöz, hatékonyabb gyógyszerekhez és célzott terápiákhoz vezethet számos betegség, különösen a rák és a fertőző betegségek kezelésében.
Jövőbeli perspektívák és kutatási irányok a glükoproteidek világában
A glükoproteidek és a glikoziláció kutatása az elmúlt évtizedekben hatalmas fejlődésen ment keresztül, de a terület még mindig tele van feltáratlan lehetőségekkel. A glikomika, a glikánok és glikoproteidek teljes készletének (glikom) tanulmányozása, egyre inkább a biológiai kutatás élvonalába kerül, ígéretes utakat nyitva meg a diagnosztika és a terápia számára.
A glikomika és a glikoinformatika fejlődése
A glikomika célja a glikánok és glikoproteidek teljes spektrumának azonosítása, jellemzése és funkcionális elemzése egy adott biológiai rendszerben. Ez rendkívül komplex feladat, mivel a glikánok szerkezeti sokfélesége messze meghaladja a fehérjék vagy nukleinsavak sokféleségét. Az új technológiai áttörések, mint a nagy felbontású tömegspektrometria, a speciális kromatográfiás módszerek és az NMR spektroszkópia, lehetővé teszik a glikánok egyre pontosabb azonosítását és kvantifikálását.
A glikoinformatika a glikomikai adatok tárolására, elemzésére és értelmezésére szolgáló számítógépes eszközök és adatbázisok fejlesztésével foglalkozik. A glikán szerkezetek komplexitása miatt speciális algoritmusokra és adatbázisokra van szükség ezen adatok hatékony kezeléséhez és a biológiai mintázatok felismeréséhez.
Új terápiás célpontok azonosítása
A glükoproteidek és a glikozilációs enzimek egyre inkább a gyógyszerfejlesztés fókuszába kerülnek. Mivel a glikozilációs mintázatok gyakran megváltoznak betegségek, például rák vagy fertőzések esetén, ezek a módosult glikánok vagy az őket létrehozó enzimek specifikus célpontként szolgálhatnak.
- Rákellenes terápiák: A rákos sejteken expresszálódó aberráns glikánok ellen irányuló antitestek vagy a tumorsejtek glikozilációját moduláló kis molekulák fejlesztése ígéretes. Cél lehet az onkogén glikoziltranszferázok gátlása, vagy olyan lektinek alkalmazása, amelyek szelektíven megkötik a tumorsejteket.
- Fertőző betegségek: A patogének (vírusok, baktériumok, paraziták) glükoproteidjeinek vagy a gazdasejt glikánjaihoz való kötődésük gátlása új antivirális vagy antibakteriális stratégiákat kínálhat. A virális glikoproteidekre specifikus antitestek vagy a glikán-kötőhelyeket blokkoló molekulák fejlesztése folyamatban van.
- Autoimmun és gyulladásos betegségek: A glikozilációs mintázatok modulálásával befolyásolható az immunválasz, csökkenthető a gyulladás, vagy korrigálhatók az autoimmun folyamatok.
Diagnosztikai eszközök fejlesztése
A glükoproteidek és a glikánok, mint biomarkerek, potenciálisan sokkal specifikusabb és érzékenyebb diagnosztikai eszközöket biztosíthatnak, mint a jelenleg használt markerek. A glikozilációs mintázatok finom változásai korai stádiumú betegségeket jelezhetnek, vagy segíthetnek a betegségek progressziójának nyomon követésében és a terápia hatékonyságának monitorozásában.
- Folyékony biopszia: A vérben vagy más testnedvekben keringő glükoproteidek, vagy akár a tumorsejtekből származó glikozilált vezikulák (exoszómák) elemzése lehetővé teheti a rák és más betegségek non-invazív diagnózisát és monitorozását.
- Személyre szabott orvoslás: A beteg egyedi glikozilációs profiljának feltérképezése segíthet a személyre szabott terápiák kiválasztásában, figyelembe véve a beteg genetikai hátterét és a betegség specifikus glikán mintázatait.
Glikomérnökség és biológiai gyógyszerek
A glikomérnökség a sejt glikozilációs útvonalainak szándékos módosítását jelenti, hogy a kívánt glikán szerkezettel rendelkező glükoproteideket állítsanak elő. Ez különösen fontos a rekombináns fehérjék, például a monoklonális antitestek vagy terápiás enzimek gyártása során.
- Optimalizált biológiai gyógyszerek: A glikán profil precíz szabályozásával javítható a gyógyszerek hatékonysága, stabilitása, oldhatósága és immunogenitása. Például a rekombináns antitestek glikozilációjának módosításával növelhető az Fc-réceptorhoz való affinitás, ami fokozza az antitest-függő sejtes citotoxicitást (ADCC).
- Új terápiás molekulák: A glikomérnökség lehetővé teheti teljesen új glükoproteid alapú terápiás molekulák tervezését és előállítását, amelyek specifikus glikán-ligandum interakciókon keresztül fejtik ki hatásukat.
A glükoproteidek és a glikoziláció kutatása a biológia egyik legdinamikusabban fejlődő területe. A glikánok rejtett nyelvének megfejtése nemcsak alapvető biológiai ismereteinket bővíti, hanem forradalmasíthatja a betegségek diagnózisát, megelőzését és kezelését, új távlatokat nyitva a gyógyászatban.