A szerves kémia lenyűgöző világában számos vegyület létezik, amelyek szerkezete és tulajdonságai alapvető fontosságúak a tudomány és az ipar számára. Ezek közül az egyik figyelemre méltó molekula a dibenzoil, más néven benzil. Ez a vegyület egy speciális diketon, amely két fenilcsoportot és két karbonilcsoportot tartalmaz, egyedi kémiai viselkedést és széles körű alkalmazási lehetőségeket biztosítva számára. A dibenzoil nem csupán egy kémiai kuriózum; a polimeriparban, a gyógyszeriparban és a laboratóriumi szintézisekben is kulcsszerepet játszik.
A dibenzoil molekuláris felépítése és elektronikus konfigurációja adja meg jellegzetes fizikai és kémiai tulajdonságait. Megértése elengedhetetlen a szerves reakciómechanizmusok, a fotokémia és a komplex vegyületek szintézisének tanulmányozásához. Különösen érdekes a benzilsav átrendeződés, amely a dibenzoil jellegzetes reakciója, és betekintést nyújt a molekuláris átalakulások mélyebb mechanizmusaiba. Cikkünkben részletesen vizsgáljuk meg a dibenzoil kémiai képletét, szerkezetét, fizikai és kémiai tulajdonságait, előállítási módjait, valamint legfontosabb ipari és tudományos alkalmazásait.
A dibenzoil kémiai képlete és molekulaszerkezete
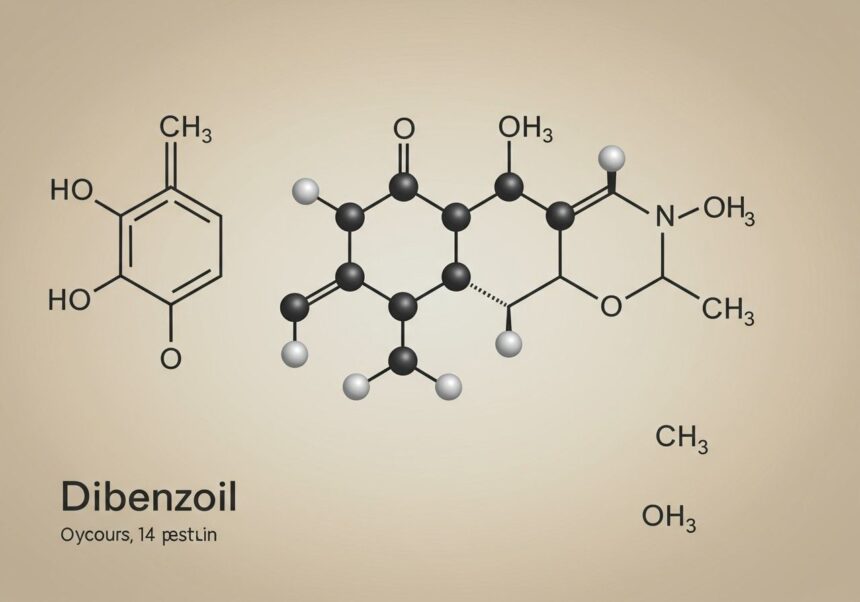
A dibenzoil, vagy más néven benzil, molekulaképlete C14H10O2. Ez a képlet árulkodik a vegyület elemi összetételéről: tizennégy szénatomot, tíz hidrogénatomot és két oxigénatomot tartalmaz. A molekulaszerkezet mélyebb vizsgálata azonban feltárja a dibenzoil egyedi jellemzőit és funkcionális csoportjait, amelyek alapvetően befolyásolják kémiai viselkedését.
Szerkezetileg a dibenzoil egy diketon, ami azt jelenti, hogy két ketoncsoportot tartalmaz a molekulájában. Ezek a ketoncsoportok közvetlenül kapcsolódnak egymáshoz, és mindegyikhez egy-egy fenilgyűrű (C6H5) kapcsolódik. A teljes szerkezet így írható le: C6H5–CO–CO–C6H5. Ez a szimmetrikus elrendezés kulcsfontosságú a vegyület stabilitása és reaktivitása szempontjából.
A két karbonilcsoport (C=O) szénatomjai sp2 hibridizáltak, ami sík háromszöges geometriát eredményez körülöttük. Az oxigénatomok elektronnegativitása miatt a karbonilcsoportok polárisak, a szénatomok parciális pozitív töltést hordoznak, míg az oxigénatomok parciális negatív töltést. Ez a polaritás teszi a karbonilcsoportokat érzékennyé a nukleofil támadásokra, ami számos kémiai reakció alapját képezi.
A két fenilgyűrű, amelyek aromás rendszerek, konjugált pi-elektron rendszert képeznek, ami stabilitást kölcsönöz a molekulának. A fenilgyűrűk sík struktúrája és a delokalizált elektronok befolyásolják a dibenzoil spektroszkópiai tulajdonságait és reaktivitását is. A fenilgyűrűk és a diketon rész közötti konjugáció kiterjedhet, ami további elektronikus hatásokhoz vezethet.
Érdekes szempont a dibenzoil konformációja. A két karbonilcsoport közötti C-C kötés körül elfordulás lehetséges, ami különböző térbeli elrendezéseket eredményezhet. A szilárd fázisban a dibenzoil leggyakrabban transz-konformációt vesz fel, ahol a két fenilgyűrű a C-C kötés két oldalán helyezkedik el. Azonban oldatban vagy gázfázisban más konformációk, például cisz-konformációk is előfordulhatnak, bár ezek kevésbé stabilak a szterikus gátlás miatt. A konformációs szabadság befolyásolhatja a vegyület reakciókészségét és kölcsönhatásait más molekulákkal.
A dibenzoil szerkezetének megértése alapvető fontosságú a kémiai reakciók előrejelzéséhez és a vegyület alkalmazásainak optimalizálásához. A diketon jelleg, az aromás fenilgyűrűk, a karbonilcsoportok polaritása és a konformációs lehetőségek mind hozzájárulnak ahhoz, hogy a dibenzoil egy sokoldalú és jelentős molekula legyen a szerves kémiában.
„A dibenzoil szerkezete kiváló példa arra, hogyan befolyásolja a molekuláris geometria és a funkcionális csoportok elrendezése egy vegyület kémiai identitását és felhasználási lehetőségeit.”
A dibenzoil fizikai tulajdonságai
A dibenzoil számos jellegzetes fizikai tulajdonsággal rendelkezik, amelyek hozzájárulnak az azonosításához és ipari alkalmazásaihoz. Ezek a tulajdonságok a molekulaszerkezetből és az intermolekuláris kölcsönhatásokból fakadnak, és alapvetőek a vegyület laboratóriumi és ipari kezeléséhez.
A dibenzoil szobahőmérsékleten szilárd anyag, jellemzően sárga színű kristályos por formájában található meg. Ennek a sárga színnek az oka a molekulában lévő kiterjedt konjugált pi-elektronrendszer, amely elnyeli a spektrum kék tartományát, és a sárga színt engedi át. A szaga enyhén aromás, kellemes.
A vegyület olvadáspontja viszonylag magas, körülbelül 94-96 °C. Ez a viszonylag magas olvadáspont a molekulák közötti erős London-diszperziós erőknek és a dipólus-dipólus kölcsönhatásoknak köszönhető, amelyek a poláris karbonilcsoportok miatt jönnek létre. A forráspontja is magas, körülbelül 346 °C, ami jól mutatja a molekulák közötti jelentős kohéziós erőket.
A dibenzoil sűrűsége körülbelül 1,23 g/cm³ szobahőmérsékleten. Ez az érték tipikusnak mondható a hasonló méretű szerves vegyületek esetében. A molekulatömege 210,23 g/mol, ami a C14H10O2 képletből számítható ki.
Oldhatóságát tekintve a dibenzoil vízben alig oldódik, ami a molekula nagyméretű, apoláris fenilgyűrűinek köszönhető. Ezzel szemben jól oldódik számos szerves oldószerben, mint például etanolban, éterben, benzolban, toluolban, acetonban, kloroformban és ecetsavban. Ez a szelektív oldhatóság hasznos a vegyület tisztításánál és reakciók végrehajtásánál.
A dibenzoil spektroszkópiai tulajdonságai szintén fontosak az azonosítás és a szerkezetmeghatározás szempontjából. Az UV-Vis spektrumban jellemző elnyelési maximumokat mutat a kiterjedt konjugált rendszer miatt, általában 250 nm és 380 nm körül. Az infravörös (IR) spektrumban a karbonilcsoportok erős elnyelést mutatnak körülbelül 1660-1680 cm-1 tartományban, ami a ketonokra jellemző. A NMR spektrum (1H NMR és 13C NMR) részletes információt szolgáltat a hidrogén- és szénatomok környezetéről, megerősítve a két fenilgyűrű és a két karbonilcsoport jelenlétét.
Ezek a fizikai paraméterek kritikusak a dibenzoil laboratóriumi kezelésében, például a kristályosításos tisztítás során, vagy ipari folyamatok tervezésekor, ahol az oldhatóság és a fázisátmenetek pontos ismerete elengedhetetlen a hatékony gyártáshoz és feldolgozáshoz.
| Tulajdonság | Érték |
|---|---|
| Molekulaképlet | C14H10O2 |
| Molekulatömeg | 210,23 g/mol |
| Halmazállapot (szobahőmérsékleten) | Szilárd (sárga kristályos por) |
| Olvadáspont | 94-96 °C |
| Forráspont | 346 °C |
| Sűrűség | 1,23 g/cm³ |
| Oldhatóság vízben | Alig oldódik |
| Oldhatóság szerves oldószerekben | Jól oldódik (etanol, éter, benzol, aceton, kloroform) |
A dibenzoil kémiai tulajdonságai és reakciói
A dibenzoil kémiai viselkedését alapvetően a két, egymással közvetlenül összekapcsolódó karbonilcsoport és a hozzájuk kapcsolódó aromás fenilgyűrűk határozzák meg. Ezek a strukturális jellemzők teszik a dibenzoilt rendkívül sokoldalúvá a szerves szintézisben és számos egyedi reakcióra képessé.
Ketonokra jellemző reakciók
Mint diketon, a dibenzoil részt vesz a ketonokra jellemző reakciókban, bár a két karbonilcsoport jelenléte és a szomszédos fenilgyűrűk némileg módosíthatják a reaktivitást.
- Nukleofil addíció: A karbonil szénatom parciális pozitív töltése miatt a dibenzoil érzékeny a nukleofil támadásokra.
- Grignard-reagenssel való reakció: Alkohollá redukálódik, majd további Grignard-reagenssel tercier alkoholt képezhet.
- Hidrogén-cianid addíció: Cianohidrint képezhet.
- Alkoholokkal való reakció: Savkatalízis mellett acetálokat vagy félacetálokat képezhet, különösen diolok jelenlétében, gyűrűs acetálokat eredményezve.
- Aminokkal való reakció: Imin képződéséhez vezethet, bár a diketon jelleg miatt bonyolultabb termékek, például pirazin-származékok is keletkezhetnek.
- Redukció: A karbonilcsoportok redukálhatók alkoholokká.
- Hidrogénezés: Katalizátor (pl. palládium, platina, nikkel) jelenlétében hidrogénnel redukálva diolokat képezhet.
- Fémhidridekkel (pl. LiAlH4, NaBH4): Szelektíven redukálhatók a karbonilcsoportok, diolokat eredményezve. A redukció mértéke és szelektivitása a reagens erősségétől függ.
- Oxidáció: Bár a ketonok általában ellenállóbbak az oxidációval szemben, mint az aldehidek, erős oxidálószerekkel (pl. hidrogén-peroxid) a dibenzoil is oxidálható, általában a C-C kötés felhasadásával.
Speciális reakciók és átrendeződések
A dibenzoil igazi kémiai jelentősége azonban a diketon szerkezetéből fakadó egyedi reakcióiban rejlik.
A benzilsav átrendeződés
A benzilsav átrendeződés (benzilic acid rearrangement) a dibenzoil egyik legfontosabb és legjellegzetesebb reakciója. Ez egy báziskatalizált intramolekuláris átrendeződés, amelynek során a dibenzoilból alfa-hidroxi-karbonsav, a benzilsav keletkezik. A reakció mechanizmusa a következő:
- Nukleofil támadás: Egy erős bázis, például hidroxidion (OH–) nukleofil támadást intéz az egyik karbonil szénatom ellen. Ez egy tetraéderes intermediert hoz létre.
- Elektronátrendeződés és fenilcsoport migráció: Az oxigénatomon lévő negatív töltés rezonanciával stabilizálódik. Ezután az egyik karbonil szénatomhoz kapcsolódó fenilcsoport (Ph) elvándorol a szomszédos, másik karbonil szénatomhoz, miközben az oxigénatomhoz kapcsolódó hidrogénatom protont ad le a bázisnak, vagy egy másik molekulának. Ez a migráció a C-C kötés átrendeződésével és a másik karbonilcsoport anionos formába történő átalakulásával jár.
- Protonálás: A keletkezett karboxilát anion protonálódik (általában a reakcióelegy savanyításával), így létrejön a végső termék, a benzilsav.
Ez az átrendeződés nem csak a dibenzoilra jellemző, hanem más alfa-diketonokra is, és fontos módszer alfa-hidroxi-karbonsavak szintézisére. A reakció mechanizmusa rávilágít a molekulákban zajló komplex elektronikus és szterikus hatásokra.
„A benzilsav átrendeződés nem csupán egy kémiai átalakulás, hanem egy elegáns bizonyítéka a molekuláris szintű elektronvándorlás és a szerkezeti stabilitás kölcsönhatásának.”
Fotokémiai reakciók
A dibenzoil rendkívül fontos fotokémiai iniciátorként. Fény hatására (különösen UV fényre) a dibenzoil molekula gerjesztett állapotba kerül. A gerjesztett dibenzoil képes hidrogénatomot elvonni más molekuláktól, vagy a C-C kötés felhasadásával gyököket képezni. Ezek a gyökök aztán elindíthatják a polimerizációs reakciókat, különösen vinilmonomerek esetében. Ez a tulajdonság teszi a dibenzoilt kulcsfontosságúvá a fényre keményedő gyanták és bevonatok technológiájában.
Komplexképződés
A dibenzoil, mint diketon, képes fémionokkal kelátkomplexeket képezni. A két karbonil oxigénatom ligandumként működhet, stabil öttagú vagy hattagú gyűrűket alkotva a fémionnal. Ez a tulajdonság felhasználható fémionok kimutatására, elválasztására, vagy akár katalizátorok előállítására.
Összességében a dibenzoil kémiai tulajdonságai a ketonokra jellemző reaktivitás és a diketon szerkezetéből fakadó egyedi reakciók (mint a benzilsav átrendeződés és a fotokémiai gyökképződés) izgalmas kombinációját mutatják be. Ez a sokoldalúság teszi a vegyületet értékes reagenssé és ipari anyaggá.
A dibenzoil előállítása és szintézise
A dibenzoil előállítása számos módon lehetséges, mind laboratóriumi, mind ipari léptékben. A szintézis módjának kiválasztása gyakran a kívánt tisztasági foktól, a hozamtól és a költséghatékonyságtól függ. A leggyakoribb és leghatékonyabb módszerek általában a benzoin vegyület oxidációján alapulnak.
Benzoin oxidációja
A dibenzoil ipari és laboratóriumi előállításának legelterjedtebb kiindulási anyaga a benzoin (C6H5–CH(OH)–CO–C6H5), amely egy alfa-hidroxi-keton. A benzoin oxidációjával a hidroxilcsoportot és a hidrogénatomot távolítják el a karbonilcsoport melletti szénatomról, így alakul ki a második karbonilcsoport.
Többféle oxidálószer is alkalmazható erre a célra:
- Salétromsavas oxidáció: Ez az egyik legrégebbi és leggyakoribb laboratóriumi módszer. A benzoint híg salétromsavval (HNO3) melegítve a benzoin oxidálódik dibenzoillá, miközben a salétromsav redukálódik nitrogén-oxidokká (pl. NO2). A reakció viszonylag egyszerű és jó hozamot biztosít.
A reakció során a salétromsav nemcsak oxidálószerként, hanem katalizátorként is működhet, elősegítve a benzoin enolizációját, ami az oxidáció kulcsfontosságú lépése.
- Réz(II)-acetáttal történő oxidáció: Réz(II)-acetát (Cu(CH3COO)2) piridin jelenlétében is hatékonyan oxidálja a benzoint dibenzoillá. Ez a módszer gyakran enyhébb körülményeket igényel, és szelektívebb lehet. A réz(II) ion oxidálószerként működik, miközben réz(I) ionná redukálódik.
- Vas(III)-kloriddal történő oxidáció: Hasonlóan a réz(II)-acetáthoz, vas(III)-klorid (FeCl3) is felhasználható a benzoin dibenzoillá történő oxidálására. Az Fe3+ ion oxidálja a benzoint, miközben Fe2+ ionná redukálódik. Ez a módszer szintén jó hozamot adhat.
- Dimerkaptánok vagy más oxidálószerek: Kutatási és speciális alkalmazások során más oxidálószereket, például dimetilszulfoxidot (DMSO) vagy egyéb szerves oxidálószereket is alkalmazhatnak, amelyek specifikus körülmények között előnyösebbek lehetnek.
- Levegővel vagy oxigénnel történő oxidáció: Bizonyos esetekben, megfelelő katalizátorok (pl. kobalt-származékok) jelenlétében, a benzoin levegővel vagy tiszta oxigénnel is oxidálható dibenzoillá. Ez a környezetbarátabb módszer ipari szempontból is vonzó lehet, mivel elkerüli a toxikus oxidálószerek használatát.
A szintézis lépései és tisztítása
A dibenzoil szintézise során a kiindulási anyag, a benzoin, általában benzaldehidből állítható elő benzoin kondenzációval. Ez a kétlépcsős folyamat – benzaldehidből benzoin, majd benzoinból dibenzoil – biztosítja a dibenzoil előállításának teljes útvonalát.
A reakció befejezése után a dibenzoilt általában kristályosítással tisztítják. Ez magában foglalja a termék feloldását egy megfelelő forró oldószerben (pl. etanol), majd a lassú hűtést, ami a tiszta dibenzoil kristályok kiválását eredményezi. A kristályokat szűréssel választják el, majd szárítják. Ez a tisztítási lépés elengedhetetlen a magas tisztaságú termék előállításához, különösen olyan alkalmazások esetén, ahol a szennyeződések károsak lehetnek, például fotopolimerizációs iniciátorként.
Az előállítási módszerek változatossága lehetővé teszi a dibenzoil termelését a laboratóriumi kísérletektől az ipari méretű gyártásig, figyelembe véve a költségeket, a környezeti hatásokat és a termékminőségi követelményeket.
A dibenzoil alkalmazásai
A dibenzoil sokoldalú vegyület, amely egyedi kémiai és fotokémiai tulajdonságainak köszönhetően számos ipari és tudományos területen talál alkalmazást. Legfontosabb felhasználási területei közé tartozik a polimeripar, a gyógyszeripar, a festékipar és a kémiai szintézis.
1. Fotopolimerizációs iniciátor
A dibenzoil egyik legjelentősebb és legelterjedtebb alkalmazása a fotopolimerizáció iniciátoraként való felhasználása. A fotopolimerizáció egy olyan folyamat, amely során monomerek polimerekké alakulnak fény (általában UV fény) hatására. A dibenzoil ebben a folyamatban kulcsszerepet játszik, mivel a fényenergia hatására szabadgyököket képez, amelyek elindítják a polimerizációs láncreakciót.
Hogyan működik? A dibenzoil molekula UV fény elnyelésekor gerjesztett állapotba kerül. Ebben a gerjesztett állapotban a molekula képes hidrogénatomot elvonni egy másik molekulától (pl. egy monomertől vagy egy additívtől), vagy homolitikusan felhasad a két karbonilcsoport közötti C-C kötésnél, így két benzilgyököt képezve. Ezek a rendkívül reaktív szabadgyökök aztán megtámadják a monomerek kettős kötéseit, elindítva a polimerizációs láncot. Ez a mechanizmus rendkívül hatékony és gyors polimerizációt tesz lehetővé.
Alkalmazási területei ebben a szegmensben rendkívül szélesek:
- Fényre keményedő gyanták és bevonatok: Fogászati tömőanyagok, körömlakkok, optikai lencsék bevonatai, nyomdafestékek, ragasztók és védőbevonatok gyártásában használják. Ezek a termékek gyorsan és hatékonyan keményednek meg UV fény hatására, ami jelentős előnyt jelent a gyártási folyamatokban.
- 3D nyomtatás: Az SLA (Stereolithography Apparatus) és DLP (Digital Light Processing) alapú 3D nyomtatási technológiákban a dibenzoil és hasonló fotoiniciátorok kulcsfontosságúak a folyékony gyanta rétegenkénti megkeményítéséhez lézer vagy projektor segítségével.
- Elektronikai ipar: Fotoreziszt anyagokban, amelyek a mikroelektronikai áramkörök gyártásában nélkülözhetetlenek. A dibenzoil segít a finom mintázatok kialakításában a félvezető chipeken.
2. Gyógyszeripar és gyógyászat
Bár nem közvetlenül gyógyszerként alkalmazzák, a dibenzoil fontos intermedier és reagens a gyógyszerhatóanyagok szintézisében. A benzilsav átrendeződés például egy olyan reakció, amely alfa-hidroxi-karbonsavakat eredményez, amelyek számos gyógyszer molekuláris vázának részét képezhetik. Emellett kutatások folynak a dibenzoil és származékainak potenciális biológiai aktivitásának feltárására, például antimikrobiális vagy tumorellenes hatások tekintetében, bár ez még a kutatás korai szakaszában van.
3. Festékipar és pigmentek
A dibenzoil és származékai felhasználhatók színezékek és pigmentek előállítására. A molekula kiterjedt konjugált rendszere, amely felelős a sárga színéért, módosítható úgy, hogy más színű vegyületeket hozzon létre. Ezenkívül a fotokémiai tulajdonságait kihasználva bizonyos festékek és bevonatok UV-keményedő rendszereiben is szerepet kaphat.
4. Kémiai szintézis és reagens
A dibenzoil értékes reagens a szerves kémiában. A fent említett benzilsav átrendeződésen kívül más reakciókban is részt vesz, amelyek új szén-szén kötések kialakításához vagy komplex molekulák szintéziséhez vezetnek. Alkalmazzák heterociklusos vegyületek, például pirazinok és imidazolszármazékok szintézisében is, amelyek számos biológiailag aktív molekula vázát képezik.
5. Kutatás és oktatás
A dibenzoil, mint modellvegyület, fontos szerepet játszik a fotokémiai kutatásokban, a gyökös reakciók mechanizmusának tanulmányozásában és a polimerizációs folyamatok megértésében. Az egyetemi laboratóriumokban gyakran használják demonstrációs célokra a benzilsav átrendeződés bemutatására, ami egy klasszikus reakciómechanizmus a szerves kémiában. Ezáltal hozzájárul a jövő vegyészeinek képzéséhez.
Összefoglalva, a dibenzoil sokoldalú vegyület, amelynek alkalmazási köre a modern ipar számos szektorát lefedi. A fotokémiai iniciátorként betöltött szerepe különösen kiemelkedő, de a kémiai szintézisben és a gyógyszerkutatásban is jelentős potenciállal rendelkezik. A vegyület iránti érdeklődés folyamatos, és a jövőben további innovatív alkalmazások megjelenése várható.
A dibenzoil biztonságos kezelése és környezeti hatásai
Mint minden kémiai vegyület esetében, a dibenzoil kezelése során is be kell tartani bizonyos biztonsági előírásokat a felhasználók és a környezet védelme érdekében. Bár a dibenzoil nem tartozik a rendkívül veszélyes anyagok közé, megfelelő óvintézkedésekre van szükség.
Biztonsági előírások és kezelés
- Személyi védőfelszerelés (PPE): A dibenzoillal való munka során mindig viseljen védőszemüveget vagy arcvédőt, kémiai kesztyűt (pl. nitril vagy latex), valamint laboratóriumi köpenyt, hogy elkerülje a bőrrel és szemmel való közvetlen érintkezést.
- Belélegzés: A dibenzoil por formájában irritálhatja a légutakat. Porral való munka során (pl. mérés, átöntés) ajánlott elszívó fülke (digesztor) használata, és szükség esetén megfelelő légzésvédő maszk viselése.
- Bőrrel való érintkezés: Bár a dibenzoil nem okoz súlyos bőrirritációt, tartós érintkezés esetén enyhe irritáció előfordulhat. Érintkezés esetén az érintett területet bő vízzel és szappannal azonnal le kell mosni.
- Lenyelés: A lenyelés kerülendő. Ha véletlenül lenyelésre kerül, azonnal orvosi segítséget kell kérni.
- Tűzveszély: A dibenzoil éghető szilárd anyag. Tűz esetén szén-dioxiddal, száraz vegyi anyaggal vagy vízzel oltóanyaggal oltható. Tárolása során távol kell tartani nyílt lángtól, hőforrásoktól és gyújtóforrásoktól.
- Tárolás: A dibenzoilt hűvös, száraz, jól szellőző helyen, szorosan lezárt edényben kell tárolni, közvetlen napfénytől védve. Kerülni kell az erős oxidálószerekkel, savakkal és bázisokkal való érintkezést, mivel ezek reakcióba léphetnek vele.
Fontos, hogy a vegyület biztonsági adatlapját (SDS) mindig elolvassuk és betartsuk az abban foglalt utasításokat a dibenzoil kezelése előtt.
Környezeti hatások
A dibenzoil környezeti hatásait tekintve fontos megjegyezni, hogy nem tekinthető rendkívül toxikus anyagnak. Azonban, mint minden kémiai anyag, nem szabad ellenőrizetlenül a környezetbe engedni.
- Vízbe kerülés: Vízben való rossz oldhatósága miatt nem jelent azonnali, súlyos vízszennyezési kockázatot, de nagy mennyiségben a vízi élővilágra káros lehet. A szennyvízbe juttatása tilos.
- Talajba kerülés: A talajban lassan bomlik le. A talajszennyezés elkerülése érdekében gondoskodni kell a megfelelő tárolásról és a hulladékkezelésről.
- Levegőbe kerülés: Por formájában a levegőbe kerülve, belélegezve irritációt okozhat. A kibocsátás minimalizálása érdekében megfelelő elszívó rendszereket kell alkalmazni.
- Hulladékkezelés: A dibenzoil tartalmú hulladékokat a helyi előírásoknak megfelelően, veszélyes hulladékként kell kezelni és ártalmatlanítani. Égetéssel történő ártalmatlanítás esetén biztosítani kell a teljes égést, hogy elkerüljék a káros égéstermékek kibocsátását.
A felelős kémiai gyakorlatok és a környezetvédelmi előírások betartása elengedhetetlen a dibenzoil biztonságos és fenntartható felhasználásához. A kockázatok minimalizálásával és a tudatos kezeléssel a dibenzoil továbbra is értékes vegyület maradhat az ipar és a kutatás számára, anélkül, hogy jelentős veszélyt jelentene az emberi egészségre vagy a környezetre.
Összehasonlítás hasonló vegyületekkel: benzoin és más diketonok
A dibenzoil helyének jobb megértéséhez a szerves kémiában érdemes összehasonlítani hasonló szerkezetű vegyületekkel, különösen a benzoinnal, amely a dibenzoil előállításának kulcsfontosságú intermedierje, valamint más diketonokkal.
Dibenzoil vs. Benzoin
A dibenzoil (Ph–CO–CO–Ph) és a benzoin (Ph–CH(OH)–CO–Ph) szerkezete rendkívül hasonló, de egy alapvető különbség választja el őket: a benzoin egy alfa-hidroxi-keton, míg a dibenzoil egy alfa-diketon. Ez a különbség alapvetően befolyásolja a két vegyület fizikai és kémiai tulajdonságait.
- Funkcionális csoportok:
- Benzoin: Tartalmaz egy hidroxilcsoportot (-OH) és egy ketoncsoportot (-CO-) egymás mellett. A hidroxilcsoport jelenléte lehetővé teszi a hidrogénkötések kialakulását, ami befolyásolja az olvadáspontját és oldhatóságát.
- Dibenzoil: Két ketoncsoportot tartalmaz egymás mellett. Nincs hidroxilcsoportja.
- Fizikai tulajdonságok:
- Olvadáspont: A benzoin olvadáspontja (körülbelül 137 °C) magasabb, mint a dibenzoilé (94-96 °C), a molekulák közötti hidrogénkötések miatt.
- Szín: A benzoin színtelen vagy fehér kristályos anyag, míg a dibenzoil jellegzetesen sárga. Ennek oka a dibenzoil kiterjedtebb konjugált pi-elektronrendszere.
- Oldhatóság: Mindkettő rosszul oldódik vízben, de jól oldódik szerves oldószerekben. A benzoin hidrogénkötés-donor és -akceptor jellege némileg eltérő oldhatósági profilt eredményezhet.
- Kémiai reaktivitás:
- Oxidáció/Redukció: A benzoin könnyen oxidálható dibenzoillá. A dibenzoil viszont tovább redukálható diollá.
- Specifikus reakciók: A benzoin részt vesz a benzoin kondenzációban, amelyben aldehidekből szintetizálódik. A dibenzoil a benzilsav átrendeződésben játszik kulcsszerepet, amely a benzoinra nem jellemző.
Ez az összehasonlítás jól mutatja, hogy egyetlen funkcionális csoport változása (hidroxilcsoportról ketonra) milyen drámai különbségeket eredményezhet a vegyületek tulajdonságaiban és kémiai viselkedésében.
Dibenzoil vs. Más diketonok
A dibenzoil egy alfa-diketon, azaz két karbonilcsoportja közvetlenül kapcsolódik egymáshoz. Más diketonok is léteznek, ahol a karbonilcsoportok elhelyezkedése eltérő lehet, és ez befolyásolja a reaktivitásukat.
- Alfa-diketonok (pl. bután-2,3-dion, más néven diacetil):
- Szerkezet: R–CO–CO–R’ típusú vegyületek. A dibenzoil esetében R és R’ fenilgyűrűk.
- Reaktivitás: Hasonlóan a dibenzoilhoz, az alfa-diketonok is részt vesznek a benzilsav átrendeződésben, amennyiben megfelelő szubsztituensek vannak jelen a migrációhoz. Fotokémiai aktivitásuk is lehet, bár a dibenzoil aromás gyűrűi miatt különösen hatékony fotoiniciátor.
- Alkalmazás: A diacetil például az élelmiszeriparban ízesítőszerként (vajíz) ismert, de fotokémiai tulajdonságai is vannak.
- Béta-diketonok (pl. acetilaceton):
- Szerkezet: R–CO–CH2–CO–R’ típusú vegyületek, ahol a két karbonilcsoportot egy metiléncsoport választja el.
- Reaktivitás: A béta-diketonok egyedi tulajdonsága a keto-enol tautoméria. Az enol forma stabilizálódik intramolekuláris hidrogénkötéssel. Emiatt rendkívül savasak a metiléncsoporton lévő hidrogének, és könnyen deprotonálhatók.
- Alkalmazás: Az acetilaceton és származékai fontos kelátképző ligandumok a koordinációs kémiában, és fémkomplexek előállítására használják őket.
- Gamma-diketonok (pl. hexán-2,5-dion):
- Szerkezet: R–CO–CH2–CH2–CO–R’ típusú vegyületek, ahol a két karbonilcsoportot két metiléncsoport választja el.
- Reaktivitás: A karbonilcsoportok távolabb vannak egymástól, így kevésbé befolyásolják egymás reaktivitását, mint az alfa- vagy béta-diketonok esetében. Gyakran gyűrűzárási reakciókban hasznosak, például pirrolok szintézisében.
Ez az összehasonlítás rávilágít arra, hogy a diketonok családján belül is jelentős különbségek vannak a szerkezet, a tulajdonságok és az alkalmazások tekintetében, attól függően, hogy a két karbonilcsoport milyen távolságra és milyen környezetben helyezkedik el egymástól. A dibenzoil különlegessége az alfa-diketon szerkezetében és az aromás gyűrűk jelenlétében rejlik, ami egyedülállóvá teszi a fotokémiai alkalmazások terén.